Clear Sky Science · he
מטבוליט מעי TMAO והאנלוגים המבניים שלו נקשרים לפיברינוגן ובכך מגבירים היווצרות קרישים: היגיון לסיכון לאטרוסקלרוזיס
מהכימיה במעי לקרישי דם
מה שמתרחש במעי אינו נשאר במעי. מחקר זה בוחן כיצד מולקולה זעירה שמיוצרת על ידי חיידקי מעי, הנקראת TMAO, יכולה לשנות את הדרך שבה קרישי דם נוצרים ומתמוססים. מאחר שקרישים בלתי תקינים נמצאים בבסיס התקפי לב ושבץ, הבנת הקישור החבוי הזה בין תזונה, חיידקי מעי, תרופות שכיחות ותהליך הקרישה מסייעת להסביר מדוע אצל חלק מהאנשים הסיכון הקרדיו-וסקולרי גבוה יותר — ואיפה אפשר להתערב טיפולים חדשים.
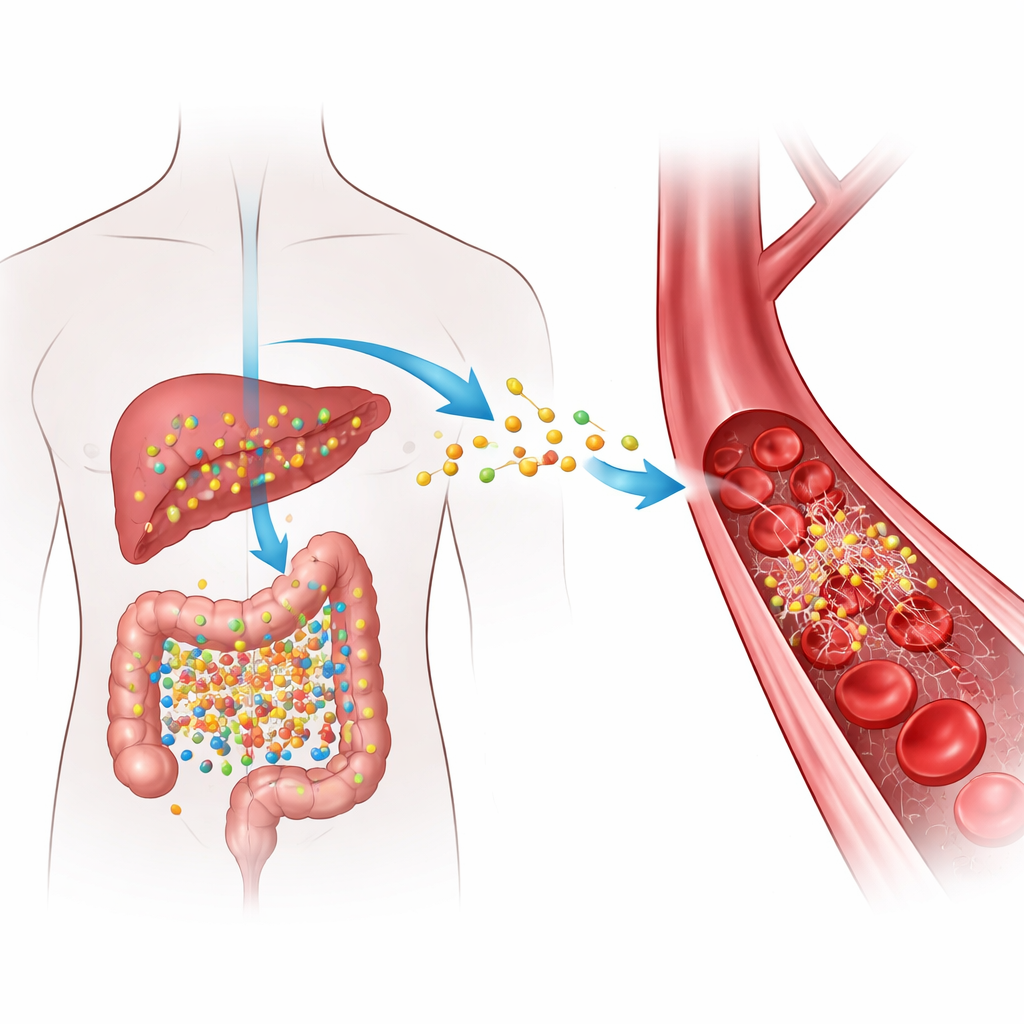
איך מזון יומיומי הופך לאות סיכון
כשאנו אוכלים מזונות עשירים ברכיבים מסוימים שנמצאים בבשר אדום, ביצים ומוצרי חלב עתירי שומן, חיידקי המעי ממירים רכיבים אלה לתרכובת ביניים שהכבד מטפל בה והופך ל‑TMAO. רמות גבוהות של TMAO בדם נמצאו שוב ושוב קשורות לעורקים סתומים ולהסתברות גבוהה יותר לקרישים מסוכנים, אך ה"איך" המדויק היה לא ברור. החוקרים התמקדו בפיברינוגן, חלבון מסיס ששוטף את הדם וכאשר הוא נחתך על ידי האנזים תרומבין, הוא הופך לפיברין — החומר הסיבי שעוזר לאטום פגיעות על ידי יצירת קרישים. הם שאלו האם TMAO מתקשר פיזית לפיברינוגן בדרך שעשויה להאיץ היווצרות קרישים או להקשות על פירוקם.
מהר יותר ועמידים יותר לפירוק
באמצעות מעקב אחרי תמיסות פיברינוגן שהופכות לפיברין עם הזמן, הראו החוקרים שהוספת TMAO מאיצה את הרכבת אבני הבניין הראשוניות של הקריש. ניסויי פיזור אור וצבע פלואורסצנטי חשפו שבלא TMAO, רק בערך שליש מהחלבון הצטרף לפיברילות לאחר פרק זמן מוגדר. עם עליית רמות ה‑TMAO, החלק הזה טיפס לעבר המרה מלאה, ותמונות מיקרוסקופ הראו רשת סיבים צפופה הרבה יותר. כשבחנו איך קרישי דם אלה מתפרקים, גילו תכונה מדאיגה נוספת: קרישים שנוצרו בנוכחות TMAO עמידים מאוד לעיכול על ידי אנזים חותך חלבונים, נשארים קומפקטיים ובעלי שלמות יחסית בעוד שקרישים רגילים מתפרקים כמעט לחלוטין.
אתר עגון מדויק על חלבון הקרישה
כדי לבדוק האם השפעה זו נובעת מהיקשרות ישירה, הצוות מדד שינויים בחום כשמכניסים TMAO לפיברינוגן ומצא ראיות ברורות שהשניים מתקשרים בעוצמה מתונה בריכוזים דומים לאלה שנצפים בקרב חולי לב. שיטות ספקטרוסקופיות הצביעו על כך שצורתו של הפיברינוגן נרפית במעט, חושפת שטחים דביקים יותר שמקלים על מגע חלבון‑חלבון. דגמי מחשב וסימולציות ארוכות מיפו היכן TMAO יושב על הפיברינוגן והדגישו אזור מסוים הידוע כאתר קשירת סידן beta1. כשאתר זה נתפס על ידי יוני סידן טבעיים, TMAO כבר לא יכול היה להפעיל את השפעתו, והיווצרות הקריש נראתה זהה בין נוכחות ליעדרות TMAO. זה מצביע על אתר beta1 כנקודת בקרה שמווסתת עד כמה מולקולות פיברינוגן ננעלות זו בזו בקלות.
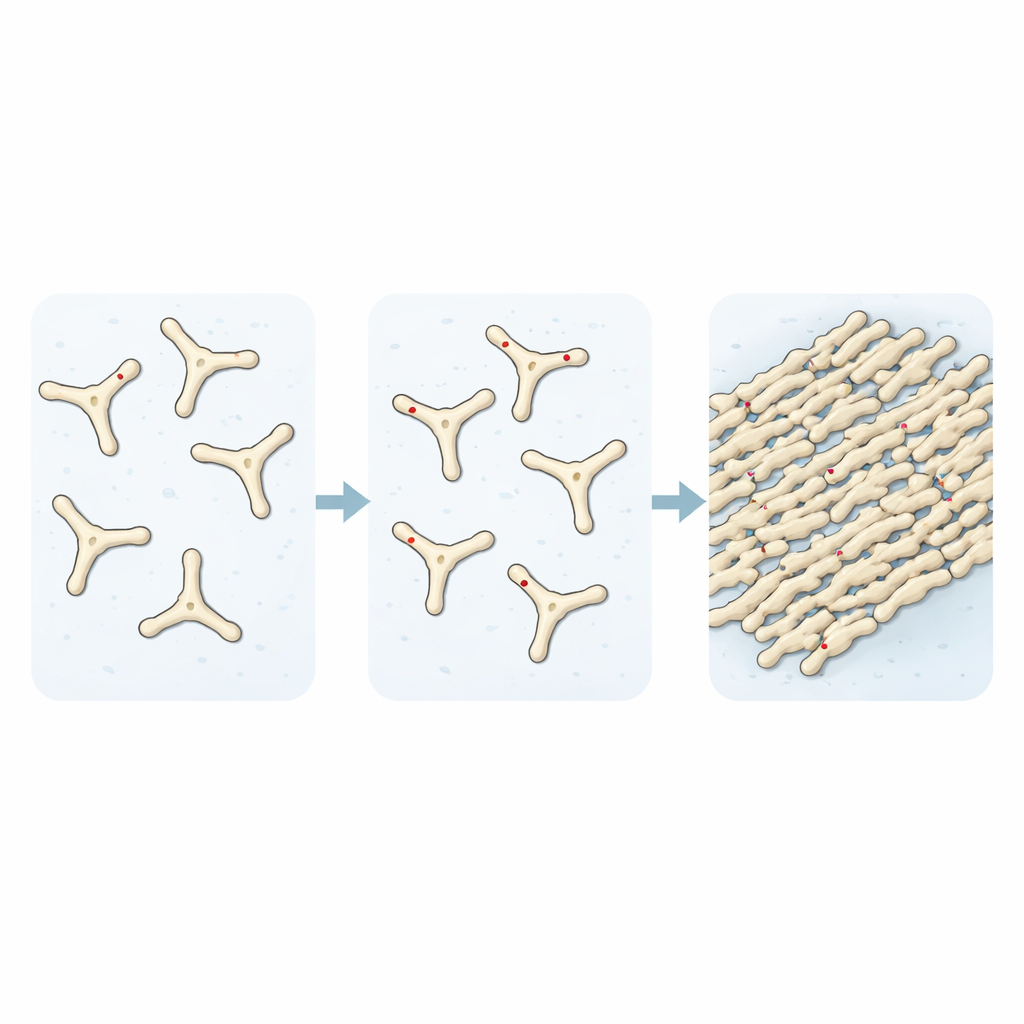
מטבוליטים של תרופות מצטרפים לסיפור
החוקרים שאלו אז האם מולקולות קטנות נוספות הדומות ל‑TMAO עשויות להתנהג באותו אופן. באמצעות מאגרי כימיה ותוכנת דוקינג, הם סרקו קבוצת תרכובות קרובות ובחרו שתיים שהן תוצרי פירוק N‑אוקסיד של תרופות נוגדות דיכאון ונגזרות ניקוטין נפוצות. בניסויים במבחנה גם מטבוליטים אלה הגבירו את מהירות והיקף הרכבת הפיברין ויצרו רשתות פיברין עבות וצפופות יותר, בדומה ל‑TMAO. ממצא זה מעלה את האפשרות שחלק מהתרופות, לאחר עיבוד בגוף, עלולות להטות בטעות את המאזן לעבר יצירת קרישים איתנים יותר על ידי פעולה על אותו "נקודת חם" בפיברינוגן.
מה זה אומר לסיכון ללב ולשבץ
בסיכום כל הראיות, העבודה חושפת שרשרת אירועים ישירה ממולקולות N‑אוקסיד שמקורן במעי או בתרופות לשינויים במבנה קרישי הדם. על‑ידי היקשרות לאתר ספציפי על הפיברינוגן, TMAO וקרוביו הכימיים דוחפים את החלבון לקונפורמציה שמעודדת היווצרות סיבים מהירה ויוצרת קרישים שקשה יותר לפרק. עבור הקורא הפשוט זה אומר שמוצרי לוואי מיקרוביאליים ומטבוליטים של תרופות עשויים בחשאי להקשיח את ה"שלד" של הקריש, ועוזרים להסביר מדוע רמות מוגברות של TMAO עוקבות אחרי סבירות גבוהה יותר לאירועים של חסימת עורקים. אתר beta1 על הפיברינוגן מתגלה כיעד מבטיח לטיפולים שמטרתם לרכך קרישים ולהפחית סיבוכים של אטרוסקלרוזיס מבלי לחסום את הקרישה לגמרי.
ציטוט: Singh, K., Kumari, A., Bakhshi, R. et al. Gut metabolite TMAO and its structural analogs bind to fibrinogen thereby enhancing clot formation: a rationale for atherosclerosis risk. Sci Rep 16, 13676 (2026). https://doi.org/10.1038/s41598-026-43910-0
מילות מפתח: מיקרוביוטת המעי, קרישי דם, TMAO, אטרוסקלרוזיס, פיברינוגן