Clear Sky Science · ru
Микробный метаболит TMAO и его структурные аналоги связываются с фибриногеном, усиливая образование тромбов: обоснование риска атеросклероза
От кишечных химикатов к тромбам
То, что происходит в кишечнике, не остается только в кишечнике. В этом исследовании изучается, как крошечная молекула, вырабатываемая кишечными бактериями и называемая TMAO, способна менять процесс образования и растворения кровяных сгустков. Поскольку патологические тромбы лежат в основе инфарктов и инсультов, понимание этой скрытой связи между питанием, микробами кишечника, распространенными лекарствами и свертыванием крови помогает объяснить, почему у одних людей риск сердечно-сосудистых событий выше, и где можно воздействовать новыми методами лечения.
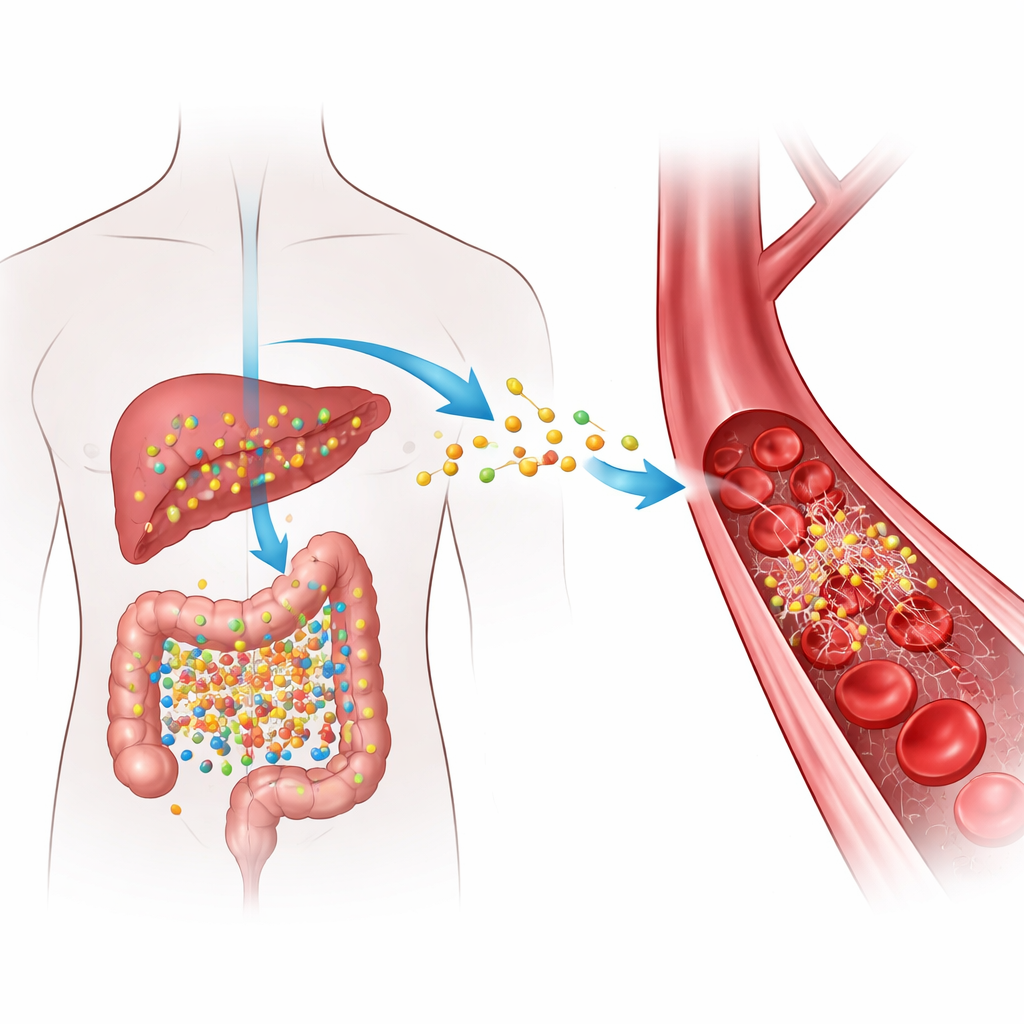
Как повседневная еда превращается в сигнал риска
Когда мы потребляем продукты, богатые определенными компонентами — например, красное мясо, яйца и жирные молочные продукты — кишечные бактерии превращают эти вещества в промежуточное соединение, которое затем печень окисляет до TMAO. Высокие уровни TMAO в крови неоднократно ассоциировались с закупоркой артерий и повышенным риском опасных тромбов, однако точный механизм оставался неясным. Авторы сосредоточились на фибриногене — растворимом белке, циркулирующем в крови, который при расщеплении тромбином превращается в фибрин — волокнистый материал, который заполняет повреждения, формируя сгустки. Они задали вопрос, взаимодействует ли TMAO физически с фибриногеном так, чтобы ускорять образование тромбов или затруднять их растворение.
Ускорение образования тромбов и их трудное расщепление
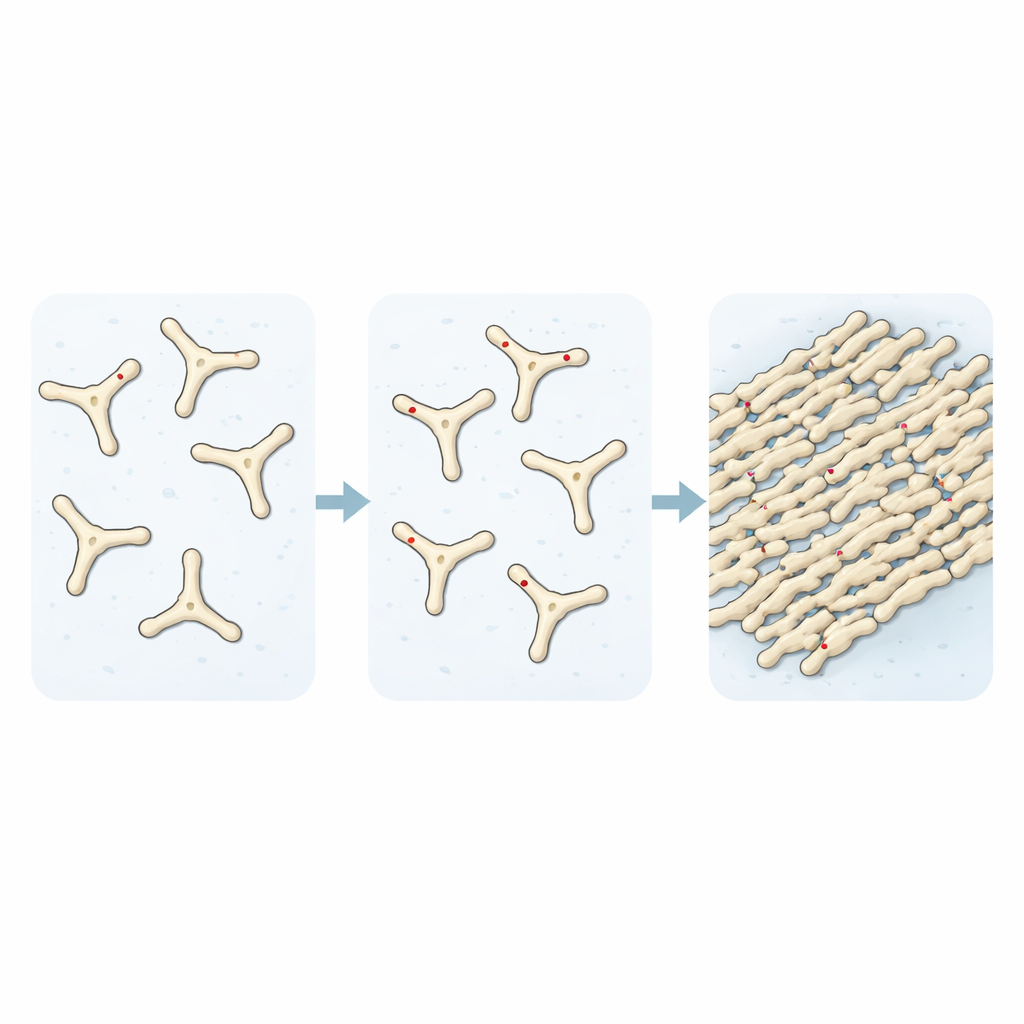
Отслеживая превращение растворов фибриногена в фибрин во времени, исследователи показали, что добавление TMAO ускоряет сборку ранних строительных блоков сгустков. Эксперименты с рассеянием света и флуоресцентными красителями показали, что без TMAO лишь около трети белка переходило в фибриллы за заданный период. С повышением концентрации TMAO эта доля приближалась к полному превращению, а микроскопические изображения демонстрировали гораздо более плотную сеть волокон. При изучении распада таких сгустков обнаружилось еще одно тревожное свойство: сгустки, образованные в присутствии TMAO, оказались сильно устойчивы к расщеплению протеазами, оставаясь компактными и в значительной степени неповрежденными, тогда как обычные сгустки почти полностью разрушались.
Точная посадочная область на свертывающем белке
Чтобы установить, связано ли это явление с прямым связыванием, команда измеряла тепловые изменения при смешивании TMAO с фибриногеном и обнаружила явные свидетельства взаимодействия умеренной силы при концентрациях, сопоставимых с таковыми у пациентов с сердечными заболеваниями. Методы спектроскопии указывали на то, что конформация фибриногена несколько ослабляется, открывая больше «липких» участков, благоприятствующих контакту белок–белок. Компьютерное моделирование и длительные симуляции показали, где именно располагается TMAO на молекуле фибриногена, и выделили специфическую область, известную как бета1-участок связывания кальция. Когда этот участок был занят природными ионами кальция, TMAO уже не оказывал своего эффекта, и образование сгустков не зависело от присутствия TMAO. Это указывает на бета1-участок как узел управления, который регулирует, насколько легко молекулы фибриногена сцепляются друг с другом.
Вовлечение метаболитов лекарств
Авторы затем поинтересовались, не проявят ли аналогичное поведение и другие малые молекулы, похожие на TMAO. Используя химические базы данных и программы для докинга, они отобрали набор родственных соединений и выделили два метаболита N-оксидного распада широко используемых антидепрессантов и препаратов, связанных с никотином. В пробирочных экспериментах эти метаболиты также ускоряли и усиливали сборку фибрина, формируя более толстые и плотные сети, схожие с эффектом TMAO. Это наблюдение допускает возможность того, что некоторые лекарственные средства, после преобразования в организме, могут тонко смещать равновесие в сторону более прочного образования сгустков, действуя на ту же «горячую точку» фибриногена.
Что это значит для риска инфаркта и инсульта
Сводя воедино все данные, работа выявляет прямую цепочку: от молекул N-оксида кишечного или фармакологического происхождения до изменений структуры тромбов. Связываясь с конкретным участком фибриногена, TMAO и его химические «родственники» переводят белок в конформацию, которая способствует быстрому образованию волокон и формирует сгустки, труднее поддающиеся разрушению. Для неспециалиста это означает, что некоторые микробные побочные продукты и метаболиты лекарств могут незаметно уплотнять «каркас» тромбов, что помогает объяснить, почему повышенные уровни TMAO коррелируют с большим риском закупорки артерий. Бета1-участок фибриногена предстает как перспективная цель для терапии, направленной на «смягчение» сгустков и снижение осложнений атеросклероза без полного блокирования свертывания крови.
Цитирование: Singh, K., Kumari, A., Bakhshi, R. et al. Gut metabolite TMAO and its structural analogs bind to fibrinogen thereby enhancing clot formation: a rationale for atherosclerosis risk. Sci Rep 16, 13676 (2026). https://doi.org/10.1038/s41598-026-43910-0
Ключевые слова: микробиота кишечника, кровяные сгустки, TMAO, атеросклероз, фибриноген