Clear Sky Science · fr
Le métabolite intestinal TMAO et ses analogues structuraux se lient à la fibrinogène, renforçant ainsi la formation de caillots : une justification du risque d’athérosclérose
Des produits chimiques intestinaux aux caillots sanguins
Ce qui se passe dans votre intestin ne reste pas confiné à l’intestin. Cette étude explore comment une petite molécule produite par les bactéries intestinales, appelée TMAO, peut modifier la façon dont les caillots sanguins se forment et se dégradent. Parce que des caillots anormaux sont à l’origine des infarctus et des AVC, comprendre ce lien caché entre alimentation, microbiote intestinal, médicaments courants et coagulation aide à expliquer pourquoi certaines personnes présentent un risque cardiovasculaire plus élevé — et où de nouveaux traitements pourraient intervenir.
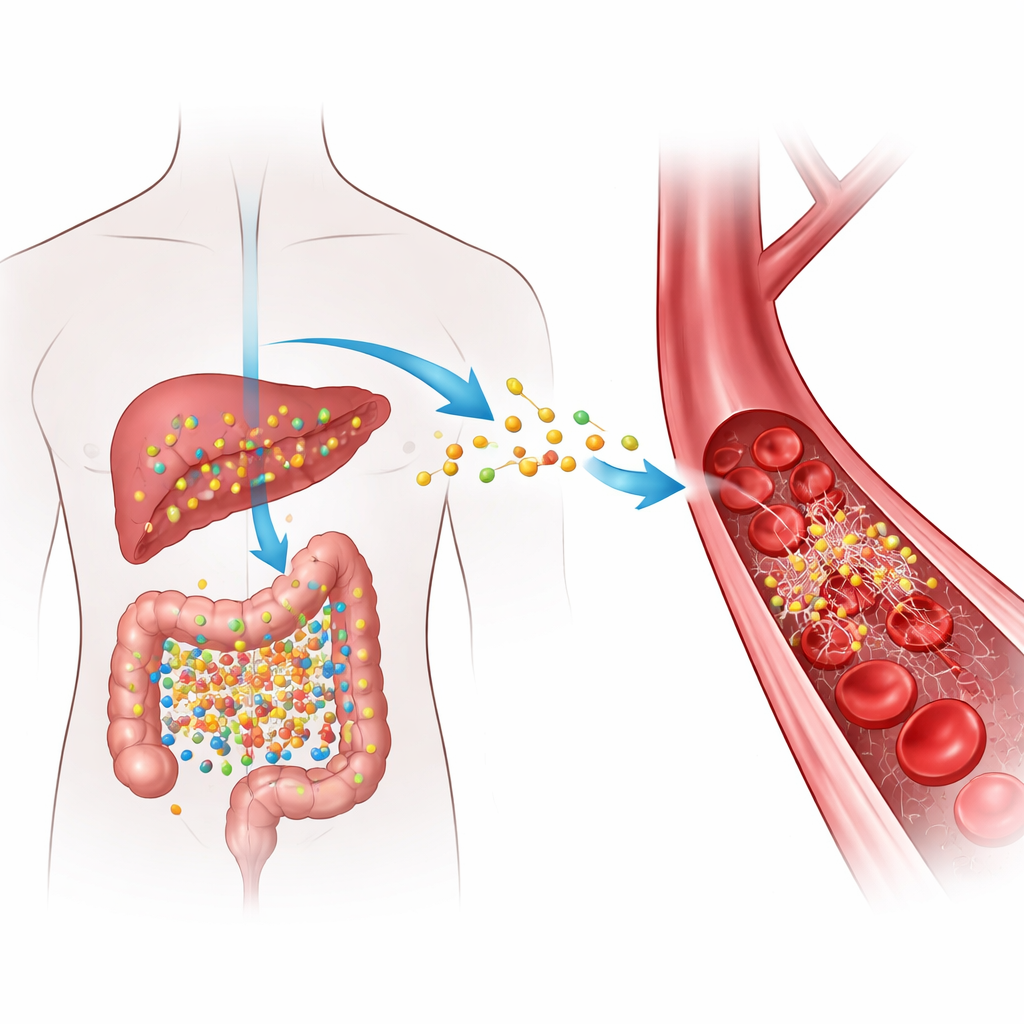
Comment des aliments quotidiens deviennent un signal de risque
Lorsque nous consommons des aliments riches en certains nutriments présents dans la viande rouge, les œufs et les produits laitiers gras, les bactéries intestinales transforment ces composants en un composé intermédiaire que le foie convertit ensuite en TMAO. Des taux élevés de TMAO dans le sang ont été à plusieurs reprises associés à l’obstruction des artères et à une probabilité accrue de caillots dangereux, mais le « comment » précis restait flou. Les auteurs se sont concentrés sur le fibrinogène, une protéine soluble circulant dans le sang qui, lorsqu’elle est clivée par l’enzyme thrombine, se transforme en fibrine — la matière filamenteuse qui aide à colmater les blessures en formant des caillots. Ils ont cherché à savoir si le TMAO interagit physiquement avec le fibrinogène d’une manière susceptible d’accélérer la formation des caillots ou de les rendre plus difficiles à dissoudre.
Des caillots plus rapides à se former et plus difficiles à dissoudre
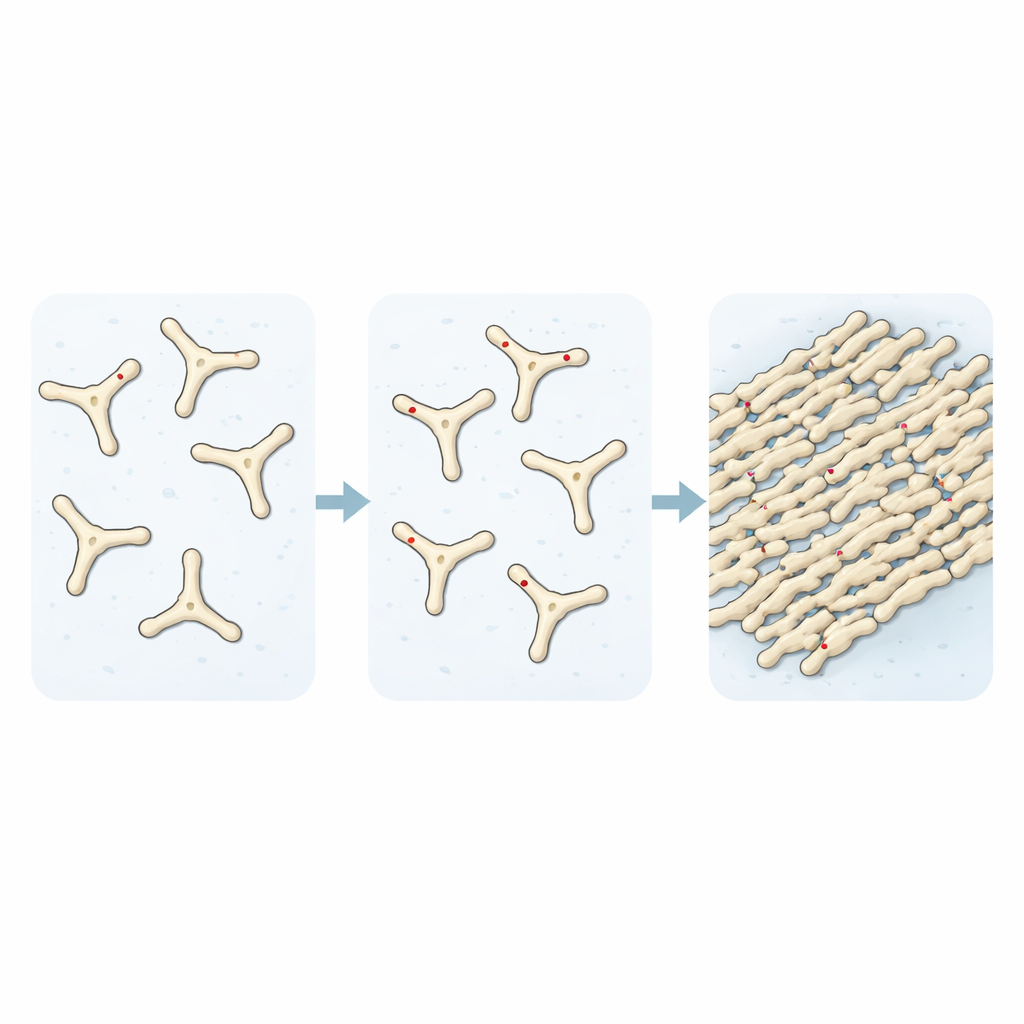
En suivant la conversion du fibrinogène en fibrine au fil du temps, les chercheurs ont montré que l’ajout de TMAO accélère l’assemblage des premiers éléments constitutifs des caillots. Des expériences de diffusion de la lumière et de colorants fluorescents ont révélé que, sans TMAO, seulement environ un tiers de la protéine s’était incorporé en fibrilles après une période donnée. Avec des niveaux croissants de TMAO, cette fraction tendait vers une conversion complète, et des images au microscope montraient un réseau de fibres beaucoup plus dense. Lorsqu’ils ont examiné la dégradation de ces caillots, ils ont observé une autre caractéristique inquiétante : les caillots formés en présence de TMAO résistaient fortement à la digestion par une enzyme protéolytique, restant compacts et largement intacts alors que les caillots normaux étaient presque complètement dégradés.
Un site d’ancrage précis sur la protéine de coagulation
Pour déterminer si cet effet provenait d’une liaison directe, l’équipe a mesuré les variations de chaleur lorsque le TMAO était mélangé au fibrinogène et a trouvé des preuves nettes d’une interaction de force modérée à des concentrations similaires à celles observées chez des personnes atteintes de maladies cardiaques. Des méthodes spectroscopiques ont indiqué que la conformation du fibrinogène s’assouplissait légèrement, exposant davantage de surfaces adhésives favorisant le contact protéine–protéine. La modélisation informatique et de longues simulations ont cartographié la position du TMAO sur le fibrinogène et mis en évidence une région spécifique connue sous le nom de site de liaison du calcium beta1. Lorsque ce site était occupé par des ions calcium naturels, le TMAO ne pouvait plus exercer son effet, et la formation du caillot était identique que le TMAO soit présent ou non. Cela désigne le site beta1 comme un point de contrôle qui module la facilité avec laquelle les molécules de fibrinogène se verrouillent entre elles.
Les métabolites de médicaments s’invitent dans l’histoire
Les auteurs se sont ensuite demandé si d’autres petites molécules ressemblant au TMAO pouvaient se comporter de manière similaire. En utilisant des bases de données chimiques et des logiciels d’arrimage, ils ont dépisté un ensemble de composés apparentés et sélectionné deux produits de dégradation N‑oxyde de médicaments antidépresseurs et de composés liés à la nicotine largement utilisés. En éprouvettes, ces métabolites ont également accéléré la vitesse et l’étendue de l’assemblage de la fibrine, et ont produit des réseaux de fibrine plus épais et plus denses, à l’instar du TMAO. Ce résultat suggère que certains médicaments, une fois métabolisés par l’organisme, pourraient subtilement faire pencher la balance vers une formation de caillots plus robuste en agissant sur le même point chaud du fibrinogène.
Quelles implications pour le risque de maladie cardiaque et d’AVC
En rassemblant toutes les preuves, ce travail révèle une chaîne d’événements directe reliant des molécules N‑oxyde d’origine intestinale ou médicamenteuse à des modifications de la structure des caillots sanguins. En se liant à un site spécifique du fibrinogène, le TMAO et ses cousins chimiques poussent la protéine vers une conformation qui favorise la formation rapide de fibres et produit des caillots plus difficiles à dégrader. Pour un lectorat non spécialiste, cela signifie que certains sous‑produits microbiens et métabolites médicamenteux peuvent discrètement durcir l’« échafaudage » des caillots, contribuant à expliquer pourquoi des niveaux élevés de TMAO sont associés à un risque accru d’événements obstruant les artères. Le site beta1 du fibrinogène apparaît comme une cible prometteuse pour des thérapies visant à assouplir les caillots et à réduire les complications liées à l’athérosclérose sans bloquer complètement la coagulation.
Citation: Singh, K., Kumari, A., Bakhshi, R. et al. Gut metabolite TMAO and its structural analogs bind to fibrinogen thereby enhancing clot formation: a rationale for atherosclerosis risk. Sci Rep 16, 13676 (2026). https://doi.org/10.1038/s41598-026-43910-0
Mots-clés: microbiote intestinal, caillots sanguins, TMAO, athérosclérose, fibrinogène