Clear Sky Science · nl
Darmmetabool TMAO en zijn structurele analogen binden aan fibrinogeen en versterken daardoor stolvorming: een rationale voor het risico op atherosclerose
Van darmchemicaliën naar bloedstolsels
Wat in uw darm gebeurt, blijft niet in uw darm. Deze studie onderzoekt hoe een klein molecuul dat door darmbacteriën wordt gemaakt, TMAO genaamd, de manier kan veranderen waarop bloedstolsels ontstaan en afbreken. Omdat afwijkende stolsels ten grondslag liggen aan hartaanvallen en beroertes, helpt inzicht in deze verborgen verbinding tussen voeding, darmmicroben, veelgebruikte medicijnen en stolling te verklaren waarom sommige mensen een hoger cardiovasculair risico lopen — en waar nieuwe behandelingen mogelijk kunnen ingrijpen.
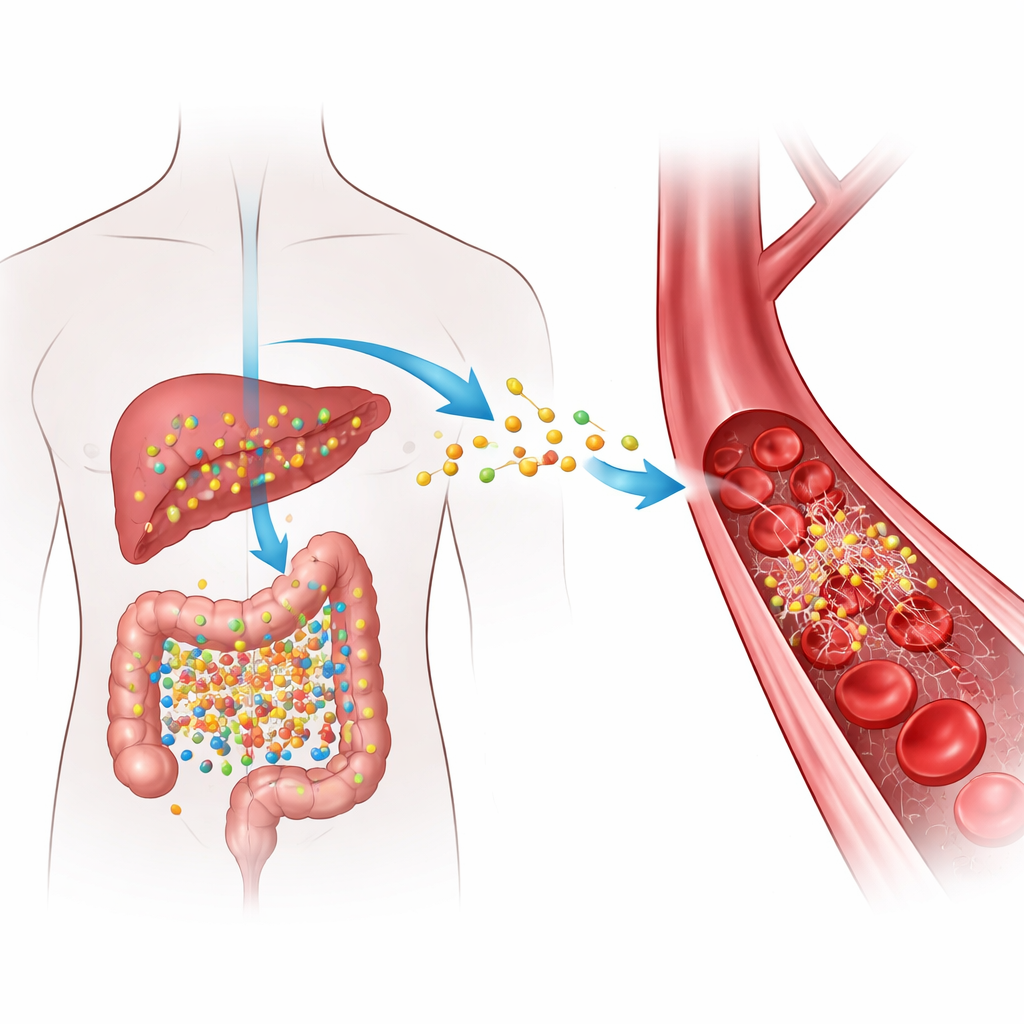
Hoe alledaags voedsel een risicosignaal wordt
Wanneer we voedingsmiddelen eten die rijk zijn aan bepaalde nutriënten uit rood vlees, eieren en vette zuivel, zetten darmbacteriën deze componenten om in een tussenproduct dat de lever vervolgens omzet in TMAO. Hoge TMAO-spiegels in het bloed zijn herhaaldelijk geassocieerd met verstopte aderen en een grotere kans op gevaarlijke stolsels, maar het precieze “hoe” was onduidelijk. De auteurs richtten zich op fibrinogeen, een oplosbaar eiwit dat in het bloed circuleert en, wanneer het door het enzym trombine wordt geknipt, verandert in fibrine — het draadvormige materiaal dat helpt verwondingen te dichten door stolsels te vormen. Ze onderzochten of TMAO fysiek met fibrinogeen interageert op een manier die stolsels sneller doet ontstaan of moeilijker oplosbaar maakt.
Stolsels sneller vormen en moeilijker te verwijderen
Door te volgen hoe oplossingen van fibrinogeen in de loop van de tijd in fibrine overgingen, lieten de onderzoekers zien dat toevoeging van TMAO de assemblage van vroege bouwstenen van stolsels versnelt. Lichtverstrooiings- en fluorescerende kleurstofexperimenten toonden aan dat zonder TMAO slechts ongeveer een derde van het eiwit na een bepaalde periode in fibrillen was gebonden. Met stijgende TMAO-niveaus steeg dat aandeel richting volledige conversie, en microscoopbeelden toonden een veel dichter web van vezels. Toen ze onderzochten hoe deze stolsels afbraken, vonden ze een andere zorgwekkende eigenschap: stolsels gevormd in aanwezigheid van TMAO waren sterk resistent tegen afbraak door een eiwitafbrekend enzym, ze bleven compact en grotendeels intact terwijl normale stolsels bijna volledig werden afgebroken.
Een precieze dockingplaats op het stollingseiwit
Om te bepalen of dit effect door directe binding werd veroorzaakt, maten de onderzoekers warmtetoenames toen TMAO met fibrinogeen werd gemengd en vonden duidelijk bewijs dat de twee met matige sterkte interageren bij concentraties vergelijkbaar met die bij mensen met hartziekten. Spectroscopiemethoden gaven aan dat de vorm van fibrinogeen lichtjes losser werd, waardoor meer kleverige plekken blootliggen die eiwit–eiwitcontact bevorderen. Computermodeling en lange simulaties brachten in kaart waar TMAO op fibrinogeen zit en wezen een specifieke regio aan die bekendstaat als de beta1-calciumbindingsplaats. Wanneer deze plaats bezet was door natuurlijke calciumionen, kon TMAO zijn effect niet meer uitoefenen, en leek de stolvorming hetzelfde ongeacht de aanwezigheid van TMAO. Dit wijst op de beta1-site als een regelpunt dat afstelt hoe gemakkelijk fibrinogeenmoleculen in elkaar vergrendelen.
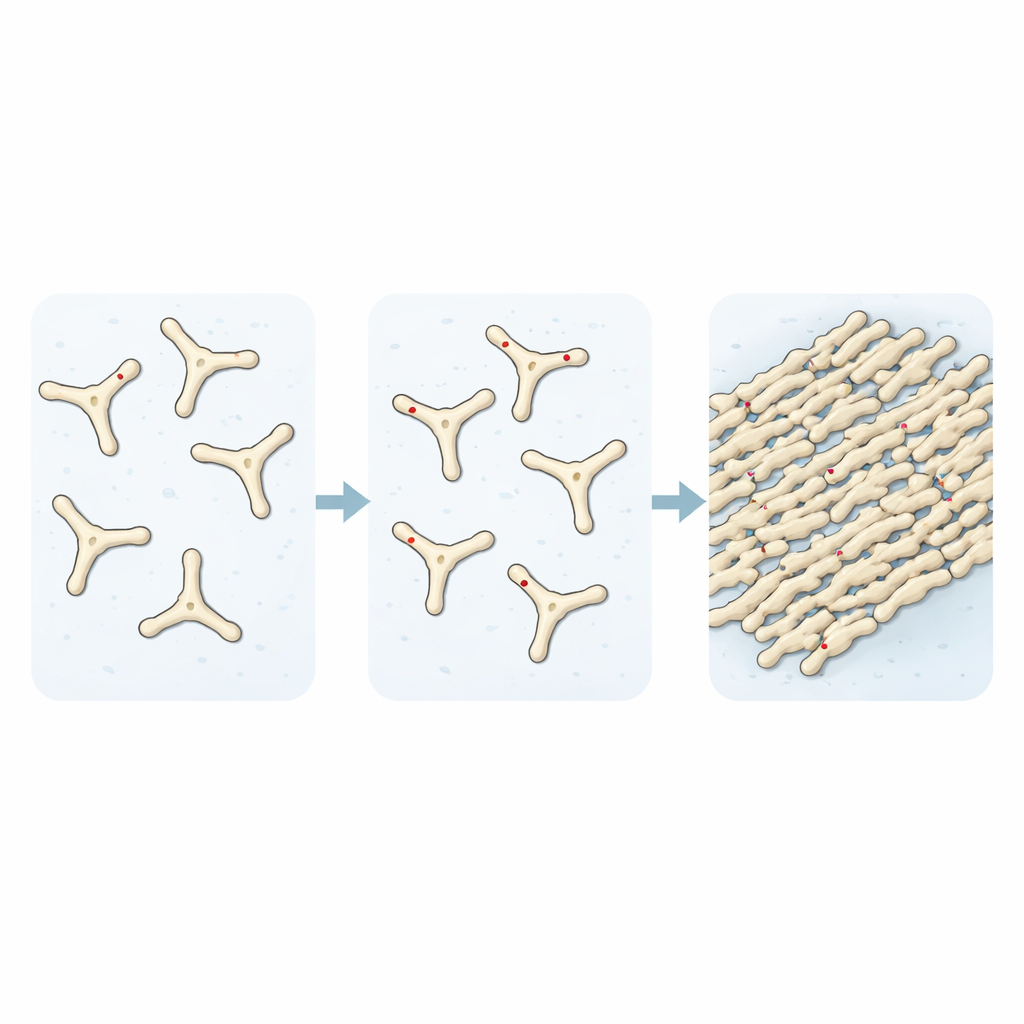
Geneesmiddelmetabolieten voegen zich bij het verhaal
De auteurs vroegen zich vervolgens af of andere kleine moleculen die op TMAO lijken zich op vergelijkbare wijze zouden kunnen gedragen. Met behulp van chemische databanken en dockingsoftware screenenden ze een reeks verwante verbindingen en selecteerden twee die N-oxide afbraakproducten zijn van wijdverbreid gebruikte antidepressiva en nicotine-gerelateerde medicijnen. In reageerbuisexperimenten versnelden deze metabolieten ook de snelheid en omvang van fibrineassemblage en gaven ze dikkere, dichtere fibrinenetwerken, heel vergelijkbaar met TMAO. Deze bevinding werpt de mogelijkheid op dat sommige geneesmiddelen, eenmaal door het lichaam verwerkt, subtiel de balans kunnen verschuiven richting robuustere stolvorming door op hetzelfde knooppunt in fibrinogeen in te werken.
Wat dit betekent voor hart- en beroerterisico
Als je al het bewijs samenvoegt, onthult het werk een directe keten van gebeurtenissen van darm- of geneesmiddelafgeleide N-oxidemoleculen naar veranderingen in de structuur van bloedstolsels. Door te binden aan een specifieke plaats op fibrinogeen, duwen TMAO en zijn chemische verwanten het eiwit in een conformatie die snelle vezelvorming bevordert en stolsels produceert die moeilijker af te breken zijn. Voor de leek betekent dit dat bepaalde microbieel geproduceerde bijproducten en geneesmiddelmetabolieten stilletjes het “skelet” van stolsels kunnen verharden, wat helpt verklaren waarom verhoogde TMAO-niveaus samenhangen met een grotere kans op aderverstoppende gebeurtenissen. De beta1-site op fibrinogeen komt naar voren als een veelbelovend doel voor therapieën die stolsels willen verzachten en complicaties van atherosclerose willen verminderen zonder de stolling volledig te blokkeren.
Bronvermelding: Singh, K., Kumari, A., Bakhshi, R. et al. Gut metabolite TMAO and its structural analogs bind to fibrinogen thereby enhancing clot formation: a rationale for atherosclerosis risk. Sci Rep 16, 13676 (2026). https://doi.org/10.1038/s41598-026-43910-0
Trefwoorden: darmmicrobioom, bloedstolsels, TMAO, atherosclerose, fibrinogeen