Clear Sky Science · es
El metabolito intestinal TMAO y sus análogos estructurales se unen a la fibrinógeno, aumentando así la formación de coágulos: una justificación del riesgo de aterosclerosis
De los químicos intestinales a los coágulos sanguíneos
Lo que ocurre en el intestino no se queda en el intestino. Este estudio explora cómo una molécula diminuta producida por bacterias intestinales, llamada TMAO, puede alterar la forma en que se forman y se degradan los coágulos sanguíneos. Dado que los coágulos anormales subyacen a infartos y accidentes cerebrovasculares, comprender este vínculo oculto entre la dieta, los microbios intestinales, medicamentos comunes y la coagulación ayuda a explicar por qué algunas personas presentan un mayor riesgo cardiovascular y dónde podrían intervenir nuevos tratamientos.
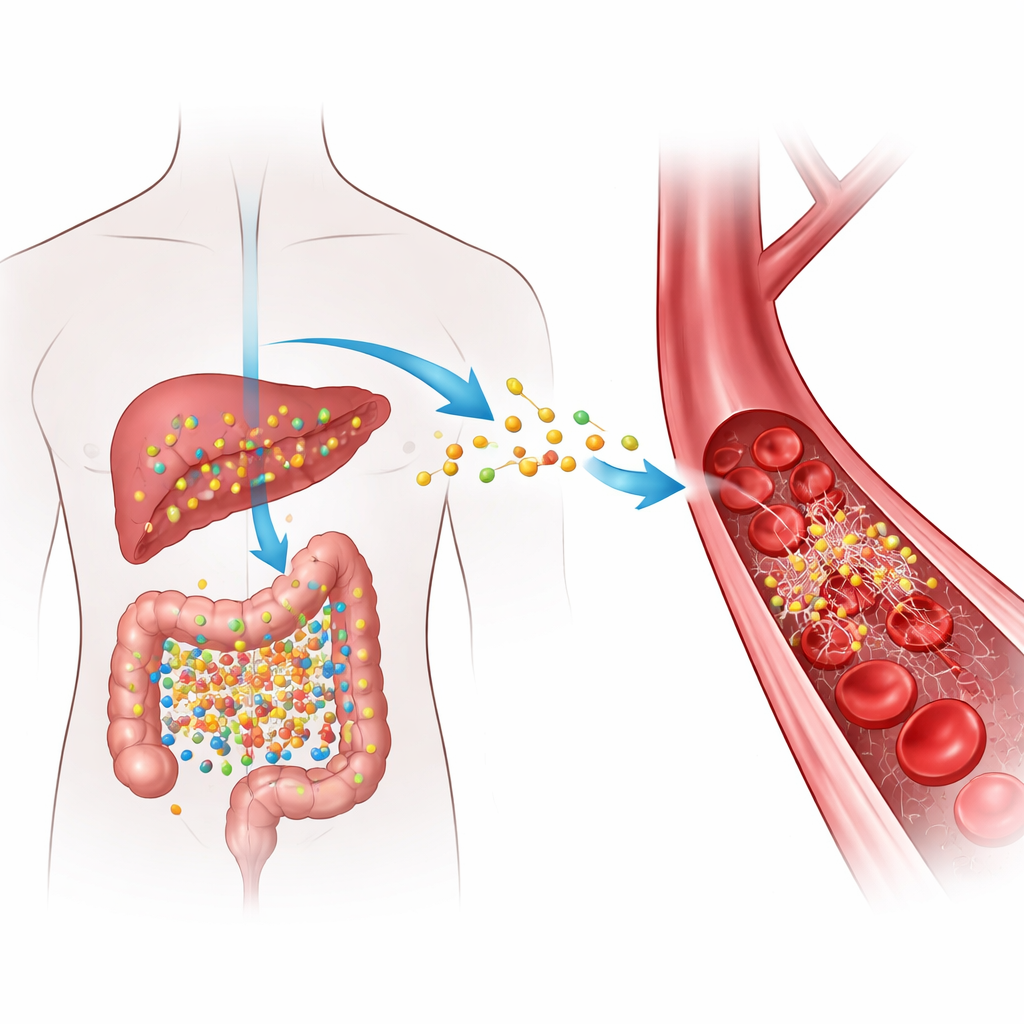
Cómo los alimentos cotidianos se convierten en una señal de riesgo
Cuando comemos alimentos ricos en ciertos nutrientes presentes en la carne roja, los huevos y los lácteos grasos, las bacterias intestinales convierten estos componentes en un compuesto intermedio que el hígado transforma en TMAO. Niveles altos de TMAO en la sangre se han asociado repetidamente con arterias obstruidas y una mayor probabilidad de coágulos peligrosos, pero el “cómo” exacto ha sido poco claro. Los autores se centraron en la fibrinógeno, una proteína soluble que circula en la sangre y que, al ser cortada por la enzima trombina, se convierte en fibrina—el material filamentoso que ayuda a sellar las lesiones formando coágulos. Preguntaron si el TMAO interacciona físicamente con la fibrinógeno de una manera que pueda hacer que los coágulos se formen más rápido o sean más difíciles de disolver.
Formando coágulos más rápido y más difíciles de eliminar
Siguiendo cómo soluciones de fibrinógeno se transforman en fibrina con el tiempo, los investigadores demostraron que añadir TMAO acelera el ensamblaje de los primeros bloques de construcción de los coágulos. Experimentos de dispersión de luz y con colorantes fluorescentes revelaron que, sin TMAO, solo alrededor de un tercio de la proteína se había incorporado a los filamentos tras un periodo determinado. Con niveles crecientes de TMAO, esa fracción ascendió hacia la conversión completa, y las imágenes al microscopio mostraron una red de fibras mucho más densa. Al examinar cómo se descomponen estos coágulos, encontraron otra característica preocupante: los coágulos formados en presencia de TMAO eran altamente resistentes a la digestión por una enzima que corta proteínas, permaneciendo compactos y en gran parte intactos mientras que los coágulos normales se degradaban casi por completo.
Un sitio de acoplamiento preciso en la proteína de la coagulación
Para ver si este efecto provenía de una unión directa, el equipo midió cambios de calor al mezclar TMAO con fibrinógeno y halló evidencia clara de que ambos interactúan con fuerza moderada a concentraciones similares a las observadas en personas con enfermedad cardiaca. Métodos espectroscópicos indicaron que la forma de la fibrinógeno se aflojaba ligeramente, exponiendo más parches adhesivos que favorecen el contacto proteína–proteína. El modelado por ordenador y largas simulaciones mapeó dónde se sitúa el TMAO en la fibrinógeno y destacó una región específica conocida como el sitio beta1 de unión al calcio. Cuando este sitio estaba ocupado por iones de calcio naturales, el TMAO ya no podía ejercer su efecto, y la formación del coágulo era la misma tanto si el TMAO estaba presente como si no. Esto apunta al sitio beta1 como un punto de control que regula cuán fácilmente las moléculas de fibrinógeno se ensamblan.
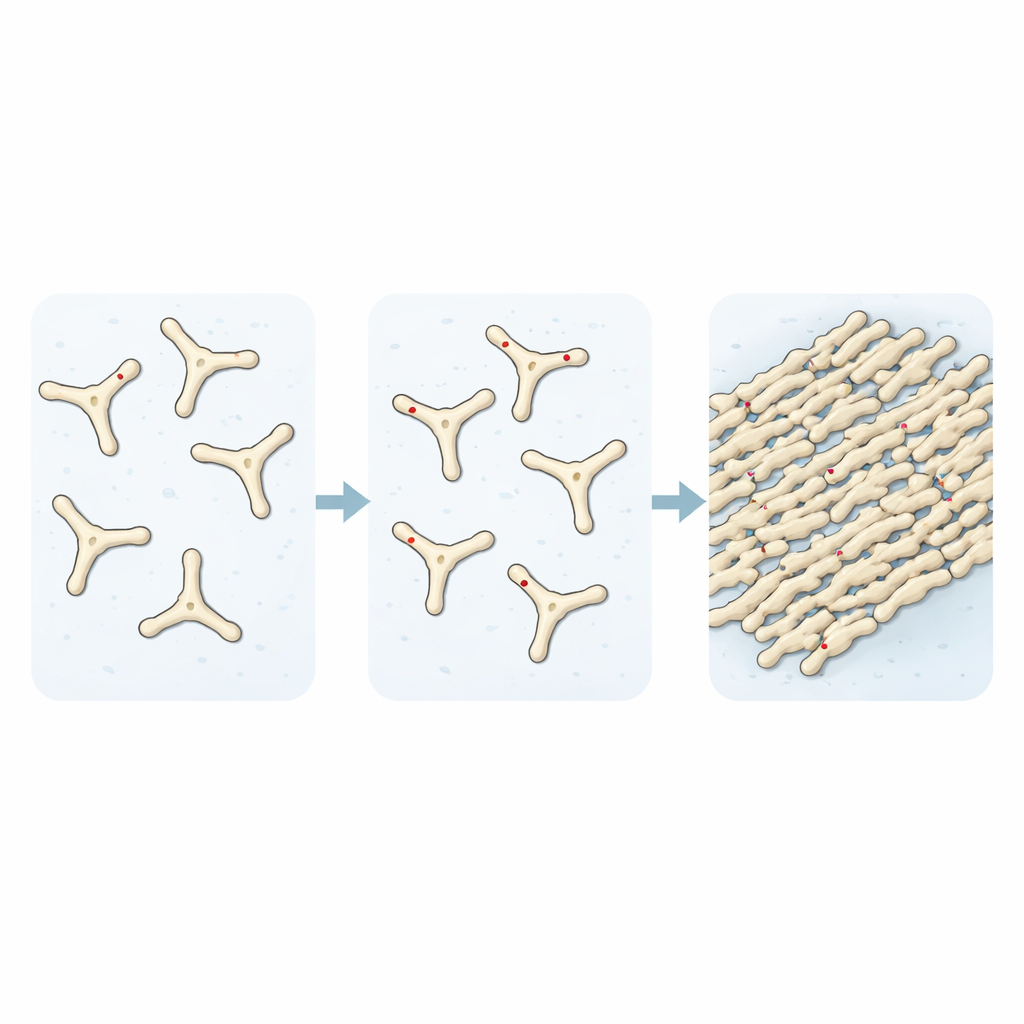
Metabolitos medicamentosos se suman a la historia
Los autores preguntaron luego si otras pequeñas moléculas que se parecen al TMAO podrían comportarse de forma similar. Usando bases de datos químicas y software de acoplamiento, seleccionaron un conjunto de compuestos relacionados y escogieron dos que son productos de ruptura N-óxido de fármacos antidepresivos y relacionados con la nicotina de uso generalizado. En experimentos de probeta, estos metabolitos también aumentaron la velocidad y el grado del ensamblaje de la fibrina, y produjeron redes de fibrina más gruesas y densas, muy parecidas al efecto del TMAO. Este hallazgo plantea la posibilidad de que algunos medicamentos, una vez procesados por el organismo, puedan inclinar sutilmente la balanza hacia la formación de coágulos más robustos actuando sobre el mismo punto crítico en la fibrinógeno.
Qué significa esto para el riesgo de infarto y accidente cerebrovascular
Poniendo toda la evidencia en conjunto, el trabajo revela una cadena directa de eventos desde moléculas N-óxido derivadas del intestino o de fármacos hasta cambios en la estructura de los coágulos sanguíneos. Al unirse a un sitio específico en la fibrinógeno, el TMAO y sus primos químicos empujan a la proteína hacia una conformación que favorece la formación rápida de fibras y produce coágulos más difíciles de descomponer. Para el lector general, esto significa que ciertos subproductos microbianos y metabolitos de fármacos pueden endurecer silenciosamente el “andamiaje” de los coágulos, ayudando a explicar por qué los niveles elevados de TMAO se asocian con una mayor probabilidad de acontecimientos que bloquean las arterias. El sitio beta1 en la fibrinógeno emerge como un objetivo prometedor para terapias dirigidas a ablandar los coágulos y reducir las complicaciones de la aterosclerosis sin bloquear la coagulación por completo.
Cita: Singh, K., Kumari, A., Bakhshi, R. et al. Gut metabolite TMAO and its structural analogs bind to fibrinogen thereby enhancing clot formation: a rationale for atherosclerosis risk. Sci Rep 16, 13676 (2026). https://doi.org/10.1038/s41598-026-43910-0
Palabras clave: microbioma intestinal, coágulos sanguíneos, TMAO, aterosclerosis, fibrinógeno