Clear Sky Science · zh
使用目标检测模型检测和分类具有姐妹染色单体粘连缺陷的染色体
为什么 DNA 的微小扭曲很重要
每次细胞分裂时,都必须将其遗传物质的精确拷贝传递下去。为了在适当的时刻之前将这些拷贝保持在一起,细胞依赖一种将成对染色体并列固定的分子“胶”。当这种“胶”失效时,染色体可能过早分离,导致基因组破裂、发育异常和癌症。这里描述的研究解决了一个非常实际的问题:如何在显微镜图像中自动识别这些微妙的粘连失效,使用现代人工智能代替疲惫的人眼。
染色体如何保持在一起
在细胞分裂前,每条染色体都会复制,形成两条相同的链,称为姐妹染色单体。一个名为 cohesin 的蛋白复合体帮助将这对姐妹保持配对,直到细胞准备拉开它们为止。如果 cohesin 或其辅助蛋白发生故障,姐妹染色单体可能过早分离。一个这样的辅助蛋白是 DDX11,这是一种解旋酶,其缺陷与一种罕见的人类疾病——华沙断裂综合征有关。在显微镜下,有粘连问题的细胞常表现为染色体的两条链在中心处异常张开或分裂,但将正常与异常形态区分开来需要耐心和判断。
为什么人工检查不够
传统上,研究人员将染色体摊在载玻片上、染色,然后手工对每个样本至少分类 50 到 100 条染色体。每条染色体按其形状及姐妹链的相对距离进行判断。这项工作既慢又主观,容易疲劳,从而增加了错误和研究者之间结果不一致的风险。同一研究团队早期的工作使用深度学习对单个染色体图像进行分类,但这些系统需要单独的软件步骤来从拥挤的显微图中裁切出单个染色体并剔除重叠干扰。额外的图像处理仍然高度依赖人工调整和清理,阻碍了真正的“一键”自动化。
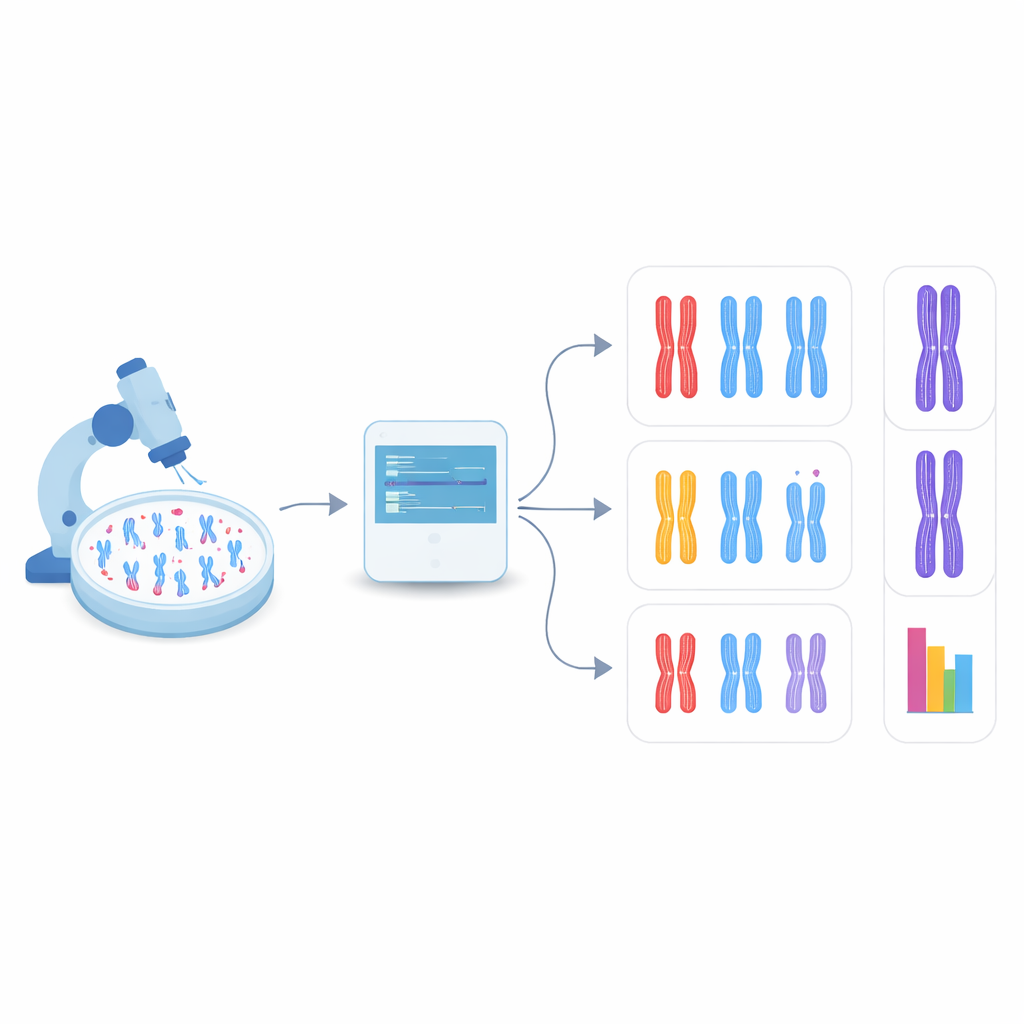
让计算机自行找到染色体
在这项新研究中,团队转向了目标检测——计算机视觉的一个分支,既能在单张图像中定位多个对象,也能对它们进行分类。他们关注一类快速且被广泛使用的模型 YOLO(You Only Look Once 的缩写)以及若干竞争方法。首先,他们通过基因工程构建了缺失 DDX11 的人源细胞,使其表现出明显的粘连问题,然后制备了这些细胞和正常细胞的染色体显微图像。图中每一条可见染色体都用矩形框标出,并被标注为三种形态之一:紧密配对、沿臂部分分离或在中心明显分裂。这些手工标注作为算法的训练资料。
教 AI 识别细微的形状差异
研究者对若干预训练的目标检测模型进行了微调,训练数据仅略多于一千条带标签的染色体,其余图像用于评估性能。他们比较了每个模型首先能否找到染色体,然后能否将其正确分到三种形态类别。被测试的系统中,名为 YOLOv8 的版本表现最好。它对近九成的染色体给出了与人工标签相符的判断,尽管类别之间的差别通常相当细微。重要的是,将该模型应用于正常和缺失 DDX11 的细胞图像时,YOLOv8 重现了人类专家观察到的关键生物学模式:有缺陷的细胞紧密配对的染色体显著减少,而中心明显分离的染色体明显增多。
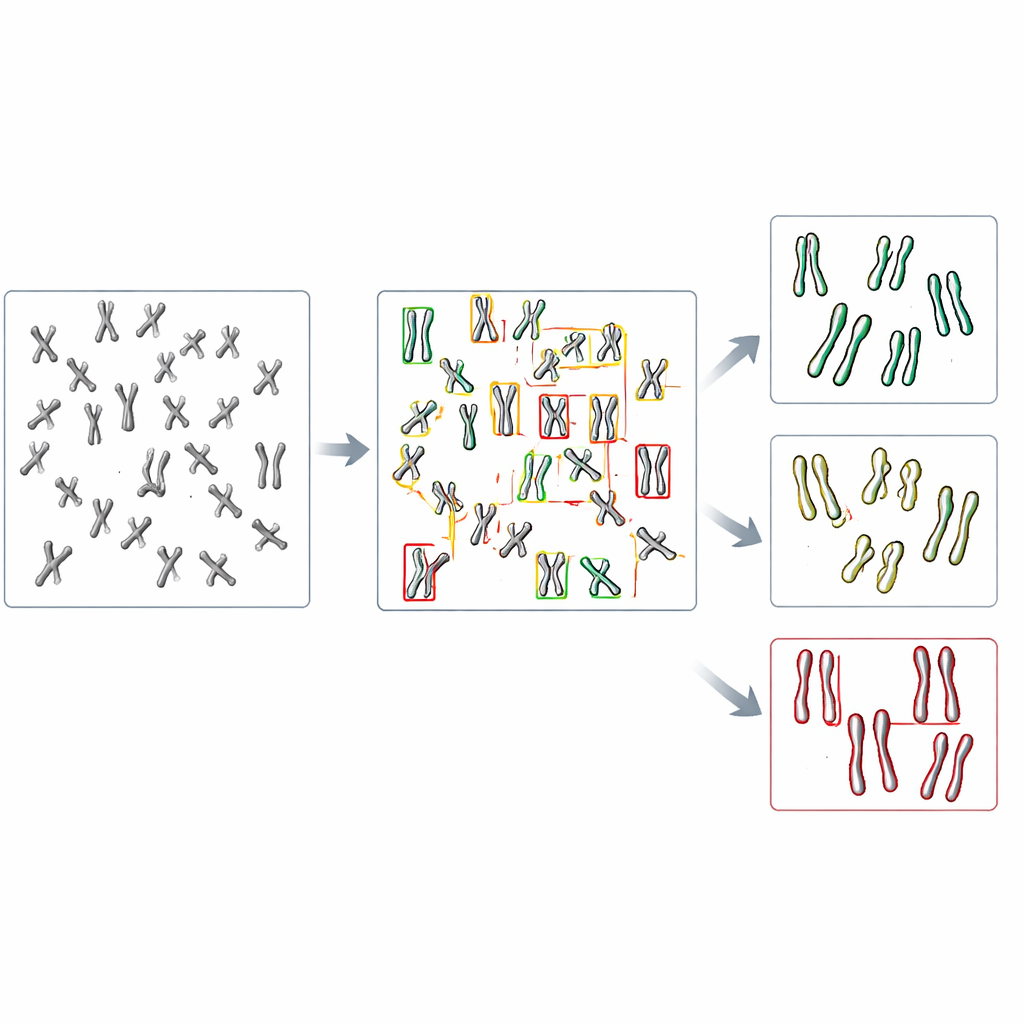
这对未来实验室工作的意义
这项研究表明,AI 模型能够扫描整张染色体摊片并在无需额外裁切或人工清理的情况下自动标注粘连缺陷。尽管在处理重叠染色体和边界形态时仍有改进空间,该方法已经能与早期那些需要更多人工干预的方法相媲美。由于这些模型是通过改造现有开源工具构建的,并可用适量图像集重新训练,那些没有深厚计算背景的实验室也可以开发出自己的定制系统。从长远看,类似策略可加速药物筛选、帮助比较大量基因突变体,并将应用范围扩展到对人类健康重要的其他细微染色体变化。
引用: Matsumoto, S., Sojo, M., Oshima, K. et al. Detection and classification of chromosomes with sister chromatid cohesion defects using object detection models. Sci Rep 16, 13719 (2026). https://doi.org/10.1038/s41598-026-43009-6
关键词: 染色体成像, 机器学习, 目标检测, 粘连缺陷, YOLOv8