Clear Sky Science · nl
Detectie en classificatie van chromosomen met defecten in zusterchromatide-cohesie met behulp van objectdetectiemodellen
Waarom kleine verwikkelingen in DNA ertoe doen
Elke keer dat een cel deelt, moet ze een exacte kopie van haar genetisch materiaal doorgeven. Om die kopieën samen te houden tot het juiste moment vertrouwen cellen op een moleculaire "lijm" die gepaarde chromosomen zij aan zij vasthoudt. Wanneer die lijm faalt, kunnen chromosomen te vroeg uiteen gaan, wat leidt tot gebroken genomen, ontwikkelingsstoornissen en kanker. De hier beschreven studie pakt een zeer praktisch probleem aan: hoe je deze subtiele lijmstoringen automatisch in microscoopbeelden kunt opsporen, met moderne kunstmatige intelligentie in plaats van vermoeide menselijke ogen.
Hoe chromosomen bij elkaar blijven
Voordat een cel zich deelt, wordt elk chromosoom gekopieerd zodat er twee identieke strengen zijn, bekend als zusterchromatiden. Een eiwitcomplex dat cohesin heet helpt deze zusters bij elkaar te houden totdat de cel ze wil uit elkaar trekken. Als cohesin of zijn hulpverlenende eiwitten niet goed werken, kunnen de zusters te vroeg uit elkaar drijven. Een van die hulpstoffen is DDX11, een DNA-opwikkel-enzyme waarvan defecten gekoppeld zijn aan een zeldzame menselijke aandoening die Warsaw Breakage-syndroom heet. Onder de microscoop tonen cellen met cohesieproblemen vaak chromosomen waarvan de twee strengen vreemd open of in het midden gespleten lijken te zijn, maar het onderscheid tussen normale en abnormale vormen vergt geduld en oordeel.
Waarom handmatige controles niet volstaan
Traditioneel spreiden onderzoekers chromosomen op een objectglaasje, kleuren ze in en classificeren dan per monster handmatig minstens 50 tot 100 exemplaren. Elk chromosoom wordt beoordeeld op vorm en hoe ver de zusterstrengen uit elkaar lijken te staan. Dit werk is traag, subjectief en vermoeiend, wat het risico op fouten en inconsistente resultaten tussen wetenschappers vergroot. Eerdere inspanningen door dezelfde onderzoeksgroep gebruikten deep learning om individuele chromosoomafbeeldingen te classificeren, maar die systemen vereisten aparte softwarestappen om losse chromosomen uit drukke microscoopbeelden te knippen en om verwarrende overlappingen te verwijderen. Die extra beeldverwerking bleef sterk afhankelijk van handmatige afstemming en opruiming, waardoor echte "druk-op-de-knop"-automatisering werd geblokkeerd.
Het de computer zelf laten vinden van chromosomen
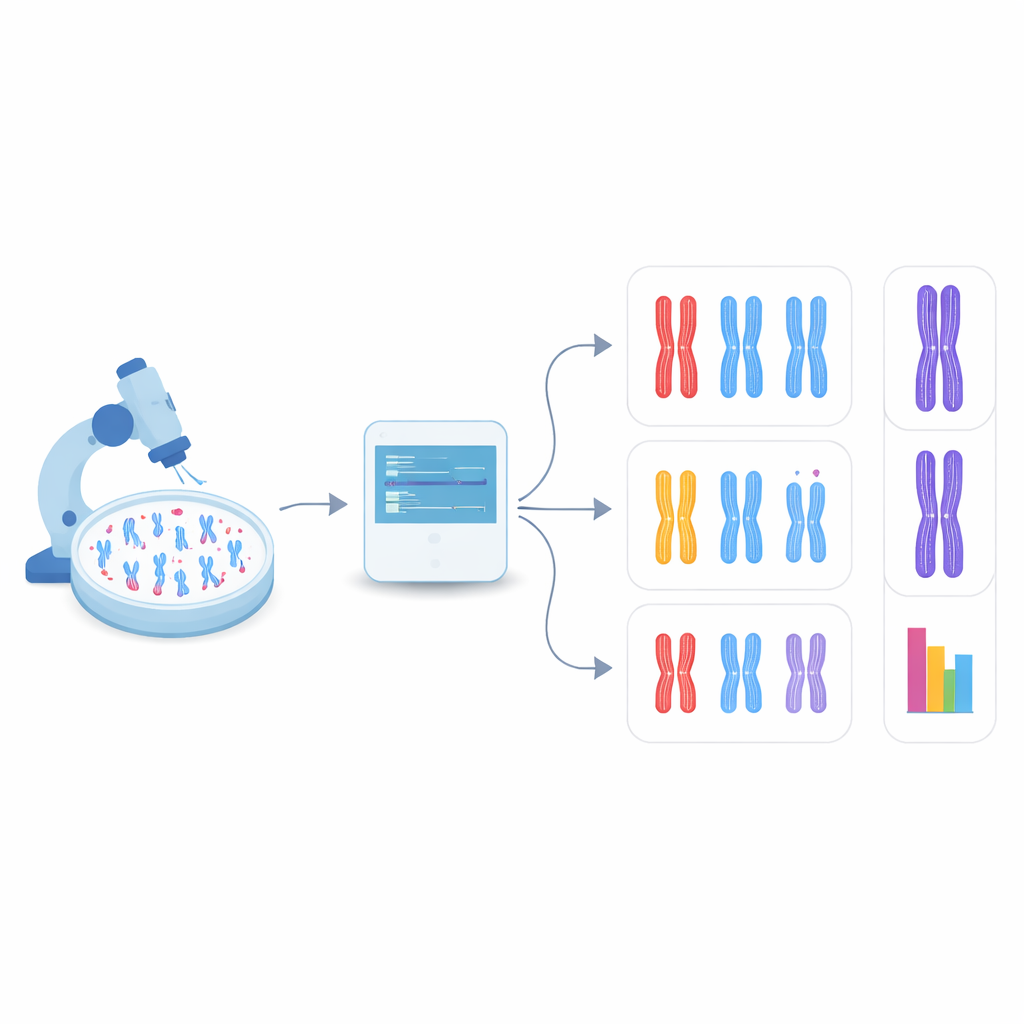
In de nieuwe studie wendde het team zich tot objectdetectie, een tak van computer vision die zowel veel objecten in een enkel beeld kan vinden als categoriseren. Ze concentreerden zich op een familie van snelle, veelgebruikte modellen genaamd YOLO (kort voor "You Only Look Once") en enkele concurrerende methoden. Eerst creëerden ze een testsysteem door menselijke cellen te maken die DDX11 missen en daardoor sterke cohesieproblemen tonen, en vervolgens microscoopbeelden van hun chromosomen te bereiden naast die van normale cellen. Elk zichtbaar chromosoom in deze beelden werd omkaderd met een rechthoek en gelabeld als een van drie vormtypes: strak gekoppeld, gedeeltelijk gescheiden langs de armen, of duidelijk in het midden gespleten. Deze handgemaakte labels dienden als leermateriaal voor de algoritmen.
AI leren subtiele vormverschillen te zien
De onderzoekers finetuneden verschillende voorgetrainde objectdetectiemodellen op iets meer dan duizend gelabelde chromosomen, waarbij ze andere beelden reserveerden om de prestatie te controleren. Ze vergeleken hoe goed elk model chromosomen eerst überhaupt kon vinden en vervolgens toewijzen aan de juiste van de drie vormcategorieën. Onder de geteste systemen presteerde een versie genaamd YOLOv8 het best. Het kwam bijna negen van de tien keer overeen met menselijke labels, zelfs wanneer de verschillen tussen categorieën vaak vrij subtiel waren. Belangrijk is dat, toegepast op beelden van normale en DDX11-deficiënte cellen, YOLOv8 het sleutelbiologische patroon reproduceerde dat menselijke experts zien: de defecte cellen hadden veel minder strak gekoppelde chromosomen en veel meer met duidelijk gescheiden zusterstrengen.
Wat dit betekent voor toekomstig laboratoriumwerk
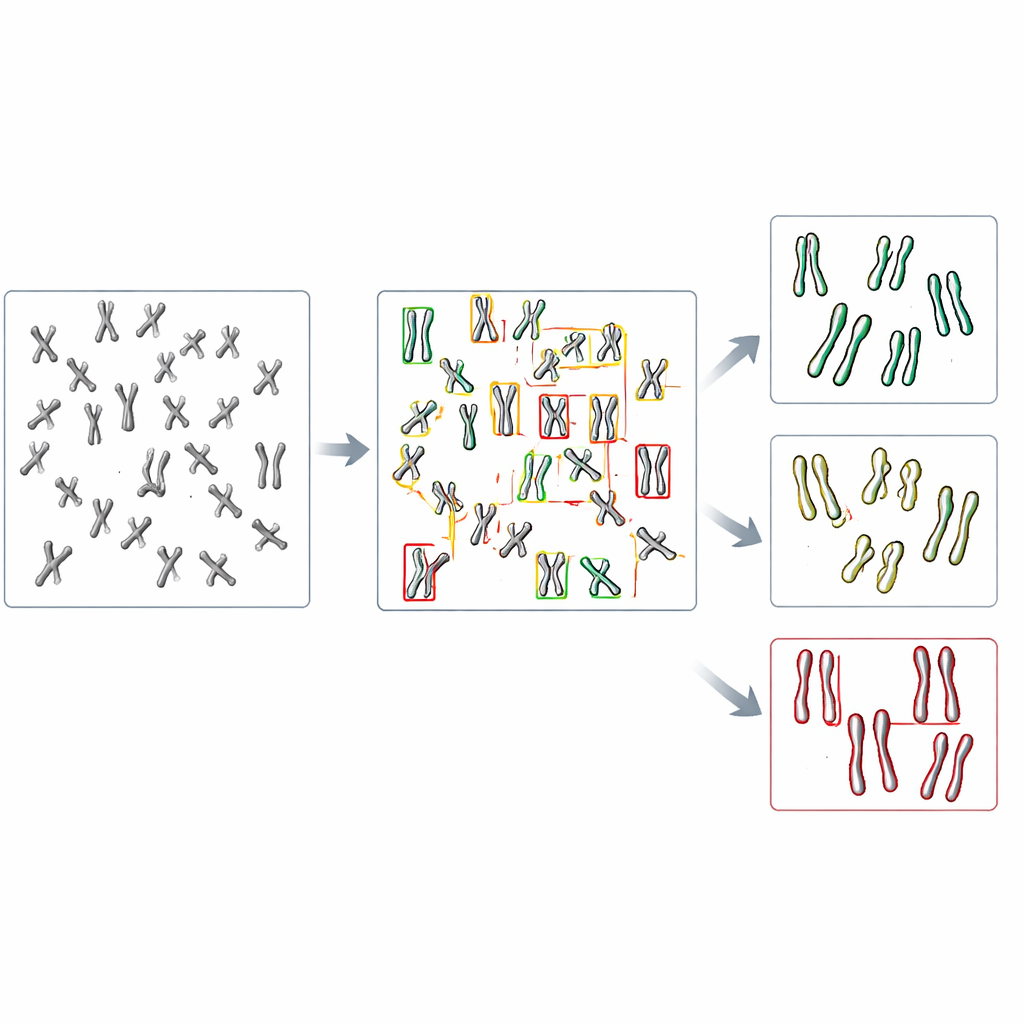
De studie toont aan dat een AI-model volledige chromosoomspreidingen kan scannen en automatisch cohesiedefecten kan signaleren zonder extra bijsnijdstappen of handmatige opschoning. Hoewel er nog ruimte is voor verbetering—vooral bij overlappende chromosomen en grensgevallen—benadert de aanpak al eerdere methoden die meer menselijke tussenkomst vereisten. Omdat de modellen zijn gebouwd door bestaande open-source tools aan te passen en met bescheiden afbeeldingssets opnieuw getraind kunnen worden, zouden laboratoria zonder diepe computerexpertise hun eigen aangepaste systemen kunnen ontwikkelen. Op de lange termijn kunnen vergelijkbare strategieën het screenen van geneesmiddelen versnellen, helpen bij het vergelijken van veel genetische mutanten en zich uitstrekken voorbij cohesie naar andere subtiele chromosoomveranderingen die van belang zijn voor de menselijke gezondheid.
Bronvermelding: Matsumoto, S., Sojo, M., Oshima, K. et al. Detection and classification of chromosomes with sister chromatid cohesion defects using object detection models. Sci Rep 16, 13719 (2026). https://doi.org/10.1038/s41598-026-43009-6
Trefwoorden: chromosoombeeldvorming, machine learning, objectdetectie, cohesiedefecten, YOLOv8