Clear Sky Science · fr
Détection et classification des chromosomes présentant des défauts de cohésion des chromatides sœurs à l’aide de modèles de détection d’objets
Pourquoi de petits enchevêtrements d’ADN comptent
Chaque fois qu’une cellule se divise, elle doit transmettre une copie exacte de son matériel génétique. Pour maintenir ces copies ensemble jusqu’au bon moment, les cellules s’appuient sur une “colle” moléculaire qui maintient les chromosomes appariés côte à côte. Lorsque cette colle fait défaut, les chromosomes peuvent se séparer trop tôt, entraînant des génomes fragmentés, des troubles du développement et des cancers. L’étude décrite ici s’attaque à un problème très concret : comment repérer automatiquement ces défaillances subtiles de la colle dans des images au microscope, en utilisant l’intelligence artificielle moderne plutôt que la vigilance fatiguée d’observateurs humains.
Comment les chromosomes restent ensemble
Avant qu’une cellule ne se divise, chaque chromosome est copié de sorte qu’il existe deux brins identiques, appelés chromatides sœurs. Une machinerie protéique nommée cohésine aide à maintenir ces sœurs appariées jusqu’à ce que la cellule soit prête à les séparer. Si la cohésine ou ses protéines auxiliaires dysfonctionnent, les chromatides sœurs peuvent s’éloigner trop tôt. Parmi ces auxiliaires figure DDX11, une hélicase d’ADN dont les défauts sont liés à une maladie humaine rare appelée syndrome de rupture de Varsovie. Au microscope, les cellules présentant des problèmes de cohésion montrent souvent des chromosomes dont les deux brins sont anormalement ouverts ou séparés au centre, mais distinguer les formes normales des formes anormales exige patience et jugement.
Pourquoi les contrôles manuels ne suffisent pas
Traditionnellement, les chercheurs étalent les chromosomes sur une lame, les colorent, puis classent au moins 50 à 100 d’entre eux par échantillon à la main. Chaque chromosome est jugé d’après sa forme et l’écartement apparent de ses chromatides sœurs. Ce travail est lent, subjectif et propice à la fatigue, ce qui augmente le risque d’erreurs et d’incohérences entre scientifiques. Des travaux antérieurs du même groupe utilisaient l’apprentissage profond pour classer des images individuelles de chromosomes, mais ces systèmes exigeaient des étapes logicielles séparées pour découper des chromosomes isolés à partir d’images micrographiques encombrées et pour écarter les chevauchements confus. Ce traitement additionnel des images dépendait encore fortement d’un réglage et d’un nettoyage humains, empêchant une véritable automatisation « bouton-poussoir ».
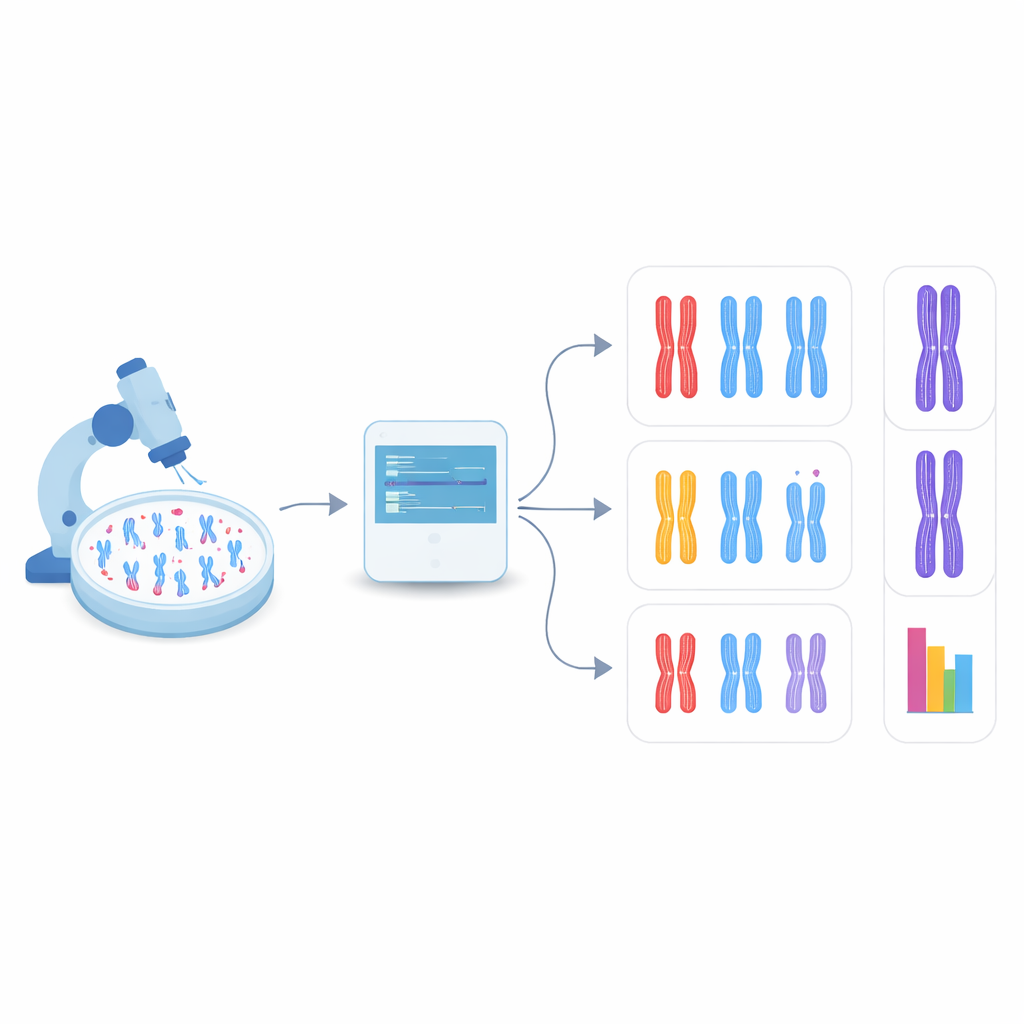
Laisser l’ordinateur trouver les chromosomes lui-même
Dans la nouvelle étude, l’équipe s’est tournée vers la détection d’objets, une branche de la vision par ordinateur capable à la fois de localiser et de catégoriser plusieurs éléments dans une seule image. Ils se sont concentrés sur une famille de modèles rapides et largement utilisés appelés YOLO (pour « You Only Look Once ») ainsi que sur plusieurs méthodes concurrentes. D’abord, ils ont créé un système-test en modifiant des cellules humaines dépourvues de DDX11 et montrant donc de forts problèmes de cohésion, puis en préparant des images de microscope de leurs chromosomes ainsi que de ceux de cellules normales. Chaque chromosome visible dans ces images a été encadré et étiqueté selon l’un des trois types de forme : étroitement apparié, partiellement séparé le long des bras, ou clairement fendu au centre. Ces annotations manuelles ont servi de matériel d’apprentissage pour les algorithmes.
Apprendre à l’IA à percevoir des différences de forme subtiles
Les chercheurs ont affiné plusieurs modèles de détection d’objets pré-entraînés sur un peu plus d’un millier de chromosomes étiquetés, en réservant d’autres images pour l’évaluation des performances. Ils ont comparé la capacité de chaque modèle à d’abord détecter les chromosomes, puis à les classer correctement parmi les trois catégories de forme. Parmi les systèmes testés, une version appelée YOLOv8 s’est révélée la meilleure. Elle correspondait correctement aux annotations humaines pour près de neuf chromosomes sur dix, même si les différences entre catégories étaient souvent très subtiles. Fait important, appliqué à des images de cellules normales et de cellules déficientes en DDX11, YOLOv8 a reproduit le schéma biologique clé observé par des experts humains : les cellules défectueuses présentaient beaucoup moins de chromosomes étroitement appariés et beaucoup plus de chromatides clairement séparées.
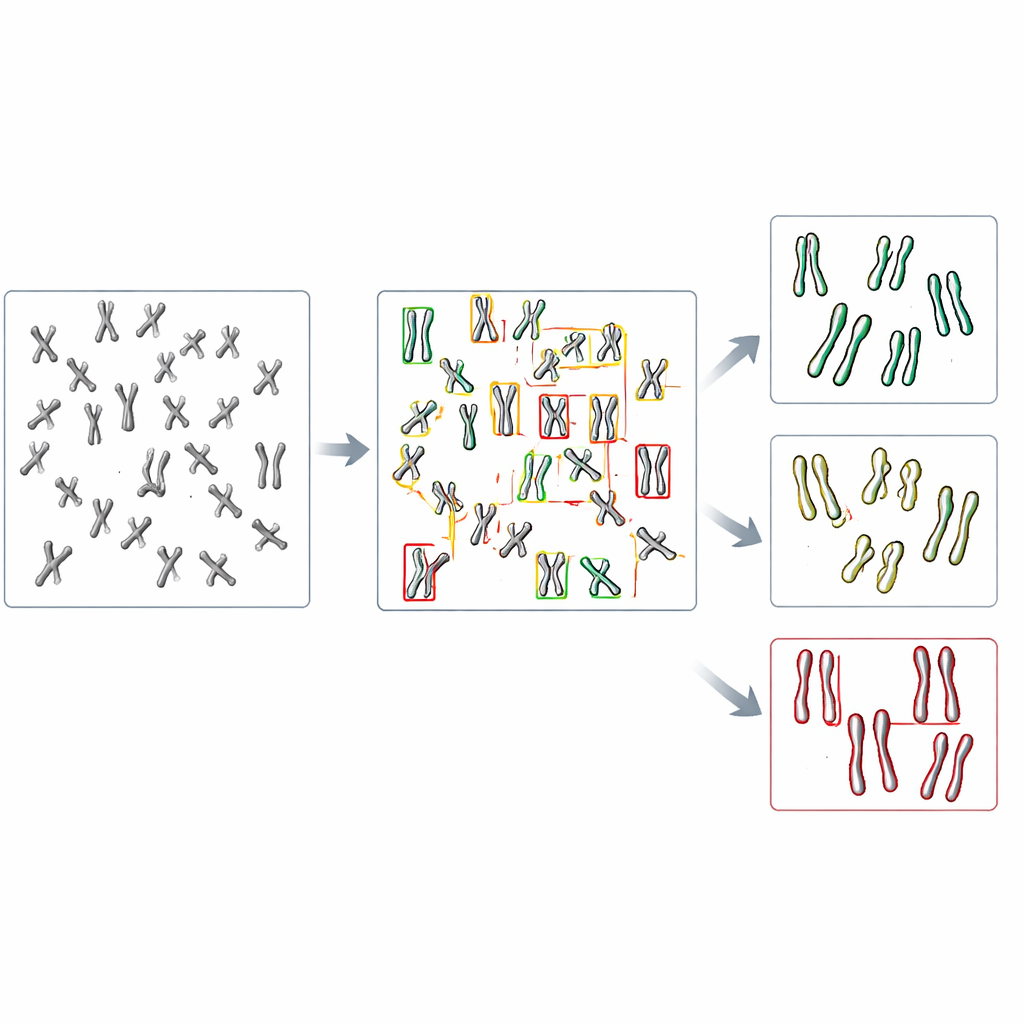
Ce que cela signifie pour le travail en laboratoire à l’avenir
L’étude montre qu’un modèle d’IA peut balayer des étalements chromosomiques complets et signaler automatiquement des défauts de cohésion sans étapes supplémentaires de recadrage ni nettoyage manuel. S’il reste des marges d’amélioration — notamment pour les chromosomes qui se chevauchent et les formes limites —, l’approche rivalise déjà avec des méthodes antérieures qui nécessitaient davantage d’intervention humaine. Parce que les modèles ont été construits en adaptant des outils open source existants et peuvent être réentraînés avec des jeux d’images modestes, des laboratoires sans expertise informatique approfondie pourraient développer leurs propres systèmes sur mesure. À terme, des stratégies similaires pourraient accélérer le criblage de médicaments, aider à comparer de nombreux mutants génétiques et s’étendre au-delà de la cohésion à d’autres altérations délicates des chromosomes importantes pour la santé humaine.
Citation: Matsumoto, S., Sojo, M., Oshima, K. et al. Detection and classification of chromosomes with sister chromatid cohesion defects using object detection models. Sci Rep 16, 13719 (2026). https://doi.org/10.1038/s41598-026-43009-6
Mots-clés: imagerie des chromosomes, apprentissage automatique, détection d’objets, défauts de cohésion, YOLOv8