Clear Sky Science · pl
Wykrywanie i klasyfikacja chromosomów z defektami spójności chromatyd siostrzanych za pomocą modeli detekcji obiektów
Dlaczego drobne skręty w DNA mają znaczenie
Za każdym razem, gdy komórka się dzieli, musi przekazać dokładną kopię swojego materiału genetycznego. Aby utrzymać te kopie razem aż do właściwego momentu, komórki polegają na molekularnym „kleju”, który trzyma sparowane chromosomy obok siebie. Gdy ten klej zawodzi, chromosomy mogą rozdzielić się zbyt wcześnie, co prowadzi do uszkodzeń genomu, zaburzeń rozwojowych i raka. Opisane tutaj badanie zajmuje się bardzo praktycznym problemem: jak automatycznie wykrywać te subtelne awarie kleju na obrazach mikroskopowych, używając nowoczesnej sztucznej inteligencji zamiast zmęczonych ludzkich oczu.
Jak chromosomy pozostają razem
Przed podziałem komórki każdy chromosom zostaje skopiowany, więc pojawiają się dwa identyczne włókna, zwane chromatydami siostrzanymi. Maszyna białkowa o nazwie kohezyna pomaga utrzymać te siostry w parze, aż komórka będzie gotowa je rozdzielić. Jeśli kohezyna lub jej białkowi pomocnicy zawodzą, siostry mogą oddalić się od siebie zbyt wcześnie. Jednym z takich pomocników jest DDX11, enzym rozwijający DNA, którego defekty powiązano z rzadkim schorzeniem ludzkim zwanym zespołem Warsaw Breakage. Pod mikroskopem komórki z problemami spójności często pokazują chromosomy, których dwa włókna są dziwnie otwarte lub rozdzielone w środku, ale odróżnienie normalnych od nieprawidłowych kształtów wymaga cierpliwości i oceny eksperta.
Dlaczego ręczne kontrole nie wystarczają
Tradycyjnie badacze rozprowadzają chromosomy na preparacie, barwią je, a następnie klasyfikują co najmniej 50–100 chromosomów na próbkę ręcznie. Każdy chromosom ocenia się po kształcie i tym, jak daleko od siebie wydają się jego chromatydy. Ta praca jest wolna, subiektywna i łatwo się nią zmęczyć, co zwiększa ryzyko błędów i niejednolitych wyników między naukowcami. Wcześniejsze wysiłki tej samej grupy badawczej stosowały głębokie uczenie do klasyfikacji pojedynczych obrazów chromosomów, ale te systemy wymagały oddzielnych kroków programowych do wycinania pojedynczych chromosomów z zatłoczonych zdjęć mikroskopowych i odrzucania mylących nakładających się fragmentów. To dodatkowe przetwarzanie obrazów wciąż w dużej mierze zależało od ludzkiego dostrajania i sprzątania, blokując prawdziwą automatyzację „na przycisk”.
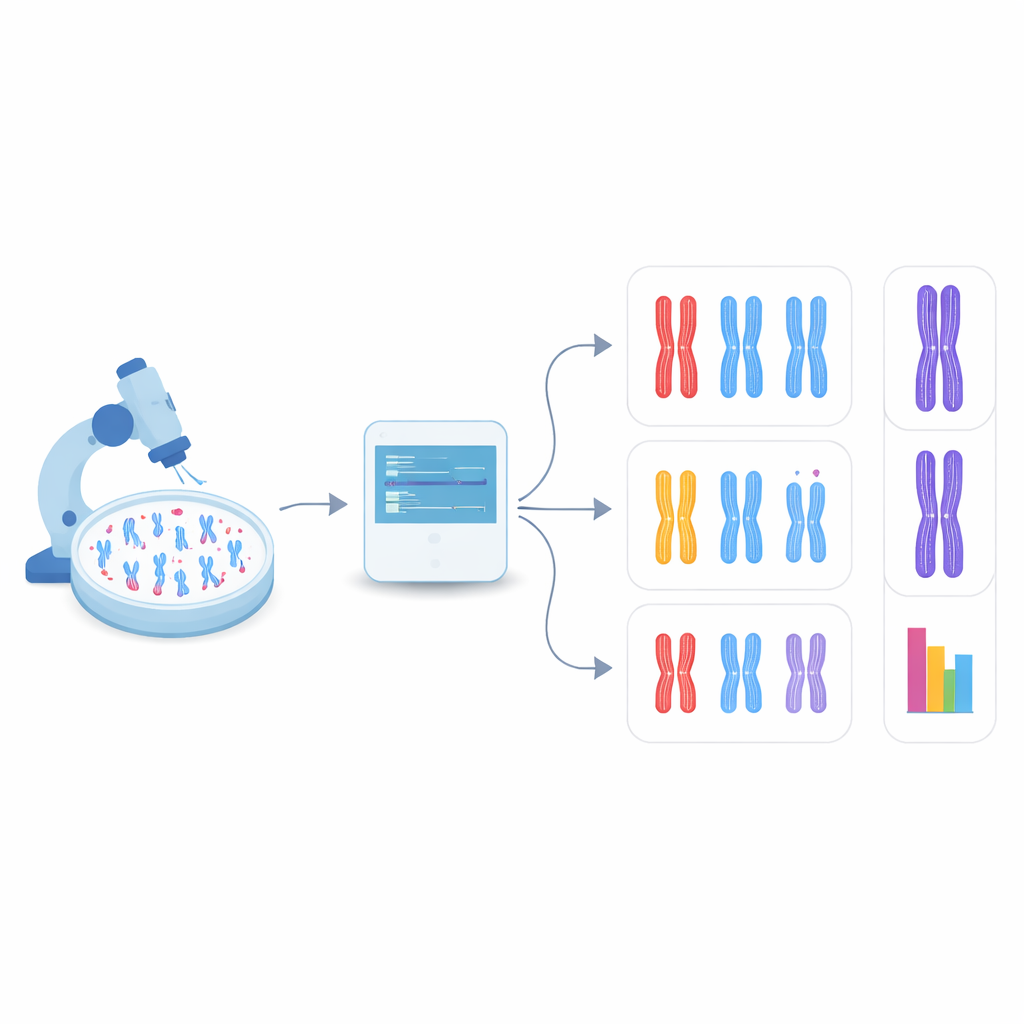
Pozwolić komputerowi samemu znaleźć chromosomy
W nowym badaniu zespół zwrócił się ku detekcji obiektów, gałęzi widzenia komputerowego, która potrafi jednocześnie znaleźć i sklasyfikować wiele obiektów na pojedynczym obrazie. Skupili się na rodzinie szybkich, szeroko stosowanych modeli zwanych YOLO (od „You Only Look Once”) oraz kilku konkurencyjnych metodach. Najpierw stworzyli system testowy, modyfikując komórki ludzkie pozbawione DDX11, które wykazują silne problemy ze spójnością, a następnie przygotowali obrazy mikroskopowe ich chromosomów oraz chromosomów z komórek normalnych. Każdy widoczny chromosom na tych obrazach został obrysowany ramką i oznaczony jako jeden z trzech typów kształtu: ściśle sparowany, częściowo rozdzielony wzdłuż ramion lub wyraźnie rozdzielony w środku. Te ręcznie przygotowane etykiety posłużyły jako materiał szkoleniowy dla algorytmów.
Nauczanie SI rozróżniania subtelnych różnic kształtu
Badacze dopracowali kilka wcześniej wytrenowanych modeli detekcji obiektów na nieco ponad tysiącu oznaczonych chromosomów, rezerwując inne obrazy do sprawdzania wydajności. Porównali, jak dobrze każdy model potrafi najpierw w ogóle znaleźć chromosomy, a potem przypisać je do właściwej z trzech kategorii kształtu. Spośród testowanych systemów najlepiej wypadła wersja o nazwie YOLOv8. Zgadzała się z ludzkimi etykietami dla prawie dziewięciu na dziesięć chromosomów, mimo że różnice między kategoriami często były bardzo subtelne. Co ważne, po zastosowaniu do obrazów z komórek normalnych i pozbawionych DDX11, YOLOv8 odtworzył kluczowy wzorzec biologiczny widziany przez ekspertów: komórki z defektem miały znacznie mniej ściśle sparowanych chromosomów i znacznie więcej z wyraźnie rozdzielonymi chromatydami.
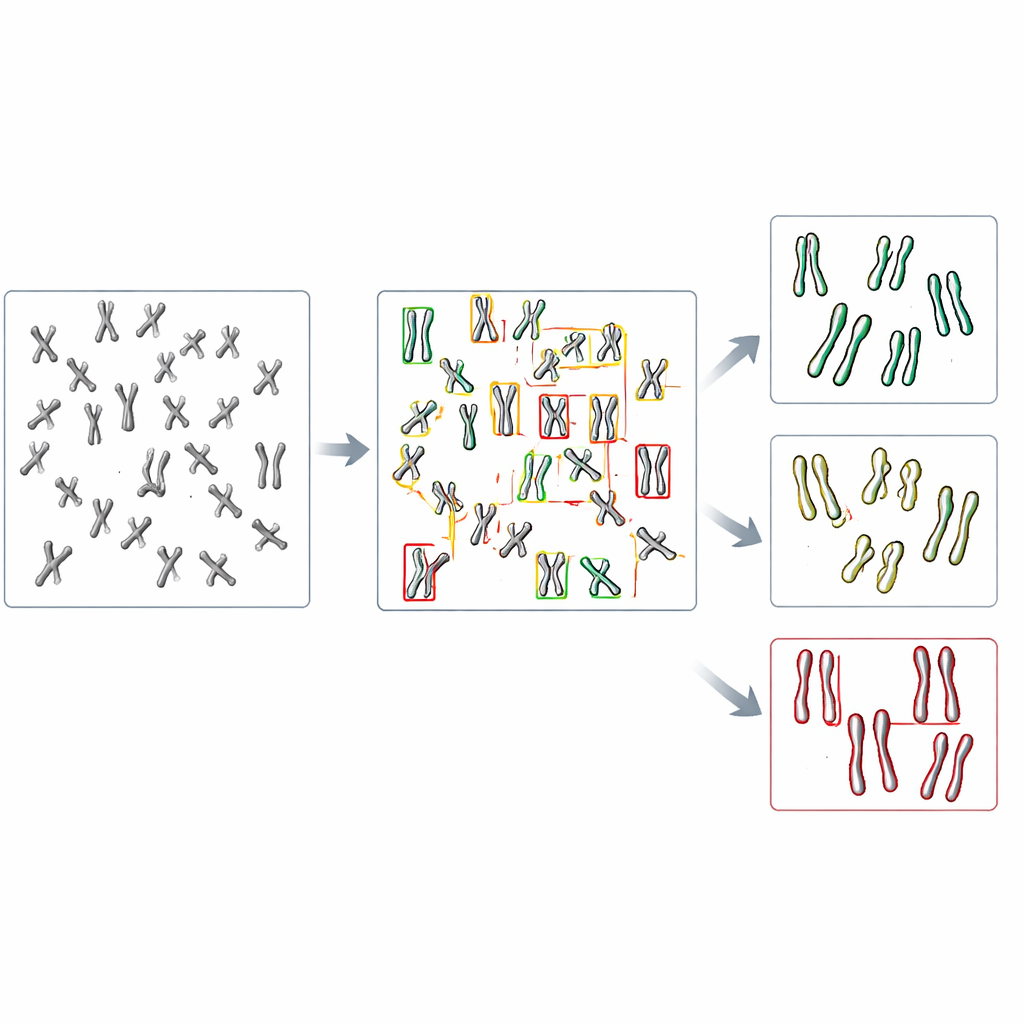
Co to oznacza dla przyszłej pracy laboratoryjnej
Badanie pokazuje, że model SI może przeskanować pełne rozproszenia chromosomów i automatycznie wskazać defekty spójności bez dodatkowych kroków przycinania czy ręcznego sprzątania. Mimo że wciąż jest miejsce na poprawę działania — szczególnie dla nakładających się chromosomów i przypadków granicznych — podejście już dorównuje wcześniejszym metodom wymagającym większej ingerencji człowieka. Ponieważ modele zbudowano, adaptując istniejące narzędzia open-source i można je do szkolić ponownie przy użyciu umiarkowanych zestawów obrazów, laboratoria bez głębokiej wiedzy obliczeniowej mogą opracować własne, dopasowane systemy. W dłuższej perspektywie podobne strategie mogą przyspieszyć przesiewy leków, pomóc porównywać liczne mutanty genetyczne i wyjść poza spójność, obejmując inne subtelne zmiany chromosomów ważne dla zdrowia człowieka.
Cytowanie: Matsumoto, S., Sojo, M., Oshima, K. et al. Detection and classification of chromosomes with sister chromatid cohesion defects using object detection models. Sci Rep 16, 13719 (2026). https://doi.org/10.1038/s41598-026-43009-6
Słowa kluczowe: obrazowanie chromosomów, uczenie maszynowe, detekcja obiektów, defekty spójności, YOLOv8