Clear Sky Science · es
Detección y clasificación de cromosomas con defectos de cohesión de cromátidas hermanas mediante modelos de detección de objetos
Por qué importan pequeñas torsiones en el ADN
Cada vez que una célula se divide, debe transmitir una copia exacta de su material genético. Para mantener esas copias juntas hasta el momento adecuado, las células dependen de un “pegamento” molecular que mantiene los cromosomas emparejados uno junto al otro. Cuando este pegamento falla, los cromosomas pueden separarse demasiado pronto, lo que conduce a genomes rotos, trastornos del desarrollo y cáncer. El estudio descrito aquí aborda un problema muy práctico: cómo detectar automáticamente estas sutiles fallas del pegamento en imágenes de microscopio, usando inteligencia artificial moderna en lugar de ojos humanos fatigados.
Cómo se mantienen unidos los cromosomas
Antes de que una célula se divida, cada cromosoma se copia de modo que hay dos hebras idénticas, conocidas como cromátidas hermanas. Una máquina proteica llamada cohesina ayuda a mantener a estas hermanas emparejadas hasta que la célula esté lista para separarlas. Si la cohesina o sus proteínas auxiliares funcionan mal, las hermanas pueden alejarse demasiado pronto. Uno de esos auxiliares es DDX11, una enzima que desenrolla el ADN cuyos defectos se asocian con una rara condición humana llamada síndrome de rotura de Varsovia. Al microscopio, las células con problemas de cohesión suelen mostrar cromosomas cuyas dos hebras están extrañamente abiertas o separadas en el centro, pero distinguir formas normales de anómalas requiere paciencia y criterio.
Por qué las comprobaciones manuales no son suficientes
Tradicionalmente, los investigadores extienden cromosomas en un portaobjetos, los tiñen y luego clasifican al menos entre 50 y 100 de ellos por muestra a mano. Cada cromosoma se juzga por su forma y por la distancia entre sus cromátidas hermanas. Este trabajo es lento, subjetivo y propenso al cansancio, lo que aumenta el riesgo de errores y de resultados inconsistentes entre científicos. Esfuerzos previos del mismo grupo usaron aprendizaje profundo para clasificar imágenes individuales de cromosomas, pero esos sistemas requerían pasos de software adicionales para recortar cromosomas individuales de imágenes de microscopio abarrotadas y descartar solapamientos confusos. Ese manejo extra de imágenes seguía dependiendo en gran medida de ajustes y limpieza manual, bloqueando una verdadera automatización de “un solo botón”.
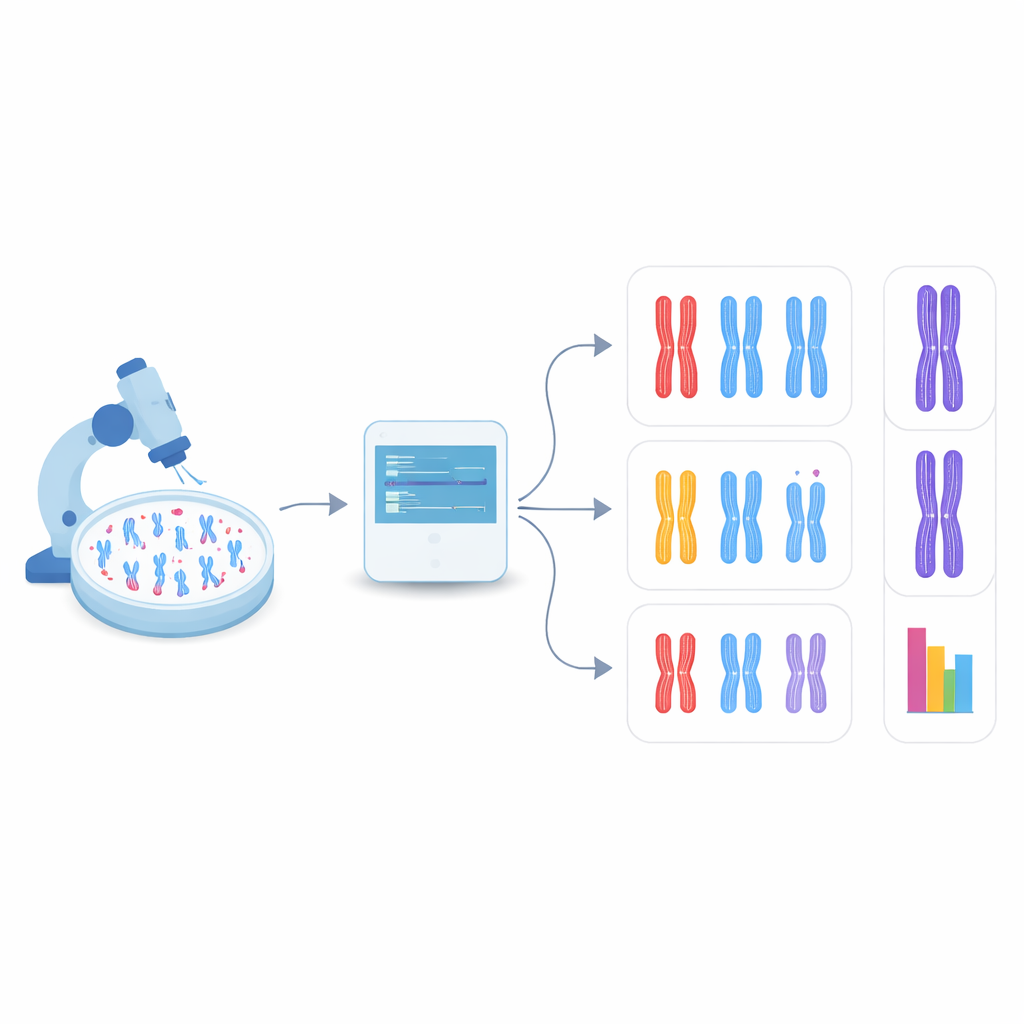
Permitir que el ordenador encuentre los cromosomas por sí mismo
En el nuevo estudio, el equipo recurrió a la detección de objetos, una rama de la visión por ordenador que puede tanto localizar como categorizar múltiples elementos dentro de una sola imagen. Se centraron en una familia de modelos rápidos y ampliamente usados llamados YOLO (por sus siglas en inglés, “You Only Look Once”) junto con varios métodos competidores. Primero, crearon un sistema de prueba mediante la ingeniería de células humanas que carecen de DDX11 y, por tanto, muestran fuertes problemas de cohesión, y prepararon imágenes de microscopio de sus cromosomas junto con los de células normales. Cada cromosoma visible en estas imágenes fue delimitado con un cuadro y etiquetado en una de tres formas: estrechamente emparejados, parcialmente separados a lo largo de los brazos, o claramente divididos en el centro. Estas etiquetas hechas a mano sirvieron como material de enseñanza para los algoritmos.
Enseñar a la IA a ver diferencias sutiles de forma
Los investigadores ajustaron finamente varios modelos de detección de objetos preentrenados con poco más de mil cromosomas etiquetados, reservando otras imágenes para verificar el rendimiento. Compararon qué tan bien cada modelo podía primero localizar cromosomas y luego asignarlos a la categoría correcta de las tres formas. Entre los sistemas probados, una versión llamada YOLOv8 fue la que mejor rendimiento ofreció. Coincidió con las etiquetas humanas en casi nueve de cada diez cromosomas, aun cuando las diferencias entre categorías eran a menudo bastante sutiles. Es importante que, al aplicarlo a imágenes de células normales y deficientes en DDX11, YOLOv8 reprodujo el patrón biológico clave que observan los expertos: las células defectuosas tenían muchas menos cromosomas estrechamente emparejados y muchas más con las cromátidas claramente separadas.
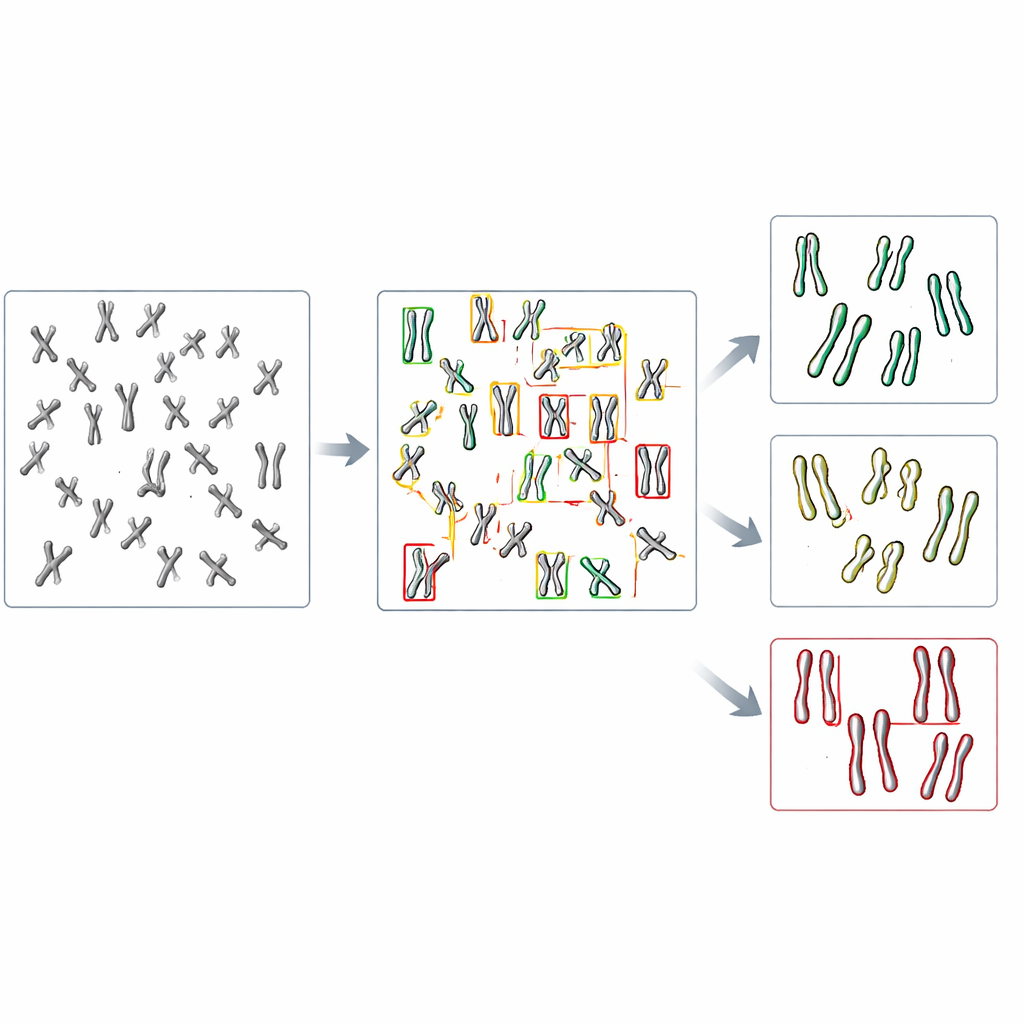
Qué significa esto para el trabajo de laboratorio futuro
El estudio muestra que un modelo de IA puede escanear extendidos cromosómicos completos y señalizar automáticamente defectos de cohesión sin pasos adicionales de recorte o limpieza manual. Si bien aún hay margen para mejorar el rendimiento—especialmente para cromosomas solapados y formas límite—el enfoque ya rivaliza con métodos anteriores que requerían más intervención humana. Dado que los modelos se construyeron adaptando herramientas de código abierto existentes y pueden volver a entrenarse con conjuntos de imágenes modestos, laboratorios sin experiencia profunda en informática podrían desarrollar sus propios sistemas a medida. A largo plazo, estrategias similares pueden acelerar el cribado de fármacos, ayudar a comparar muchos mutantes genéticos y extenderse más allá de la cohesión a otros cambios cromosómicos sutiles que importan para la salud humana.
Cita: Matsumoto, S., Sojo, M., Oshima, K. et al. Detection and classification of chromosomes with sister chromatid cohesion defects using object detection models. Sci Rep 16, 13719 (2026). https://doi.org/10.1038/s41598-026-43009-6
Palabras clave: imágenes de cromosomas, aprendizaje automático, detección de objetos, defectos de cohesión, YOLOv8