Clear Sky Science · sv
Detektion och klassificering av kromosomer med defekter i systerkromatidkohesionen med hjälp av objektigenkänningsmodeller
Varför små vridningar i DNA spelar roll
Varje gång en cell delar sig måste den föra vidare en exakt kopia av sitt genetiska material. För att hålla dessa kopior tillsammans tills rätt ögonblick förlitar sig celler på ett molekylärt ”lim” som håller parade kromosomer sida vid sida. När detta lim misslyckas kan kromosomer separera för tidigt, vilket leder till skadade genom, utvecklingsstörningar och cancer. Den studie som beskrivs här tar itu med ett väldigt praktiskt problem: hur man automatiskt upptäcker dessa subtila limfel i mikroskopbilder med modern artificiell intelligens istället för trötta mänskliga ögon.
Hur kromosomer hålls ihop
Innan en cell delar sig kopieras varje kromosom så att det finns två identiska strängar, kända som systerkromatider. Ett proteinkomplex kallat cohesin hjälper till att hålla dessa systrar ihop tills cellen är redo att dra isär dem. Om cohesin eller dess hjälpproteiner fungerar dåligt kan systrarna driva isär för tidigt. En sådan hjälpare är DDX11, ett DNA-avtrasslande enzym vars defekter är kopplade till ett sällsynt mänskligt tillstånd kallat Warsaw Breakage-syndrom. Under mikroskop visar celler med kohesionsproblem ofta kromosomer vars två strängar är märkbart öppna eller splittrade i mitten, men att skilja normala från onormala former kräver tålamod och omdöme.
Varför manuella kontroller inte räcker
Traditionellt sprider forskare kromosomer på ett preparat, färgar dem och klassificerar sedan minst 50 till 100 av dem per prov för hand. Varje kromosom bedöms utifrån form och hur långt isär dess systersträngar verkar vara. Det här arbetet är långsamt, subjektivt och lätt att tröttna på, vilket ökar risken för misstag och inkonsekventa resultat mellan forskare. Tidigare försök av samma forskargrupp använde djupinlärning för att klassificera individuella kromosombilder, men dessa system krävde separata programsteg för att klippa ut enskilda kromosomer från trånga mikroskopbilder och för att kasta bort förvirrande överlappningar. Den extra bildhanteringen berodde fortfarande i hög grad på manuell justering och efterarbete, vilket hindrade verklig "tryck-knapp"-automation.
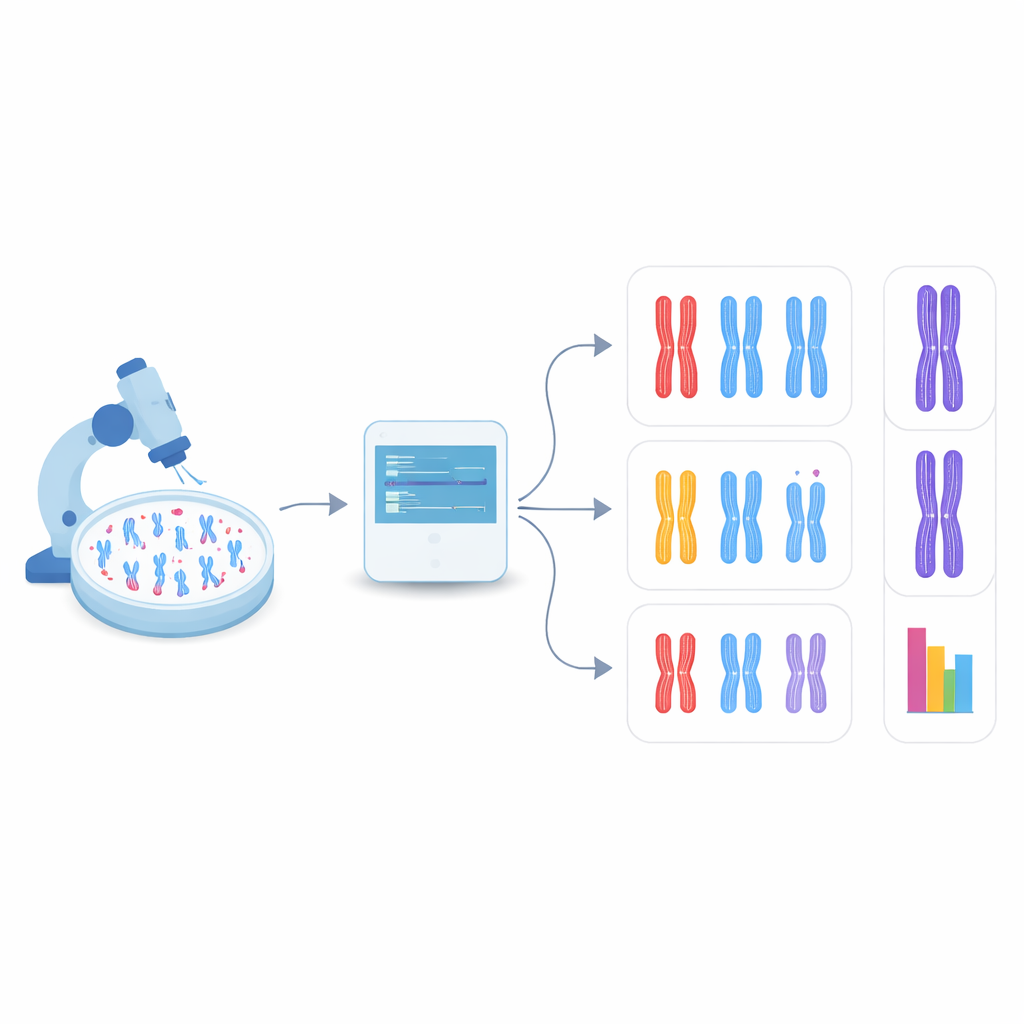
Låta datorn hitta kromosomer själv
I den nya studien vände sig teamet till objektigenkänning, en gren av datorseende som både kan hitta och kategorisera många objekt inom en enda bild. De fokuserade på en familj snabba, vida använda modeller kallade YOLO ("You Only Look Once") tillsammans med flera konkurrerande metoder. Först skapade de ett testsystem genom att konstruera humana celler som saknar DDX11 och därför visar starka kohesionsproblem, och sedan förberedde de mikroskopbilder av deras kromosomer tillsammans med sådana från normala celler. Varje synlig kromosom i dessa bilder ritades in med en ruta och märktes som en av tre formtyper: tätt parade, delvis separerade längs armarna eller tydligt splittrade i mitten. Dessa handgjorda etiketter tjänade som undervisningsmaterial för algoritmerna.
Att lära AI att se subtila formskillnader
Forskarnas finjusterade flera förtränade objektigenkänningsmodeller på lite över tusen märkta kromosomer, och reserverade andra bilder för att kontrollera prestanda. De jämförde hur väl varje modell först kunde hitta kromosomer överhuvudtaget och sedan tilldela dem rätt av de tre formkategorierna. Bland de testade systemen presterade en version kallad YOLOv8 bäst. Den matchade mänskliga etiketter korrekt för nästan nio av tio kromosomer, trots att skillnaderna mellan kategorier ofta var ganska subtila. Viktigt är att när modellen tillämpades på bilder från normala och DDX11-bristande celler återgav YOLOv8 det centrala biologiska mönstret som mänskliga experter ser: de defekta cellerna hade långt färre tätt parade kromosomer och betydligt fler med tydligt separerade systersträngar.
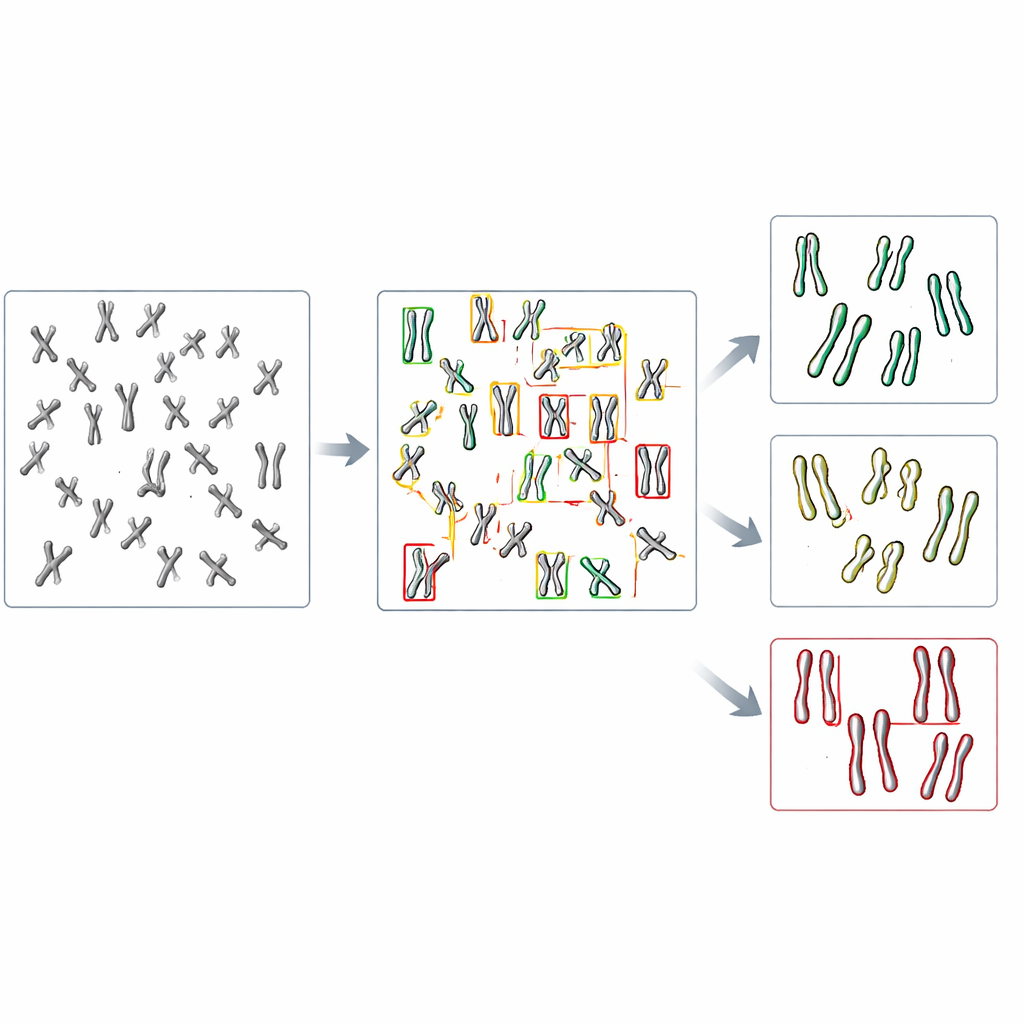
Vad detta betyder för framtida labbarbete
Studien visar att en AI-modell kan skanna fullständiga kromosomspreder och automatiskt flagga kohesionsdefekter utan extra beskärningssteg eller manuell efterbearbetning. Även om det fortfarande finns utrymme att förbättra prestandan—särskilt för överlappande kromosomer och gränsfall i former—konkurrerar tillvägagångssättet redan med tidigare metoder som krävde mer mänsklig insats. Eftersom modellerna byggdes genom att anpassa befintliga öppen-källkod-verktyg och kan tränas om med måttliga bildmängder, skulle laboratorier utan djup datorkunskap kunna utveckla egna skräddarsydda system. På sikt kan liknande strategier snabba upp screening för läkemedel, hjälpa till att jämföra många genetiska mutanter och sträcka sig bortom kohesion till andra subtila kromosomförändringar som är viktiga för människors hälsa.
Citering: Matsumoto, S., Sojo, M., Oshima, K. et al. Detection and classification of chromosomes with sister chromatid cohesion defects using object detection models. Sci Rep 16, 13719 (2026). https://doi.org/10.1038/s41598-026-43009-6
Nyckelord: kromosomavbildning, maskininlärning, objektigenkänning, kohesionsdefekter, YOLOv8