Clear Sky Science · it
Rilevamento e classificazione dei cromosomi con difetti di coesione tra cromatidi fratelli usando modelli di object detection
Perché piccole torsioni nel DNA contano
Ogni volta che una cellula si divide, deve trasmettere una copia esatta del suo materiale genetico. Per mantenere queste copie unite fino al momento opportuno, le cellule fanno affidamento su una «colla» molecolare che tiene affiancati i cromosomi appaiati. Quando questa colla fallisce, i cromosomi possono separarsi troppo presto, portando a genomi frammentati, disordini dello sviluppo e tumori. Lo studio descritto qui affronta un problema molto pratico: come individuare automaticamente questi sottili guasti della colla nelle immagini al microscopio, usando l’intelligenza artificiale moderna al posto degli occhi stanchi degli operatori umani.
Come i cromosomi restano insieme
Prima che una cellula si divida, ogni cromosoma viene copiato in modo da avere due filamenti identici, noti come cromatidi fratelli. Una macchina proteica chiamata cohesin aiuta a mantenere questi fratelli appaiati fino a quando la cellula non è pronta a separarli. Se cohesin o le proteine che lo assistono non funzionano correttamente, i cromatidi possono allontanarsi troppo presto l’uno dall’altro. Uno di questi aiutanti è DDX11, un enzima che svolge il DNA la cui disfunzione è collegata a una rara condizione umana chiamata sindrome da rottura di Varsavia. Al microscopio, le cellule con problemi di coesione spesso mostrano cromosomi i cui due filamenti appaiono stranamente aperti o divisi al centro, ma distinguere forme normali da quelle anomale richiede pazienza e giudizio.
Perché i controlli manuali non bastano
Tradizionalmente, i ricercatori stendono i cromosomi su un vetrino, li colorano e poi classificano a mano almeno 50-100 cromosomi per campione. Ogni cromosoma viene giudicato in base alla forma e a quanto distanti appaiono i suoi cromatidi fratelli. Questo lavoro è lento, soggettivo e stancante, il che aumenta il rischio di errori e risultati incoerenti tra gli scienziati. Sforzi precedenti dello stesso gruppo di ricerca hanno usato il deep learning per classificare immagini di singoli cromosomi, ma quei sistemi richiedevano passaggi software separati per ritagliare singoli cromosomi da immagini di microscopia affollate e per scartare sovrapposizioni confuse. Quel trattamento aggiuntivo delle immagini dipendeva ancora molto da interventi e pulizie manuali, bloccando una vera automazione «a pulsante».
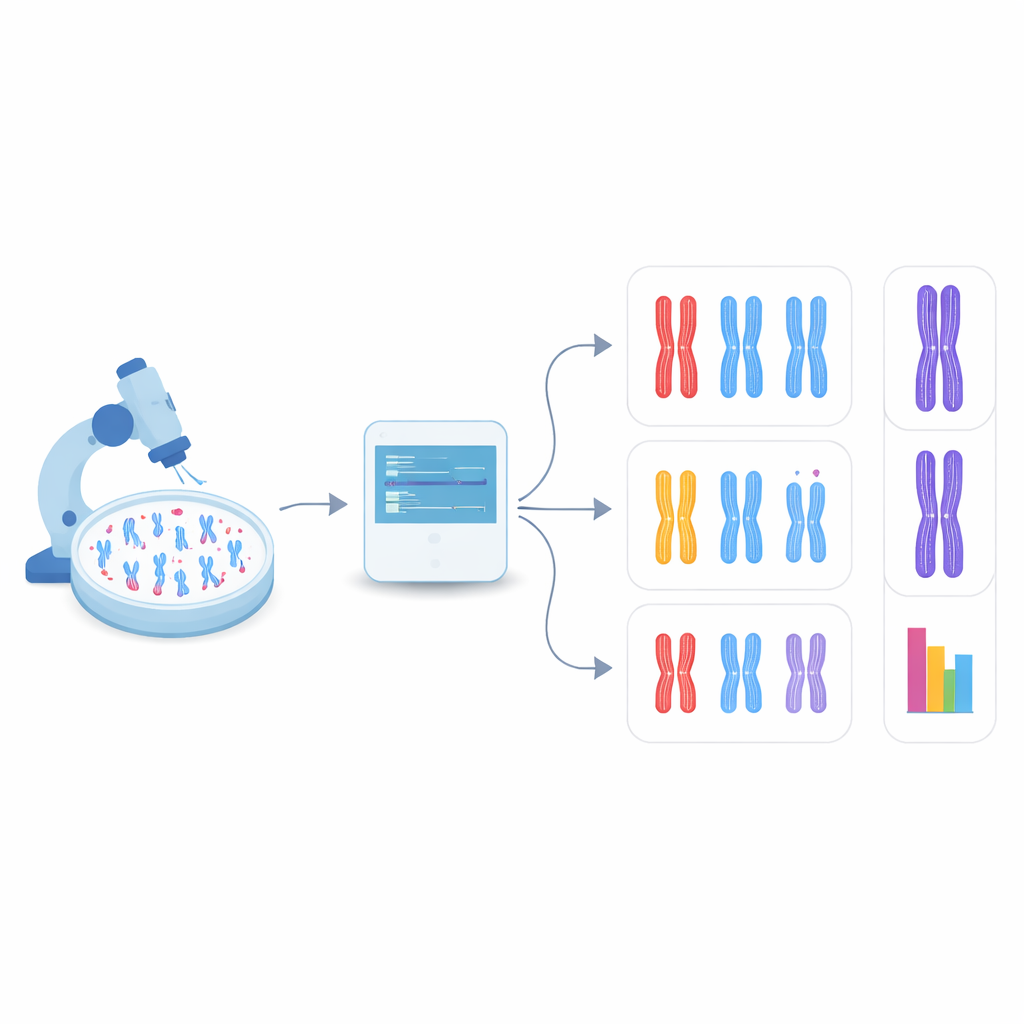
Lasciare che il computer trovi i cromosomi da solo
Nello studio più recente, il team si è rivolto all’object detection, un ramo della visione artificiale che può sia trovare sia classificare molti oggetti all’interno di una singola immagine. Si sono concentrati su una famiglia di modelli rapida e ampiamente usata chiamata YOLO (acronimo di “You Only Look Once”) insieme a diversi metodi concorrenti. Per prima cosa hanno creato un sistema di prova modificando geneticamente cellule umane privi di DDX11 e quindi con marcati problemi di coesione, poi hanno preparato immagini microscopiche dei loro cromosomi insieme a quelli di cellule normali. Ogni cromosoma visibile in queste immagini è stato delimitato con una scatola e etichettato in una delle tre tipologie di forma: strettamente appaiato, parzialmente separato lungo i bracci, o chiaramente diviso al centro. Queste etichette manuali sono servite come materiale di insegnamento per gli algoritmi.
Insegnare all’IA a vedere sottili differenze di forma
I ricercatori hanno perfezionato diversi modelli di object detection pre-addestrati su poco più di mille cromosomi etichettati, riservando altre immagini per verificare le prestazioni. Hanno confrontato quanto bene ogni modello riuscisse prima a individuare i cromosomi e poi ad assegnarli alla corretta delle tre categorie di forma. Tra i sistemi testati, una versione chiamata YOLOv8 ha ottenuto i migliori risultati. Ha corrisposto correttamente le etichette umane per quasi nove cromosomi su dieci, nonostante le differenze tra le categorie fossero spesso molto sottili. È importante che, applicato a immagini di cellule normali e di cellule prive di DDX11, YOLOv8 abbia riprodotto il modello biologico chiave osservato dagli esperti: le cellule difettose avevano molto meno cromosomi strettamente appaiati e molti più cromatidi chiaramente separati.
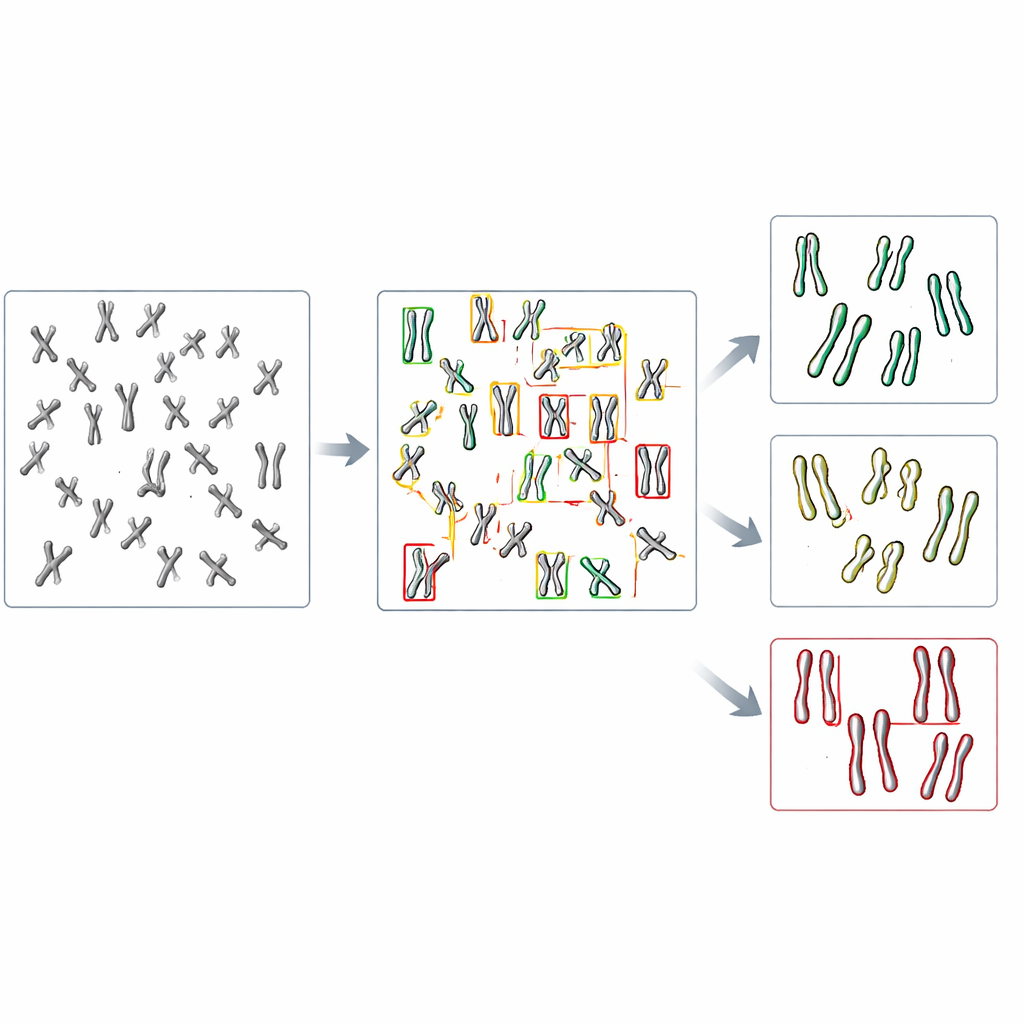
Cosa significa per il lavoro di laboratorio futuro
Lo studio dimostra che un modello di IA può analizzare distese di cromosomi complete e segnalare automaticamente i difetti di coesione senza passaggi aggiuntivi di ritaglio o pulizie manuali. Sebbene ci sia ancora margine di miglioramento — specialmente per i cromosomi sovrapposti e le forme borderline — l’approccio è già alla pari con metodi precedenti che richiedevano maggiore intervento umano. Poiché i modelli sono stati costruiti adattando strumenti open-source esistenti e possono essere riaddestrati con set di immagini modesti, laboratori privi di profonda esperienza informatica potrebbero sviluppare sistemi personalizzati. A lungo termine, strategie simili potrebbero accelerare lo screening di farmaci, aiutare a confrontare molti mutanti genetici ed estendersi oltre la coesione ad altri sottili cambiamenti cromosomici rilevanti per la salute umana.
Citazione: Matsumoto, S., Sojo, M., Oshima, K. et al. Detection and classification of chromosomes with sister chromatid cohesion defects using object detection models. Sci Rep 16, 13719 (2026). https://doi.org/10.1038/s41598-026-43009-6
Parole chiave: imaging dei cromosomi, apprendimento automatico, rilevamento oggetti, difetti di coesione, YOLOv8