Clear Sky Science · zh
牙龈卟啉单胞菌通过 IL-6/EZH2/Snai2 轴促进口腔鳞状细胞癌进展
为何一种牙龈细菌与口腔癌有关
大多数人把出血的牙龈视为牙科上的麻烦,而非癌症风险。该研究展示了一种常见牙周致病菌Porphyromonas gingivalis如何助推口腔鳞状细胞癌(OSCC)生长与扩散,这是一种常见且致命的口腔癌。通过追踪从感染到细胞失控的一连串事件,研究者们找到了一个分子弱点,可能成为减缓或阻止癌症进展的靶点。
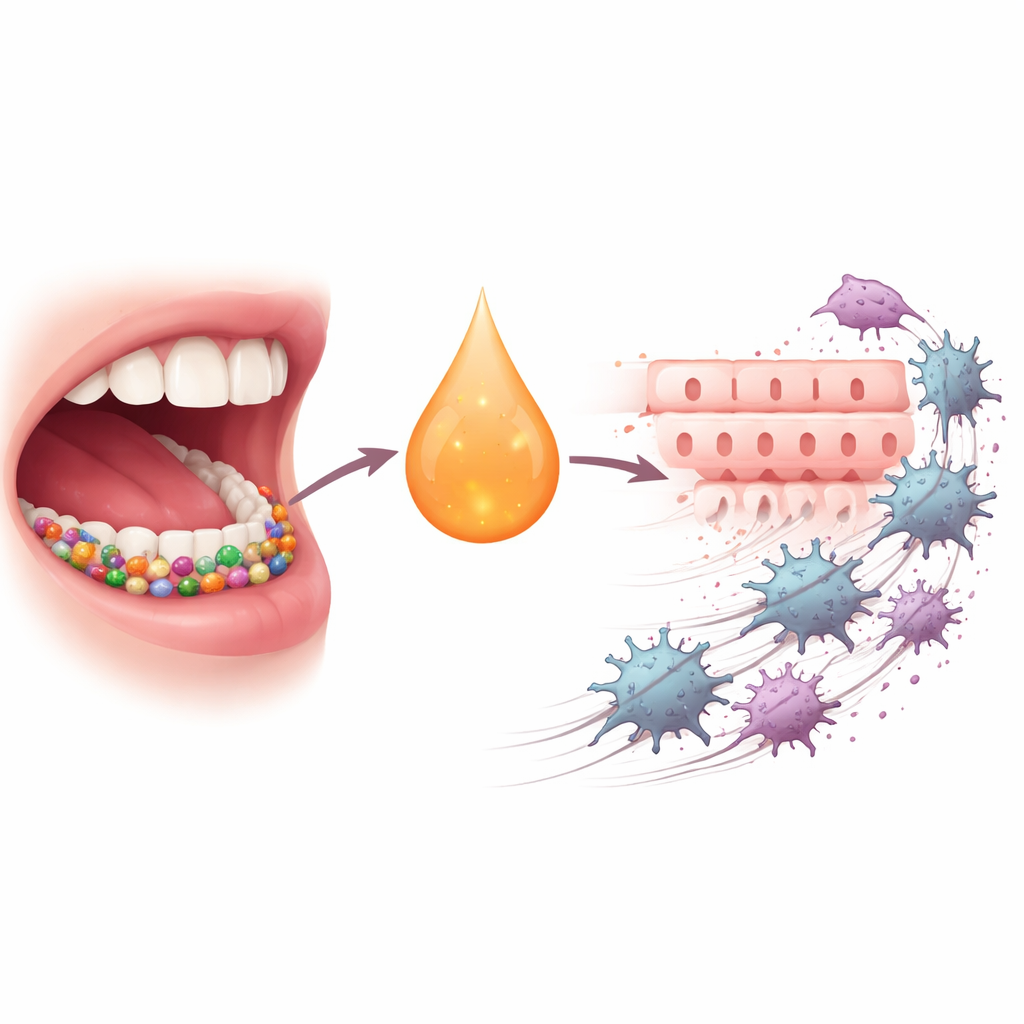
一种顽固的癌症与隐藏的帮手
口腔鳞状细胞癌(OSCC)是全球十种最常见癌症之一,且极难治愈;尽管有手术、放疗、化疗和新兴的免疫疗法,诊断后五年存活率仍不足一半。近年来,科学家意识到口腔微生物群不仅仅导致蛀牙或牙周病。当其平衡被打破时,某些细菌会加剧慢性炎症、改变局部免疫并推动细胞走向更具侵袭性和移动性的状态。作为牙周炎的主要病原体,P. gingivalis多次与OSCC以及一种称为上皮-间质转化(EMT)的细胞转变有关——在该过程中有序的表面细胞松动、移动并侵入邻近组织。
从牙龈感染到强烈的化学信号
作者首先探问P. gingivalis感染是否会提高患者口腔中炎性信使IL-6的水平。通过测量牙齿缝隙周围的液体,他们发现携带P. gingivalis的牙周病患者和OSCC患者的IL-6水平均明显高于健康志愿者。随后他们分离出OSCC患者的原代肿瘤细胞并将其暴露于IL-6,许多细胞上调了IL-6受体,使其对该信号更敏感。受体表达高的细胞分裂更快、迁移能力更强,这些都是更具危险性的癌细胞群体的典型特征。
肿瘤细胞内的三步接力
进一步研究中,团队关注了癌细胞内的两种蛋白:EZH2,一种调控DNA包装和基因表达的酶;以及Snai2,一种已知能促使细胞变得更具移动性和侵袭性的转录因子。他们发现OSCC细胞中EZH2和Snai2的含量已高于正常口腔细胞,且IL-6刺激进一步在RNA和蛋白水平上提升了这两者。当他们在标准OSCC细胞系中人为提高EZH2时,细胞生长更快、迁移更多。敲低EZH2则产生相反效果,但补回EZH2蛋白可恢复侵袭性行为。关键是,EZH2水平的变化会直接按相同方向调节Snai2基因活性,表明EZH2在这条接力中位于Snai2上游。
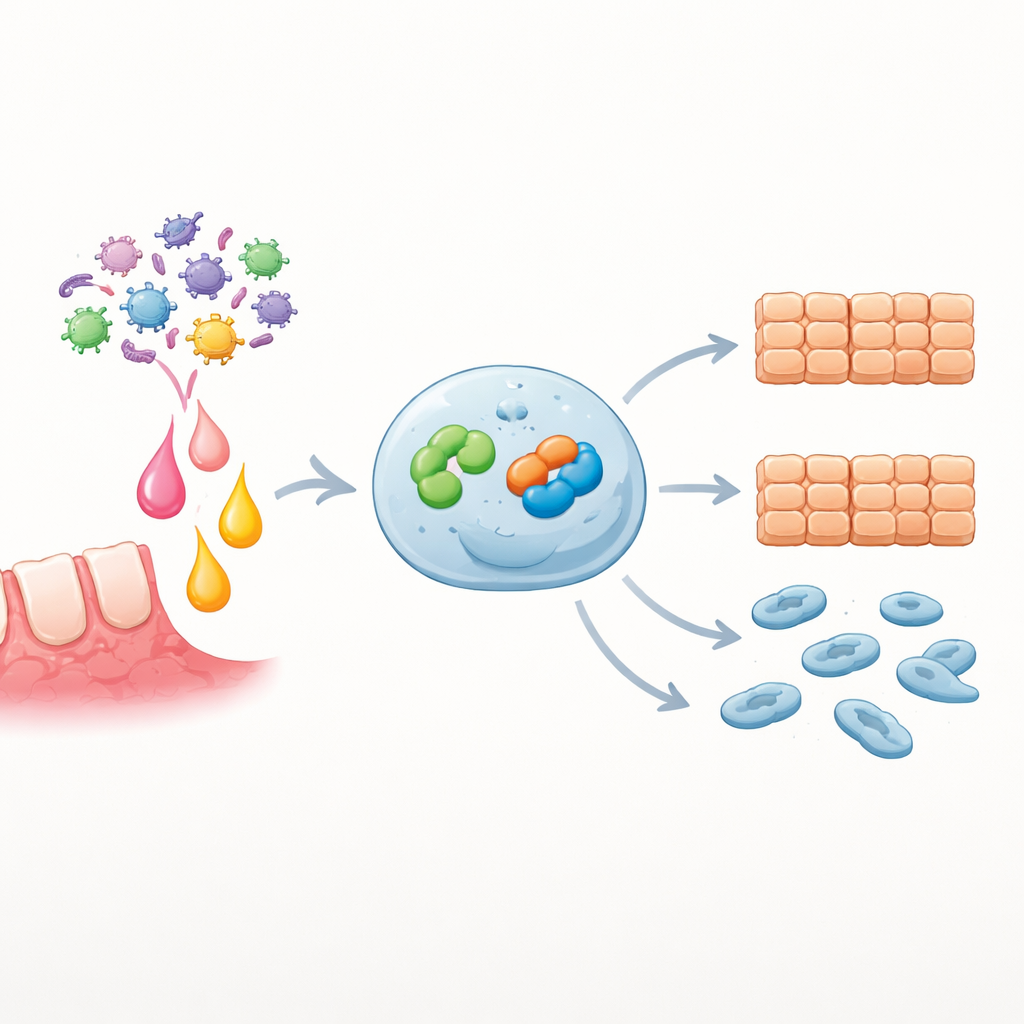
阻断接力可减缓癌症特征
为检验Snai2是否为EZH2效应所必需,研究者在提高EZH2的同时沉默了Snai2。在这种条件下,与单独过表达EZH2相比,细胞增殖、愈伤闭合和迁移均显著降低,表明Snai2是EZH2驱动的侵袭性特征的关键引擎。在对IL-6有响应的原代肿瘤细胞中,添加EZH2化学抑制剂或用于敲低Snai2的小RNA分子都显著减弱了IL-6诱导的增殖和迁移。对大型患者数据集的生物信息学分析进一步支持了这些实验室发现:高SNAI2表达富集于与感染和细胞运动相关的通路,而肿瘤中SNAI2较高的患者往往预后较差。
对患者与预防的意义
综上所述,这项工作讲述了一个清晰的链条:牙周致病菌提升口腔中IL-6水平;IL-6在邻近肿瘤细胞内启动EZH2;EZH2进而上调Snai2,帮助癌细胞脱离并扩散。这条IL-6/EZH2/Snai2链将日常口腔感染与危及生命的癌症行为联系起来,并指出了新的干预点。未来,更好地控制慢性牙龈感染、降低IL-6信号的药物或有针对性的EZH2或Snai2抑制剂,或许能减缓OSCC的进展。尽管这些发现仍需在动物模型和临床研究中进一步验证,但它们为口腔卫生与癌症风险之间搭建了一个具体的分子桥梁,并提供了一组有希望的、更基于生物学的治疗靶点。
引用: Liu, S., Guan, T., Xu, B. et al. Porphyromonas gingivalis promotes oral squamous cell carcinoma progression via the IL-6/EZH2/Snai2 axis. Sci Rep 16, 10296 (2026). https://doi.org/10.1038/s41598-026-41528-w
关键词: 口腔癌, 牙周病, 牙龈卟啉单胞菌, 炎症, 癌症信号通路