Clear Sky Science · fr
Porphyromonas gingivalis favorise la progression du carcinome épidermoïde oral via l’axe IL-6/EZH2/Snai2
Pourquoi une bactérie gingivale compte pour le cancer de la bouche
La plupart des gens considèrent les gencives qui saignent comme une nuisance dentaire, non comme un risque cancéreux. Cette étude montre comment une bactérie courante responsable de la maladie des gencives, Porphyromonas gingivalis, peut contribuer à la croissance et à la dissémination du carcinome épidermoïde oral, une forme fréquente et mortelle de cancer buccal. En retraçant une chaîne d’événements depuis l’infection jusqu’au comportement cellulaire incontrôlé, les chercheurs identifient un point faible moléculaire qui pourrait être ciblé pour ralentir ou prévenir la progression du cancer.
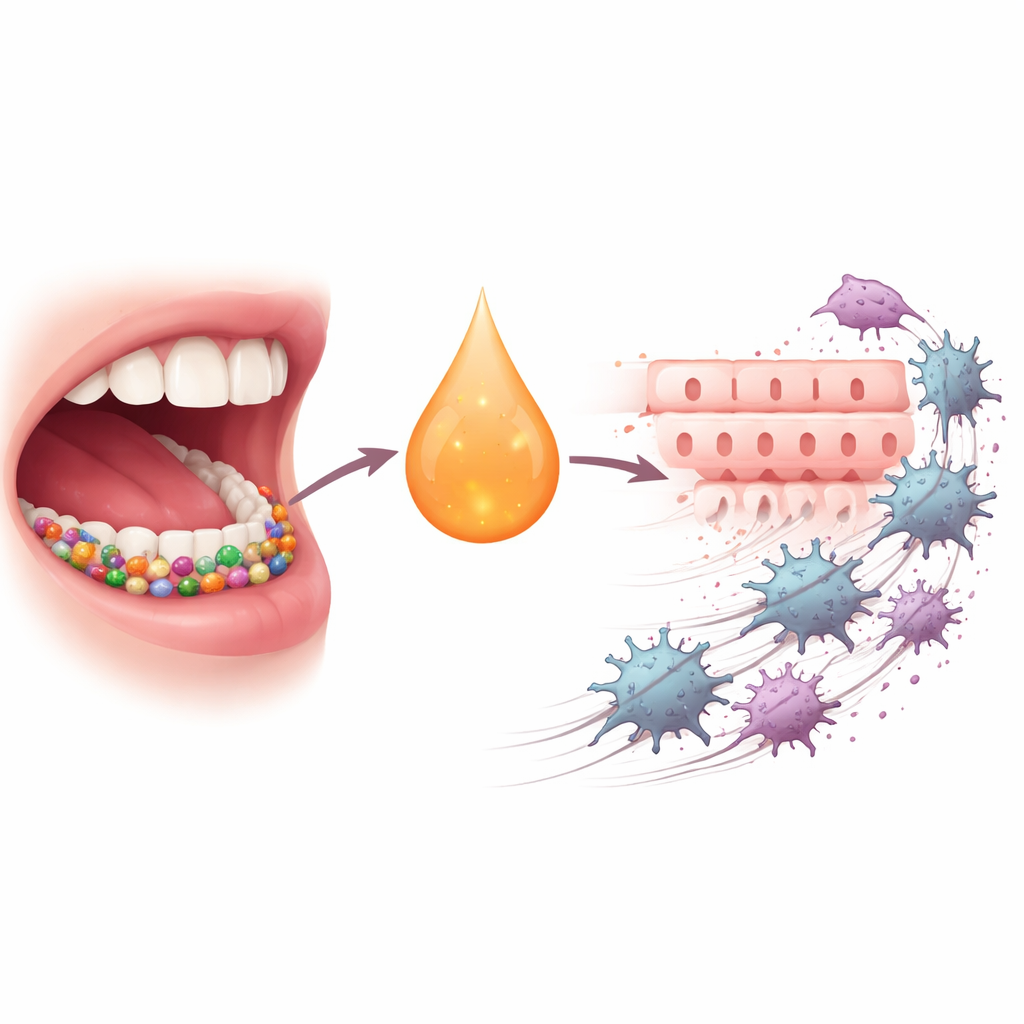
Un cancer tenace aidé par des complices cachés
Le carcinome épidermoïde oral (OSCC) figure parmi les dix cancers les plus fréquents dans le monde et est notoirement difficile à guérir ; malgré la chirurgie, la radiothérapie, la chimiothérapie et les immunothérapies récentes, moins de la moitié des patients sont en vie cinq ans après le diagnostic. Ces dernières années, les scientifiques ont réalisé que les communautés microbiennes de notre bouche font plus que causer des caries ou des maladies parodontales. Lorsqu’elles sont déséquilibrées, certaines bactéries peuvent attiser l’inflammation chronique, modifier l’immunité locale et pousser les cellules vers des états plus agressifs et mobiles. P. gingivalis, un acteur majeur de la parodontite, a été maintes fois associé à l’OSCC et à un basculement cellulaire appelé transition épithélio–mésenchymateuse, où les cellules de surface ordonnées se détachent, migrent et envahissent les tissus voisins.
De l’infection gingivale à de puissants signaux chimiques
Les auteurs ont commencé par se demander si l’infection par P. gingivalis augmente les niveaux du messager inflammatoire IL-6 dans la bouche des patients. En mesurant le liquide du sillon gingival, ils ont constaté que l’IL-6 était beaucoup plus élevée chez les patients atteints de maladie des gencives porteurs de P. gingivalis et chez les personnes atteintes d’OSCC que chez les volontaires sains. Ils ont ensuite isolé des cellules tumorales primaires de patients atteints d’OSCC et les ont exposées à l’IL-6. Nombre de ces cellules ont augmenté leurs niveaux du récepteur de l’IL-6, les rendant plus réceptives au signal. Les cellules à récepteur élevé proliféraient plus vite et migraient plus facilement, des signes clairs d’une population cellulaire cancéreuse plus dangereuse.
Un relais en trois étapes au sein des cellules tumorales
Allant plus loin, l’équipe s’est concentrée sur deux protéines à l’intérieur des cellules cancéreuses : EZH2, une enzyme qui contrôle la façon dont l’ADN est emballé et quels gènes sont activés, et Snai2, un facteur de transcription connu pour pousser les cellules vers un état plus mobile et invasif. Ils ont constaté que les cellules OSCC présentaient déjà plus d’EZH2 et de Snai2 que les cellules orales normales, et que la stimulation par l’IL-6 augmentait encore ces deux protéines au niveau de l’ARN et des protéines. Lorsqu’ils ont augmenté artificiellement EZH2 dans une lignée cellulaire OSCC standard, les cellules se multipliaient plus vite et migraient davantage. La réduction d’EZH2 produisait l’effet inverse, mais la remise d’EZH2 protéique rétablissait le comportement agressif. De manière cruciale, les variations des niveaux d’EZH2 modifiaient directement l’activité du gène Snai2 dans le même sens, montrant qu’EZH2 agit en amont de Snai2 dans ce relais.
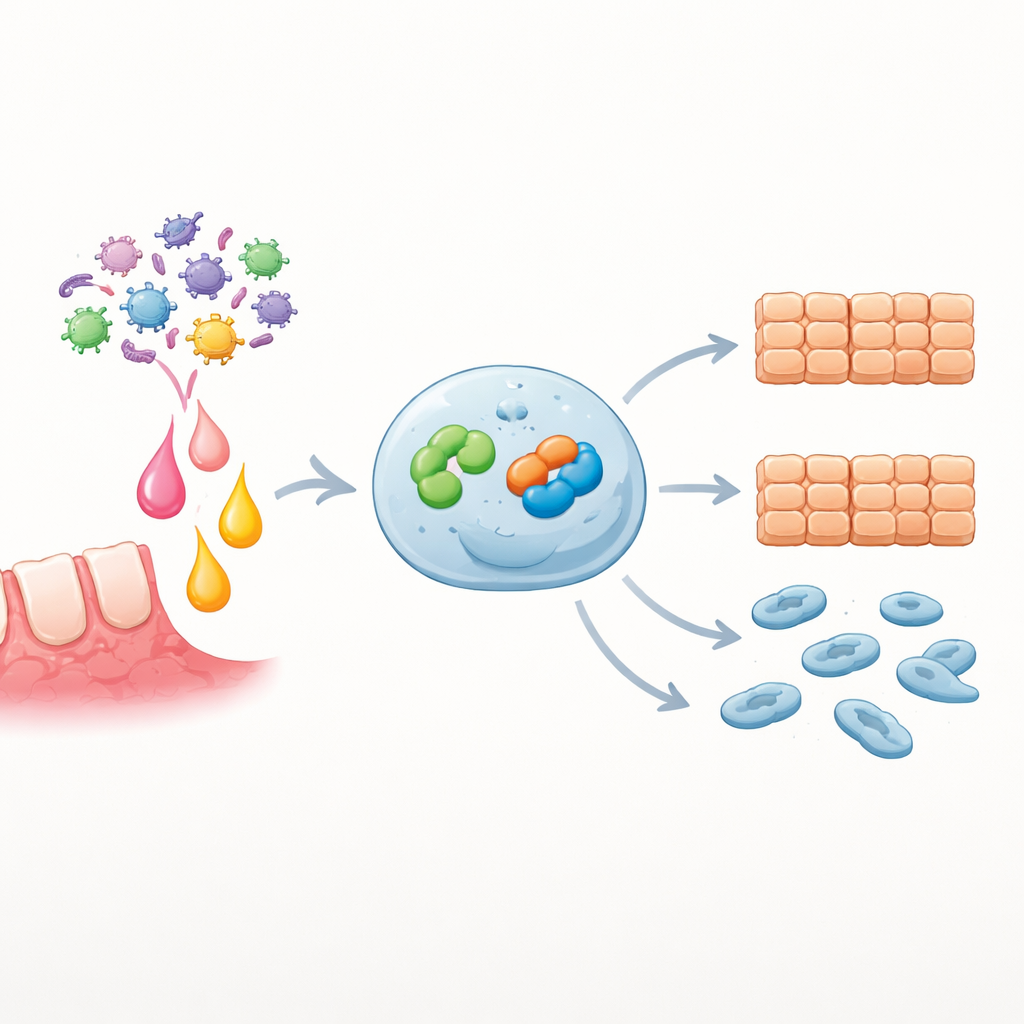
Bloquer le relais atténue les traits cancéreux
Pour tester si Snai2 est nécessaire aux effets d’EZH2, les chercheurs ont surexprimé EZH2 tout en réduisant simultanément Snai2. Dans ces conditions, la croissance cellulaire, la fermeture de plaie et la migration étaient toutes significativement réduites par rapport à la surexpression d’EZH2 seule, indiquant que Snai2 est un moteur clé des traits agressifs induits par EZH2. Dans des cellules tumorales primaires réactives à l’IL-6, l’ajout soit d’un inhibiteur chimique d’EZH2 soit d’ARNs petits ciblant Snai2 a fortement atténué la prolifération et la migration induites par l’IL-6. Des analyses bioinformatiques de grandes séries de patients ont renforcé ces résultats de laboratoire : une expression élevée de SNAI2 était enrichie dans des voies liées à l’infection et au mouvement cellulaire, et les patients dont les tumeurs exprimaient davantage de SNAI2 avaient tendance à une survie plus mauvaise.
Ce que cela signifie pour les patients et la prévention
Au total, ce travail trace un récit clair et simple : une bactérie responsable de maladie des gencives augmente les niveaux d’IL-6 dans la bouche ; l’IL-6 active EZH2 à l’intérieur des cellules tumorales voisines ; EZH2, à son tour, augmente Snai2, qui aide les cellules cancéreuses à se détacher et à se propager. Cette chaîne IL-6/EZH2/Snai2 relie les infections buccales courantes à un comportement cancéreux potentiellement mortel et met en évidence de nouveaux points d’intervention. À l’avenir, un meilleur contrôle des infections gingivales chroniques, des médicaments qui réduisent les signaux de l’IL-6, ou des inhibiteurs ciblés d’EZH2 ou de Snai2 pourraient aider à ralentir la progression de l’OSCC. Bien que ces résultats doivent encore être confirmés dans des modèles animaux et des études cliniques, ils offrent un pont moléculaire concret entre l’hygiène buccale et le risque de cancer — et un ensemble prometteur de cibles pour des traitements plus efficaces et fondés sur la biologie.
Citation: Liu, S., Guan, T., Xu, B. et al. Porphyromonas gingivalis promotes oral squamous cell carcinoma progression via the IL-6/EZH2/Snai2 axis. Sci Rep 16, 10296 (2026). https://doi.org/10.1038/s41598-026-41528-w
Mots-clés: cancer buccal, maladie des gencives, Porphyromonas gingivalis, inflammation, signalisation cancéreuse