Clear Sky Science · ar
البكتيريا Porphyromonas gingivalis تعزز تقدم سرطان الخلايا الحرشفية الفموي عبر محور IL-6/EZH2/Snai2
لماذا تهمّ بكتيريا اللثة في سرطان الفم
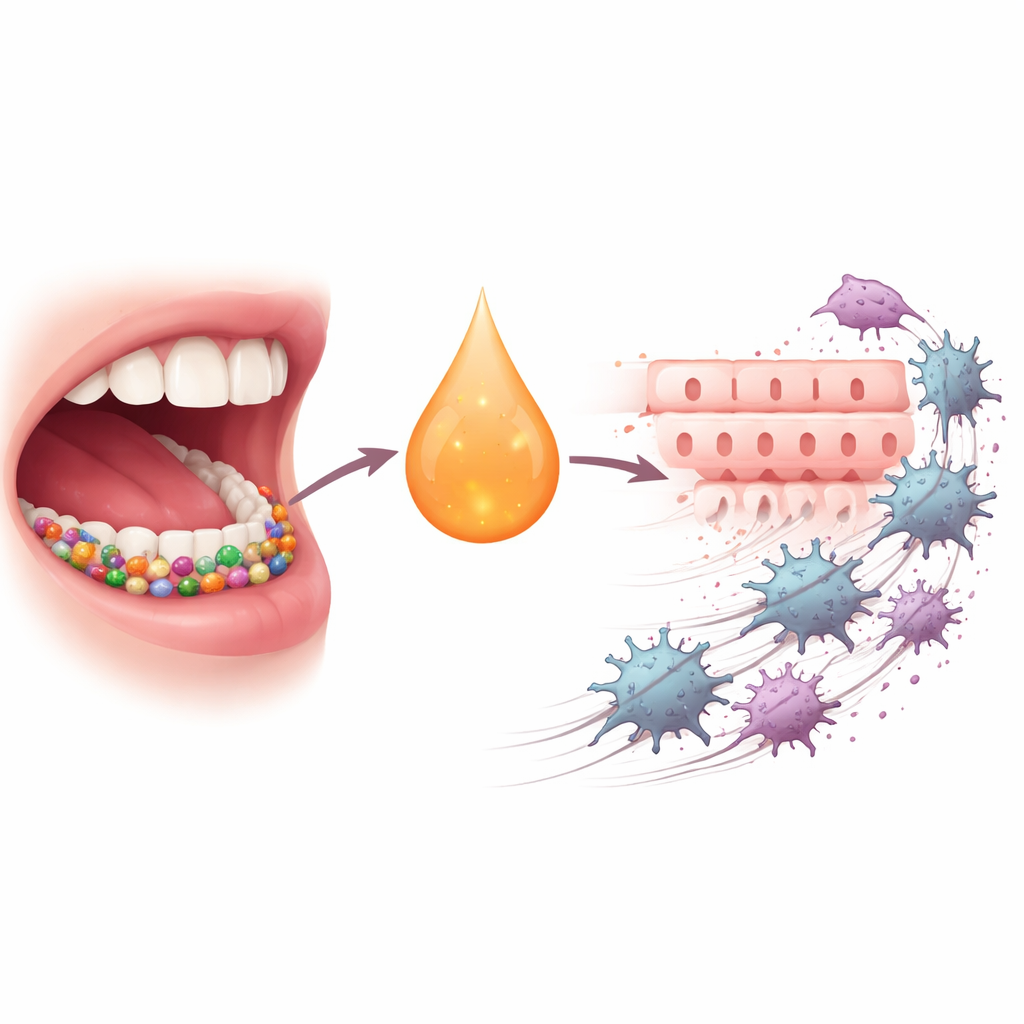
يفكر معظم الناس في نزيف اللثة بوصفه إزعاجًا طبّيًا أسنانيًا وليس عامل خطر للسرطان. تُظهر هذه الدراسة كيف يمكن لبكتيريا شائعة ممرِضة للثة، Porphyromonas gingivalis، أن تساعد في دفع نمو وانتشار سرطان الخلايا الحرشفية الفموي، وهو شكل شائع وخطير من سرطانات الفم. من خلال تتبُّع سلسلة أحداث من العدوى إلى سلوك الخلايا الخارج عن السيطرة، يحدد الباحثون نقطة ضعف جزيئية قد تُستغل لإبطاء أو منع تقدم السرطان.
سرطان عنيد ولديه مساهمون خفيون
يصنّف سرطان الخلايا الحرشفية الفموي (OSCC) ضمن أكثر عشرة سرطانات شيوعًا عالميًا ويشتهر بصعوبة علاجه؛ فعلى الرغم من الجراحة والعلاج الإشعاعي والكيميائي وكذلك المناعاتية الحديثة، يبقى أقل من نصف المرضى على قيد الحياة بعد خمس سنوات من التشخيص. في السنوات الأخيرة، أدرك العلماء أن مجتمعات الميكروبات في أفواهنا تفعل أكثر من التسبب بتسوس الأسنان أو أمراض اللثة. عندما يختل توازنها، يمكن لبعض البكتيريا أن تؤجج الالتهاب المزمن، وتعدّل المناعة المحلية، وتدفع الخلايا نحو حالات أكثر عدوانية وقابلية للحركة. وقد رُبطت P. gingivalis، المذنبة الأساسية في التهاب دواعم السن، مرارًا بسرطان الخلايا الحرشفية الفموي وبتحول خلوي يسمى الانتقال الظهاري-اللحائي، حيث تفقد الخلايا السطحية انتظامها وتصبح أكثر ارتخاءً وحركة وغزوًا للأنسجة المجاورة.
من عدوى اللثة إلى إشارات كيميائية قوية
بدأ المؤلفون بسؤال إن كانت عدوى P. gingivalis ترفع مستويات الرسول الالتهابي IL-6 في أفواه المرضى. بقياس سائل الشق حول الأسنان، وجدوا أن مستويات IL-6 كانت أعلى بكثير لدى مرضى أمراض اللثة الحاملين لـ P. gingivalis وكذلك لدى أشخاص مصابين بـ OSCC مقارنةً بالمتطوّعين الأصحاء. ثم عزلوا خلايا ورمية أولية من مرضى OSCC وعرضوها لـ IL-6. زادت العديد من هذه الخلايا من مستويات مستقبل IL-6، مما جعلها أكثر استجابة للإشارة. الخلايا ذات المستقبلات العالية انقسمت أسرع وتحركت بسهولة أكبر، وهي سمات واضحة لسكان خلايا سرطانية أكثر خطورة.
تتابع من ثلاث خطوات داخل خلايا الورم
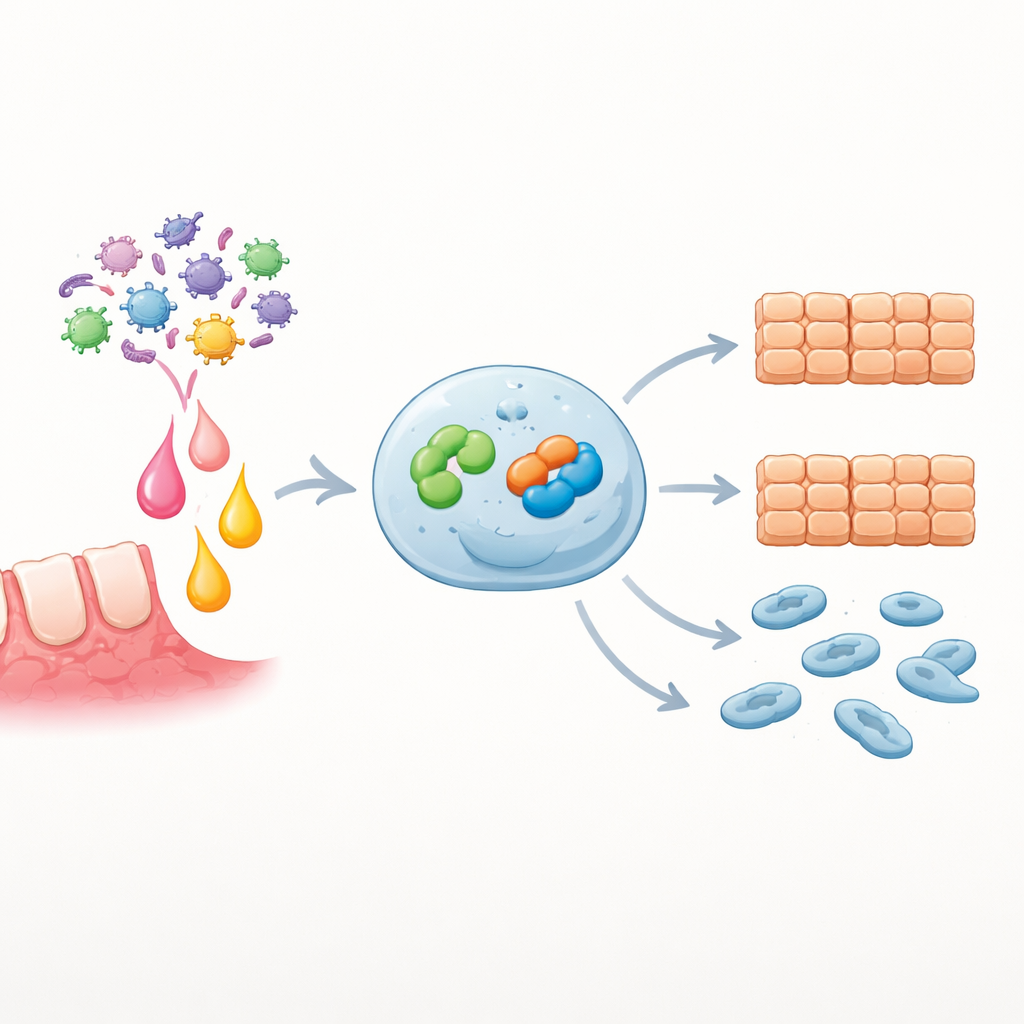
باتّباع مستوى أعمق، ركز الفريق على بروتينين داخل الخلايا السرطانية: EZH2، إنزيم يتحكم في كيفية تغليف الحمض النووي وتفعيل الجينات، وSnai2، عامل نسخي معروف بدفع الخلايا نحو حالة أكثر حركة وغزوًا. وجدوا أن خلايا OSCC تحتوي بالفعل على مستويات أعلى من EZH2 وSnai2 مقارنة بالخلايا الفموية الطبيعية، وأن تحفيز IL-6 يعزز كلا البروتينين على مستوى الرنا والبروتين. عندما زادوا EZH2 صناعيًا في سلالة خلوية معيارية من OSCC، نمت الخلايا بشكل أسرع وتحركت أكثر. وكان تثبيط EZH2 له التأثير المعاكس، لكن إعادة إضافة بروتين EZH2 أعادت السلوك العدواني. والأهم من ذلك، أن التغيرات في مستويات EZH2 غيرت مباشرة نشاط جين Snai2 في نفس الاتجاه، ما يظهر أن EZH2 يقع أعلى Snai2 في هذا التتابع.
حجب التتابع يبطئ خواص السرطان
لاختبار ما إذا كان Snai2 مطلوبًا لتأثيرات EZH2، عزز الباحثون EZH2 لكنهم في الوقت نفسه خامدوا Snai2. في هذه الظروف، انخفضت بسرعة معدلات نمو الخلايا وإغلاق الجروح والهجرة مقارنةً بزيادة EZH2 وحدها، مما يدل على أن Snai2 هو محرك رئيسي للصفات العدوانية التي يسببها EZH2. في الخلايا الورمية الأولية التي استجابت لـ IL-6، أدى إضافة مثبط كيميائي لـ EZH2 أو جزيئات RNA صغيرة تخفض Snai2 إلى تقليل حاد في التكاثر والهجرة المُحثة بواسطة IL-6. عززت التحليلات الحاسوبية لبيانات مرضى كبيرة هذه النتائج المخبرية: إذ كان تعبير SNAI2 المرتفع مُثرًا في المسارات المرتبطة بالعدوى وحركة الخلايا، ويميل المرضى الذين تحتوي أورامهم على مزيد من SNAI2 إلى البقاء على قيد الحياة بشكل أسوأ.
ماذا يعني هذا للمرضى والوقاية
تجتمع النتائج لتوضّح قصة واضحة ببساطة: بكتيريا ممرِضة للثة ترفع مستويات IL-6 في الفم؛ IL-6 يُشغّل EZH2 داخل الخلايا الورمية القريبة؛ وEZH2 بدوره يرفع Snai2، الذي يساعد الخلايا السرطانية على الانفصال والانتشار. يربط هذا المحور IL-6/EZH2/Snai2 بين العدوى الفموية اليومية وسلوكيات سرطانية مهددة للحياة ويبرز نقاط تدخل جديدة. في المستقبل، قد يساعد التحكم الأفضل في العدوى المزمنة للثة، أو أدوية تخفف إشارات IL-6، أو مثبطات مُستهدفة لـ EZH2 أو Snai2 في إبطاء تقدم OSCC. وبينما تحتاج هذه النتائج إلى تأكيد في نماذج حيوانية ودراسات سريرية، فإنها تقدّم جسرًا جزيئيًا ملموسًا بين نظافة الفم وخطر السرطان—ومجموعة واعدة من الأهداف لعلاجات أكثر فعالية ومعتمدة على البيولوجيا.
الاستشهاد: Liu, S., Guan, T., Xu, B. et al. Porphyromonas gingivalis promotes oral squamous cell carcinoma progression via the IL-6/EZH2/Snai2 axis. Sci Rep 16, 10296 (2026). https://doi.org/10.1038/s41598-026-41528-w
الكلمات المفتاحية: سرطان الفم, أمراض اللثة, Porphyromonas gingivalis, الالتهاب, إشارات السرطان