Clear Sky Science · pt
Porphyromonas gingivalis promove a progressão do carcinoma espinocelular oral via o eixo IL-6/EZH2/Snai2
Por que um micro-organismo gengival importa para o câncer bucal
A maioria das pessoas vê sangramento gengival como um incômodo odontológico, não como um risco de câncer. Este estudo demonstra como uma bactéria comum da doença periodontal, Porphyromonas gingivalis, pode facilitar o crescimento e a disseminação do carcinoma espinocelular oral, uma forma frequente e mortal de câncer de boca. Ao traçar uma cadeia de eventos da infecção ao comportamento celular descontrolado, os pesquisadores identificam um ponto fraco molecular que poderia ser alvo para retardar ou prevenir a progressão do câncer.
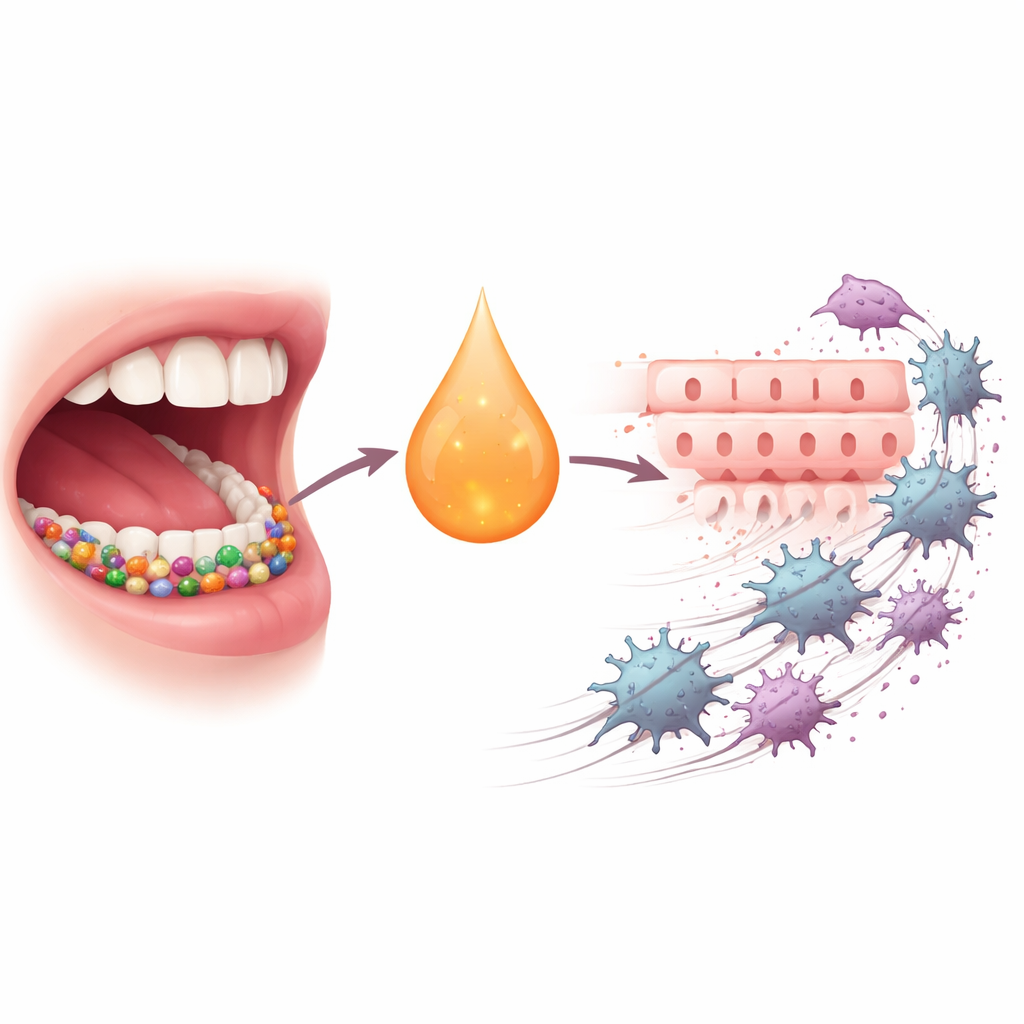
Um câncer persistente com ajudantes ocultos
O carcinoma espinocelular oral (CEOC) está entre os dez cânceres mais comuns no mundo e é notoriamente difícil de curar; apesar de cirurgia, radioterapia, quimioterapia e imunoterapias mais recentes, menos da metade dos pacientes está viva cinco anos após o diagnóstico. Nos últimos anos, cientistas perceberam que as comunidades microbianas na nossa boca fazem mais do que causar cáries ou doenças gengivais. Quando seu equilíbrio é perturbado, certas bactérias podem alimentar a inflamação crônica, alterar a imunidade local e empurrar as células para estados mais agressivos e móveis. P. gingivalis, um culpado chave na periodontite, tem sido repetidamente associado ao CEOC e a uma mudança celular chamada transição epitélio-mesenquimal, na qual células superficiais ordenadas se afrouxam, migram e invadem tecidos próximos.
Da infecção gengival a sinais químicos potentes
Os autores começaram perguntando se a infecção por P. gingivalis eleva os níveis do mensageiro inflamatório IL-6 na boca dos pacientes. Medindo o fluido do sulco gengival, encontraram níveis muito maiores de IL-6 tanto em pacientes com doença gengival que carregavam P. gingivalis quanto em pessoas com CEOC, em comparação com voluntários saudáveis. Em seguida, isolaram células tumorais primárias de pacientes com CEOC e as expuseram a IL-6. Muitas dessas células aumentaram seus níveis do receptor de IL-6, tornando-se mais responsivas ao sinal. As células com alto nível de receptor proliferaram mais e migraram com mais facilidade, marcas claras de uma população de células cancerígenas mais perigosa.
Um revezamento em três etapas dentro das células tumorais
Aprofundando, a equipe focou em duas proteínas dentro das células cancerígenas: EZH2, uma enzima que controla como o DNA é empacotado e quais genes são ativados, e Snai2, um fator de transcrição conhecido por impulsionar células a um estado mais móvel e invasivo. Eles descobriram que células de CEOC já apresentavam mais EZH2 e Snai2 do que células orais normais, e que a estimulação por IL-6 aumentava ainda mais ambas as proteínas nos níveis de RNA e proteína. Quando aumentaram artificialmente o EZH2 em uma linhagem padrão de CEOC, as células cresceram mais rápido e se moveram mais. Reduzir o EZH2 teve o efeito oposto, mas a reintrodução da proteína EZH2 restaurou o comportamento agressivo. Crucialmente, mudanças nos níveis de EZH2 alteraram diretamente a atividade do gene Snai2 na mesma direção, mostrando que EZH2 está a montante de Snai2 nesse revezamento.
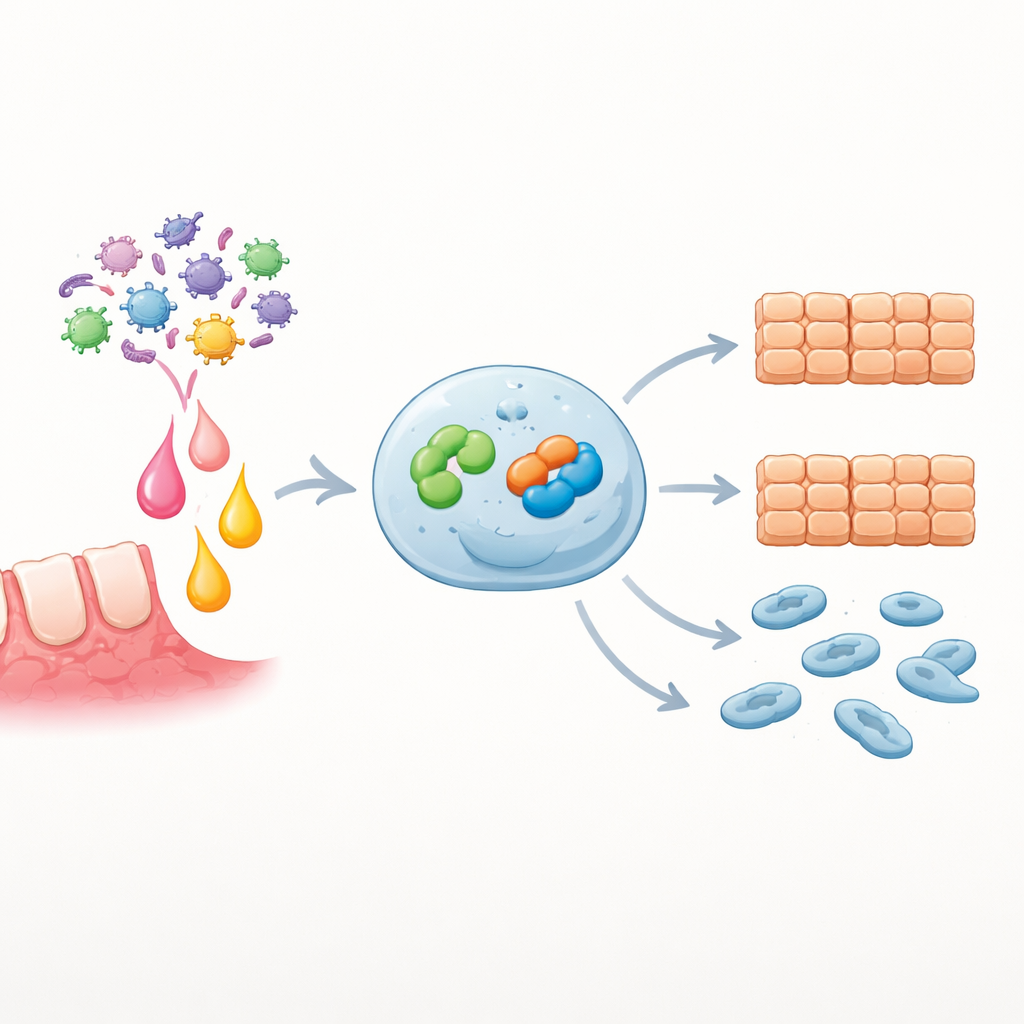
Bloquear o revezamento reduz traços cancerígenos
Para testar se Snai2 é necessário para os efeitos de EZH2, os pesquisadores aumentaram o EZH2 enquanto silenciavam simultaneamente o Snai2. Nestas condições, crescimento celular, fechamento de feridas e migração foram todos significativamente reduzidos em comparação com a superexpressão de EZH2 isolada, indicando que Snai2 é um motor chave dos traços agressivos induzidos por EZH2. Em células tumorais primárias que respondiam a IL-6, a adição de um inibidor químico de EZH2 ou de pequenas moléculas de RNA que reduzem Snai2 atenuou fortemente a proliferação e migração induzidas por IL-6. Análises bioinformáticas de grandes conjuntos de dados de pacientes reforçaram esses achados de laboratório: alta expressão de SNAI2 estava enriquecida em vias relacionadas à infecção e ao movimento celular, e pacientes cujos tumores apresentavam mais SNAI2 tendiam a ter pior sobrevida.
O que isso significa para pacientes e prevenção
Em conjunto, o trabalho descreve uma história clara em termos simples: uma bactéria da doença gengival aumenta os níveis de IL-6 na boca; IL-6 ativa EZH2 dentro de células tumorais vizinhas; EZH2, por sua vez, eleva Snai2, que ajuda células cancerígenas a se desprenderem e se espalharem. Essa cadeia IL-6/EZH2/Snai2 conecta infecções orais cotidianas a comportamentos cancerígenos potencialmente fatais e destaca novos pontos de intervenção. No futuro, melhor controle da infecção gengival crônica, drogas que reduzam os sinais de IL-6 ou inibidores seletivos de EZH2 ou Snai2 podem ajudar a retardar a progressão do CEOC. Embora essas descobertas ainda precisem ser confirmadas em modelos animais e estudos clínicos, elas oferecem uma ponte molecular concreta entre higiene oral e risco de câncer — e um conjunto promissor de alvos para tratamentos mais eficazes e baseados na biologia.
Citação: Liu, S., Guan, T., Xu, B. et al. Porphyromonas gingivalis promotes oral squamous cell carcinoma progression via the IL-6/EZH2/Snai2 axis. Sci Rep 16, 10296 (2026). https://doi.org/10.1038/s41598-026-41528-w
Palavras-chave: câncer oral, doença gengival, Porphyromonas gingivalis, inflamação, sinalização do câncer