Clear Sky Science · ru
Porphyromonas gingivalis способствует прогрессированию плоскоклеточного рака полости рта через ось IL-6/EZH2/Snai2
Почему микроб десен важен для рака рта
Большинство людей воспринимают кровоточивость десен как зубную неприятность, а не как риск рака. В этом исследовании показано, как обычная бактерия, вызывающая заболевания десен, Porphyromonas gingivalis, может способствовать росту и распространению плоскоклеточного рака полости рта — частой и смертельной формы рака рта. Проследив цепочку событий от инфекции до неконтролируемого поведения клеток, исследователи выявили молекулярную уязвимость, на которую можно было бы нацелиться, чтобы замедлить или предотвратить прогрессирование рака.
Упрямый рак с тайными помощниками
Плоскоклеточный рак полости рта (OSCC) входит в десятку самых распространённых видов рака в мире и известен своей высокой трудноизлечимостью; несмотря на операцию, лучевую и химиотерапию, а также новые иммунотерапии, менее половины пациентов остаются в живых через пять лет после диагноза. В последние годы учёные поняли, что микробные сообщества в нашей полости рта делают не только кариес или вызывают заболевания десен. При нарушении их равновесия некоторые бактерии разжигают хроническое воспаление, изменяют местный иммунитет и подталкивают клетки к более агрессивным, подвижным состояниям. P. gingivalis, один из ключевых возбудителей пародонтита, неоднократно связывали с OSCC и с клеточным переключением, называемым эпителиально-мезенхимальным переходом, при котором упорядоченные поверхностные клетки теряют сцепление, становятся подвижными и проникают в соседние ткани.
От инфекции десен до мощных химических сигналов
Авторы исследования начали с вопроса, повышает ли инфекция P. gingivalis уровни провоспалительного мессенджера IL-6 в ротовой полости пациентов. Измеряя жидкость из десневых карманов, они обнаружили, что IL-6 был значительно выше как у пациентов с заболеваниями десен, несущих P. gingivalis, так и у людей с OSCC по сравнению со здоровыми добровольцами. Затем они выделили первичные опухолевые клетки от пациентов с OSCC и подвергли их воздействию IL-6. Многие из этих клеток увеличили уровни рецептора IL-6, что делало их более отзывчивыми на сигнал. Клетки с высоким уровнем рецептора делились быстрее и мигрировали охотнее — явные признаки более опасной популяции раковых клеток.
Трёхступенчатая передача внутри опухолевых клеток
Углубляясь, команда сосредоточилась на двух белках внутри раковых клеток: EZH2 — ферменте, контролирующем упаковку ДНК и включение генов, и Snai2 — транскрипционном факторе, известном тем, что способствует переходу клеток в более подвижное, инвазивное состояние. Они обнаружили, что клетки OSCC уже содержат больше EZH2 и Snai2, чем нормальные клетки полости рта, а стимуляция IL-6 дополнительно усиливала оба белка на уровне РНК и белка. Когда они искусственно повышали EZH2 в стандартной линии клеток OSCC, клетки росли быстрее и демонстрировали повышенную подвижность. Понижение уровня EZH2 давало противоположный эффект, но добавление белка EZH2 восстанавливало агрессивное поведение. Критически важно, что изменения уровня EZH2 прямо сдвигали активность гена Snai2 в ту же сторону, что показывает, что EZH2 находится выше Snai2 в этой передающей цепочке.
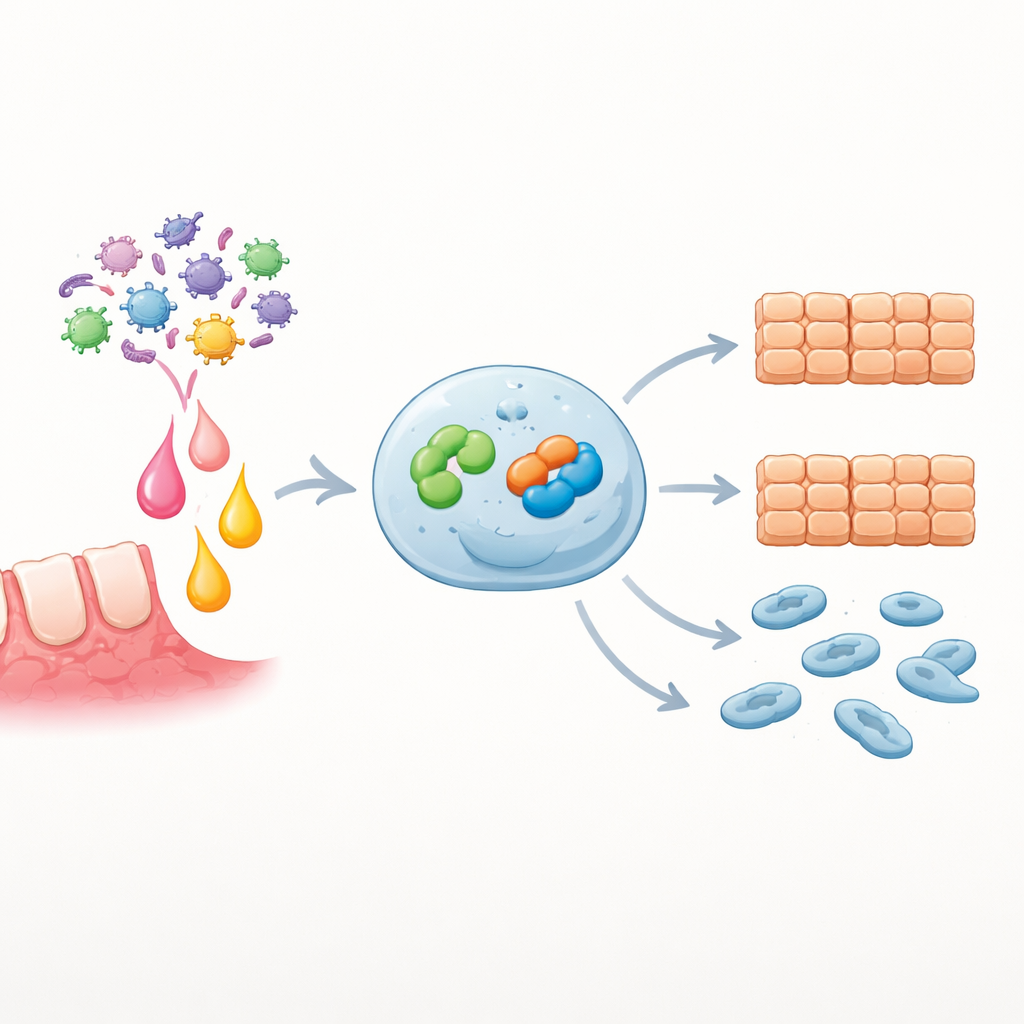
Блокировка цепочки замедляет признаки рака
Чтобы проверить, необходим ли Snai2 для эффектов EZH2, исследователи повысили EZH2, но одновременно заглушили Snai2. При таких условиях рост клеток, закрытие ран и миграция были значимо снижены по сравнению с одним только сверхэкспрессированным EZH2, что указывает на ключевую роль Snai2 в обеспечении агрессивных признаков, вызванных EZH2. В первичных опухолевых клетках, реагировавших на IL-6, добавление либо химического ингибитора EZH2, либо малых РНК, подавляющих Snai2, резко ослабляло IL-6-индуцированную пролиферацию и миграцию. Биоинформатический анализ больших наборов клинических данных укрепил эти лабораторные находки: высокая экспрессия SNAI2 была обогащена в путях, связанных с инфекцией и клеточной подвижностью, а у пациентов с опухолями, содержащими больше SNAI2, как правило, было худшее выживание.
Что это означает для пациентов и профилактики
В совокупности работа рисует ясную картину простыми словами: бактерия, вызывающая болезни десен, повышает уровни IL-6 в ротовой полости; IL-6 включает EZH2 внутри соседних опухолевых клеток; EZH2 в свою очередь усиливает Snai2, что помогает раковым клеткам отделяться и распространяться. Эта ось IL-6/EZH2/Snai2 связывает повседневные инфекции полости рта с угрожающим жизни поведением рака и выделяет новые точки для вмешательства. В будущем лучшее контролирование хронической инфекции десен, препараты, снижающие сигналы IL-6, или целевые ингибиторы EZH2 или Snai2 могут помочь замедлить прогрессирование OSCC. Хотя эти выводы ещё нужно подтвердить на животных моделях и в клинических исследованиях, они предлагают конкретный молекулярный мост между гигиеной полости рта и риском рака — и перспективный набор мишеней для более эффективных, основанных на биологии лечений.
Цитирование: Liu, S., Guan, T., Xu, B. et al. Porphyromonas gingivalis promotes oral squamous cell carcinoma progression via the IL-6/EZH2/Snai2 axis. Sci Rep 16, 10296 (2026). https://doi.org/10.1038/s41598-026-41528-w
Ключевые слова: рак полости рта, заболевание десен, Porphyromonas gingivalis, воспаление, сигналы рака