Clear Sky Science · it
Porphyromonas gingivalis favorisce la progressione del carcinoma squamoso orale tramite l’asse IL-6/EZH2/Snai2
Perché un germe gengivale conta nel cancro orale
La maggior parte delle persone considera le gengive sanguinanti un fastidio dentistico, non un fattore di rischio per il cancro. Questo studio mostra come un comune batterio responsabile di malattia gengivale, Porphyromonas gingivalis, possa favorire la crescita e la diffusione del carcinoma squamoso orale, una forma frequente e spesso letale di cancro della bocca. Tracciando una catena di eventi dall’infezione al comportamento incontrollato delle cellule, i ricercatori individuano un punto molecolare vulnerabile che potrebbe essere bersagliato per rallentare o prevenire la progressione tumorale.
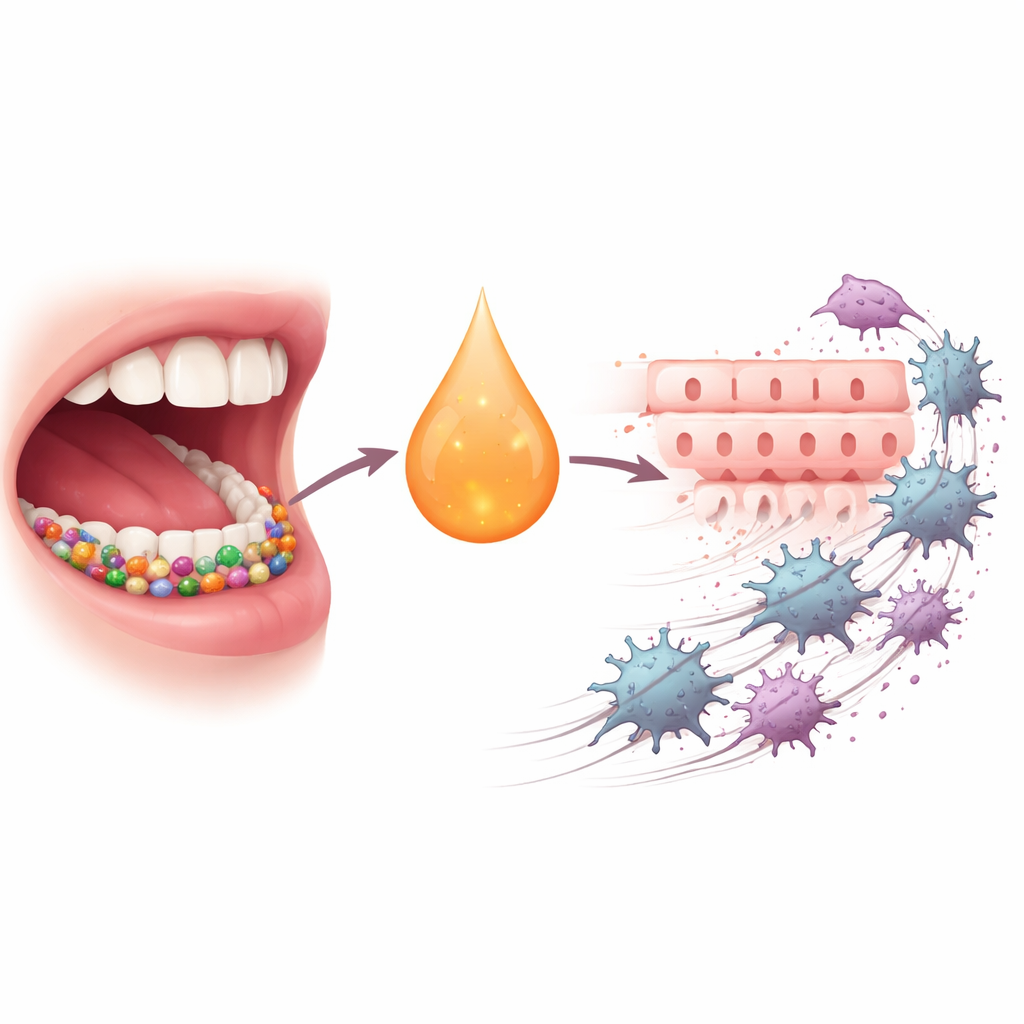
Un cancro ostinato con aiutanti nascosti
Il carcinoma squamoso orale (OSCC) è tra i dieci tumori più comuni al mondo ed è notoriamente difficile da curare; nonostante interventi chirurgici, radioterapia, chemioterapia e nuove immunoterapie, meno della metà dei pazienti è ancora in vita cinque anni dopo la diagnosi. Negli ultimi anni gli scienziati hanno compreso che le comunità microbiche nella nostra bocca fanno più che causare carie o gengiviti. Quando il loro equilibrio viene alterato, alcuni batteri possono alimentare l’infiammazione cronica, modificare l’immunità locale e spingere le cellule verso stati più aggressivi e mobili. P. gingivalis, un attore chiave nella parodontite, è stato ripetutamente associato all’OSCC e a uno spostamento cellulare chiamato transizione epitelio-mesenchimale, in cui le cellule superficiali ordinate si distaccano, si muovono e invadono i tessuti vicini.
Dall’infezione gengivale a segnali chimici potenti
Gli autori hanno iniziato chiedendosi se l’infezione da P. gingivalis aumenti i livelli del mediatore infiammatorio IL-6 nella bocca dei pazienti. Misurando il fluido dalla tasca gengivale, hanno riscontrato che l’IL-6 era molto più elevato sia nei pazienti con malattia gengivale portatori di P. gingivalis sia nelle persone con OSCC rispetto ai volontari sani. Hanno quindi isolato cellule tumorali primarie da pazienti con OSCC e le hanno esposte all’IL-6. Molte di queste cellule hanno aumentato i livelli del recettore per l’IL-6, rendendosi più sensibili al segnale. Le cellule con alto livello di recettore si dividevano più rapidamente e migravano più facilmente, chiari segni di una popolazione cellulare tumorale più pericolosa.
Una staffetta in tre passaggi dentro le cellule tumorali
Approfondendo, il team si è concentrato su due proteine all’interno delle cellule tumorali: EZH2, un enzima che controlla il modo in cui il DNA è impacchettato e quali geni vengono attivati, e Snai2, un fattore di trascrizione noto per spingere le cellule verso uno stato più mobile e invasivo. Hanno scoperto che le cellule OSCC avevano già più EZH2 e Snai2 rispetto alle cellule orali normali, e che la stimolazione con IL-6 aumentava ulteriormente entrambe le proteine sia a livello di RNA sia proteico. Quando hanno aumentato artificialmente EZH2 in una linea cellulare standard di OSCC, le cellule crescevano più velocemente e migravano di più. L’abbassamento di EZH2 aveva l’effetto opposto, ma il reintegro della proteina EZH2 ripristinava il comportamento aggressivo. In modo cruciale, le variazioni nei livelli di EZH2 spostavano direttamente l’attività del gene Snai2 nella stessa direzione, dimostrando che EZH2 agisce a monte di Snai2 in questa staffetta.
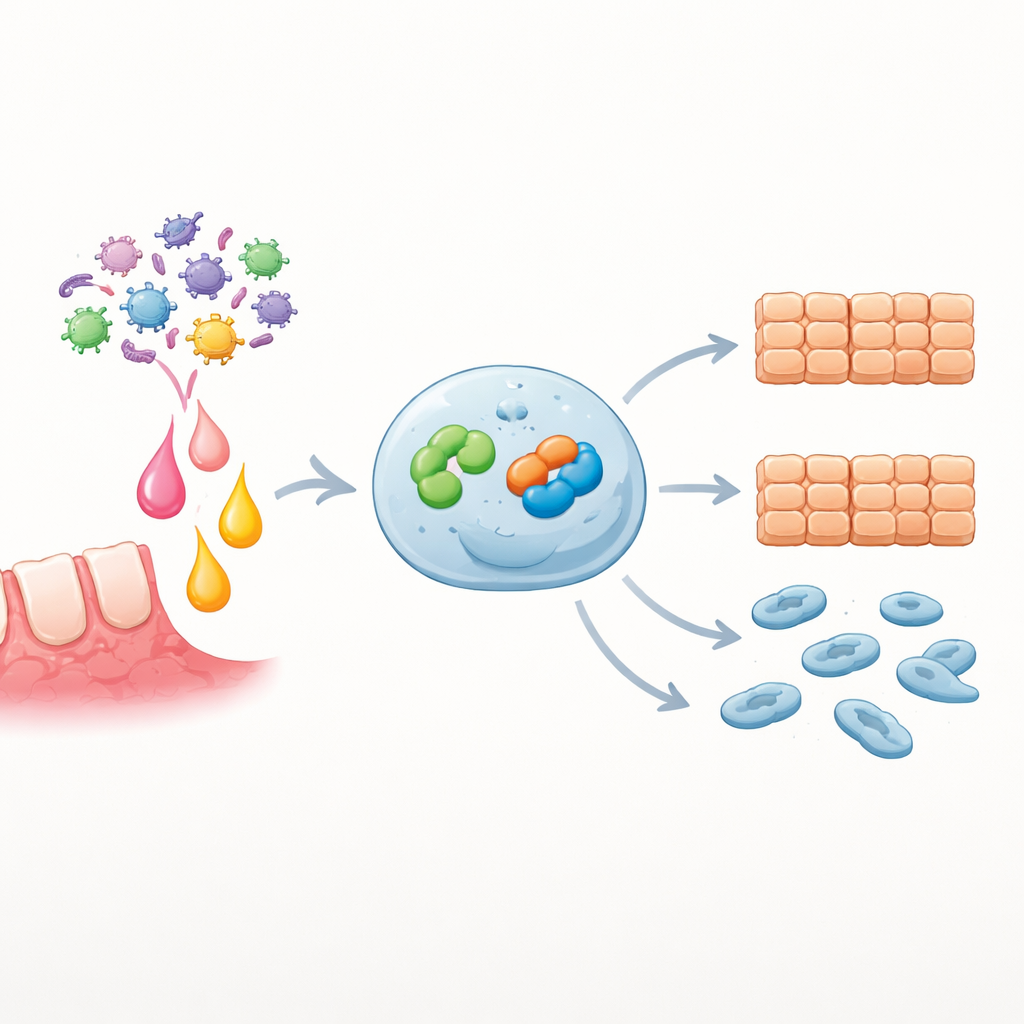
Bloccare la staffetta rallenta i tratti cancerosi
Per verificare se Snai2 è necessario per gli effetti di EZH2, i ricercatori hanno potenziato EZH2 ma contemporaneamente silenziato Snai2. In queste condizioni crescita cellulare, chiusura delle ferite e migrazione risultavano tutte significativamente ridotte rispetto alla sola sovraespressione di EZH2, indicando che Snai2 è un motore chiave dei tratti aggressivi indotti da EZH2. Nelle cellule tumorali primarie che rispondevano all’IL-6, l’aggiunta di un inibitore chimico di EZH2 o di piccoli RNA che abbassano Snai2 attenuava fortemente la proliferazione e la migrazione indotte dall’IL-6. Analisi bioinformatiche su grandi dataset di pazienti hanno rafforzato questi risultati sperimentali: l’espressione elevata di SNAI2 risultava arricchita in vie legate all’infezione e al movimento cellulare, e i pazienti i cui tumori presentavano maggiori livelli di SNAI2 tendevano ad avere una sopravvivenza peggiore.
Cosa significa per i pazienti e la prevenzione
Nel complesso, il lavoro delinea una storia chiara in termini semplici: un batterio della malattia gengivale aumenta i livelli di IL-6 nella bocca; l’IL-6 attiva EZH2 nelle cellule tumorali vicine; EZH2 a sua volta aumenta Snai2, che aiuta le cellule tumorali a distaccarsi e metastatizzare. Questa catena IL-6/EZH2/Snai2 collega le comuni infezioni orali a comportamenti tumorali potenzialmente letali e evidenzia nuovi punti di intervento. In futuro, un migliore controllo delle infezioni gengivali croniche, farmaci che attenuino i segnali di IL-6 o inibitori mirati di EZH2 o Snai2 potrebbero aiutare a rallentare la progressione dell’OSCC. Pur richiedendo conferme in modelli animali e studi clinici, questi risultati offrono un ponte molecolare concreto tra igiene orale e rischio di cancro — e un promettente insieme di bersagli per terapie più efficaci basate sulla biologia.
Citazione: Liu, S., Guan, T., Xu, B. et al. Porphyromonas gingivalis promotes oral squamous cell carcinoma progression via the IL-6/EZH2/Snai2 axis. Sci Rep 16, 10296 (2026). https://doi.org/10.1038/s41598-026-41528-w
Parole chiave: cancro orale, malattia gengivale, Porphyromonas gingivalis, infiammazione, segnalazione del cancro