Clear Sky Science · he
Porphyromonas gingivalis מקדמת את התקדמות סרטן התאים הסקוומיים של הפה דרך ציר IL-6/EZH2/Snai2
מדוע חיידק חניכיים חשוב בסרטן הפה
רוב האנשים רואים דימומים בחניכיים כמטרד דנטלי ולא כסיכון לסרטן. מחקר זה מראה כיצד חיידק נפוץ הגורם למחלות חניכיים, Porphyromonas gingivalis, יכול לתרום לצמיחה ולהתפשטות של קרצינומה של תאי אפיתל רירית הפה (OSCC), צורה שכיחה וקטלנית של סרטן הפה. על ידי מעקב אחרי שרשרת אירועים מהדבקה ועד שינוי התנהגותי של תאים, החוקרים מזהים נקודת תורשה מולקולרית שאפשר למקד בה כדי להאט או למנוע התקדמות סרטן.
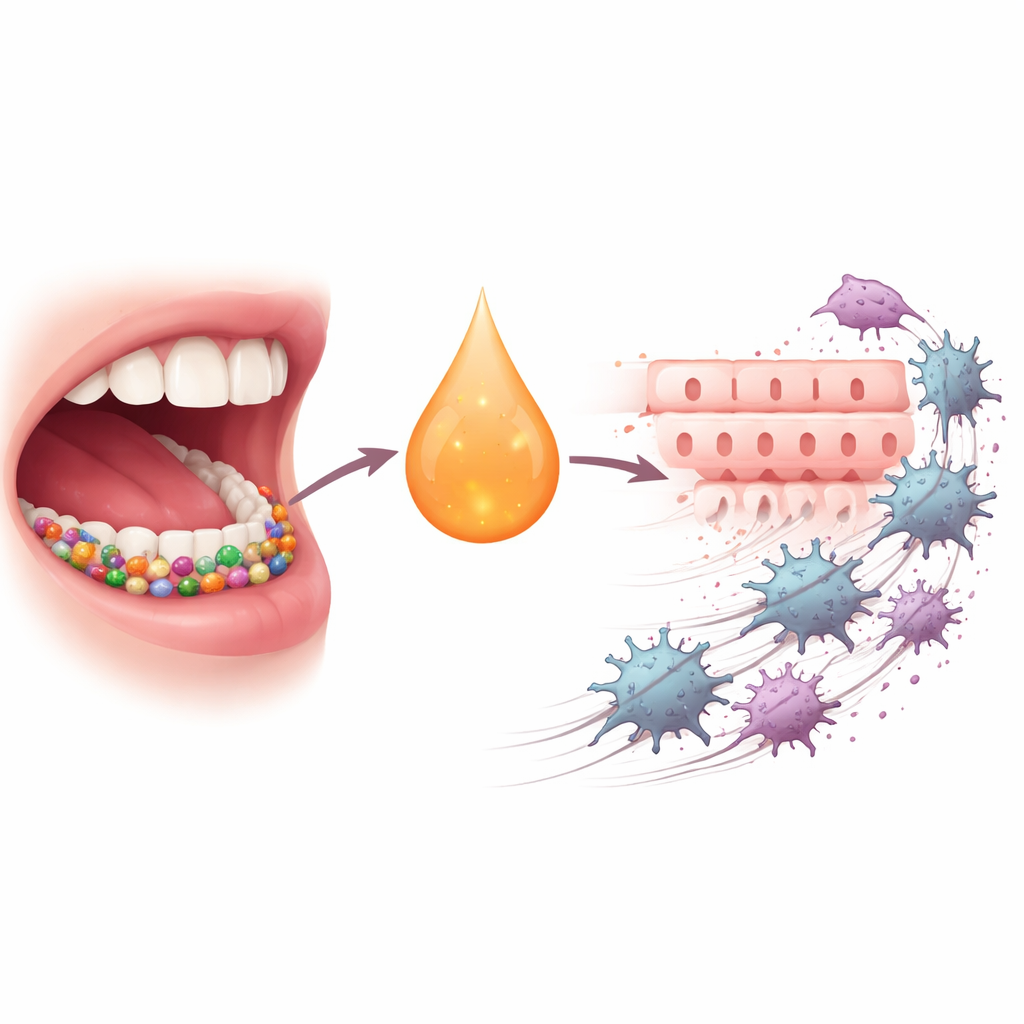
סרטן עקשן עם עוזרים נסתרים
קרצינומת תאי אפיתל רירית הפה (OSCC) נמנית בין עשרת סוגי הסרטן השכיחים בעולם וידועה כקשה לריפוי; למרות ניתוח, קרינה, כימותרפיה וטיפולים אימונותרפיים חדשים, פחות ממחצית המטופלים שורדים חמש שנים לאחר האבחון. בשנים האחרונות התברר שלקהילות המיקרובים בפה שלנו יש תפקיד מעבר לחריצות ושיניים רקובות או מחלות חניכיים. כשמאזן המיקרובים מופר, חיידקים מסוימים יכולים להעצים דלקת כרונית, לשנות את החיסון המקומי ולהדחיק תאים למצב תוקפני ונייד יותר. P. gingivalis, גורם מרכזי בפריודונטיטיס, נקשר שוב ושוב ל-OSCC ולמעבר תאי הנקרא epithelial–mesenchymal transition, שבו תאים סדרתיים במשטח נרפאים, זזים וחודרים לרקמות סמוכות.
מהדבקה בחניכיים לאותות כימיים חזקים
המחברים התחילו בשאלה האם הדבקה ב-P. gingivalis מעלה רמות של שליח דלקתי IL-6 בפיות המטופלים. מדידה של נוזל מחלל סביב השן הראתה שרמות IL-6 היו גבוהות בהרבה אצל חולי מחלות חניכיים הנושאים P. gingivalis וכמו גם אצל אנשים עם OSCC לעומת מתנדבים בריאים. הם אז חילצו תאים ראשוניים מהגידול של חולי OSCC וחשפו אותם ל-IL-6. תאים רבים העלו את רמות הקולטן ל-IL-6, מה שהגביר את תגובתם לאות. תאי הקולטן הגבוהים התחלקו מהר יותר והיגרו ביתר קלות — סימנים ברורים לאוכלוסיית תאים סרטניים אגרסיבית יותר.
מרוץ של שלושה שלבים בתוך תאי הגידול
בהעמקה פנימה, הצוות התמקד בשני חלבונים בתוך תאי הסרטן: EZH2, אנזים השולט באריזת ה-DNA ובאיזה גנים מופעלים, ו-Snai2, פקטור שעתוק הידוע בדחיפת תאים למצב נייד וחודר. הם מצאו שתאי OSCC כבר הכילו יותר EZH2 ו-Snai2 מתאים אוראליים תקינים, ושהגירוי ב-IL-6 הגביר את שני החלבונים ברמות RNA וחלבון. כאשר העלו באופן מלאכותי את EZH2 בקו תאי OSCC סטנדרטי, התאים גדלו מהר יותר ונעו יותר. דיכוי של EZH2 נתן את התוצאה ההפוכה, אך החזרת חלבון EZH2 השיבה את ההתנהגות האגרסיבית. באופן מכריע, שינויים ברמות EZH2 שינו ישירות את פעילות גן SNAI2 באותו כיוון, מה שמראה ש-EZH2 עומד מעל SNAI2 בשרשרת זו.
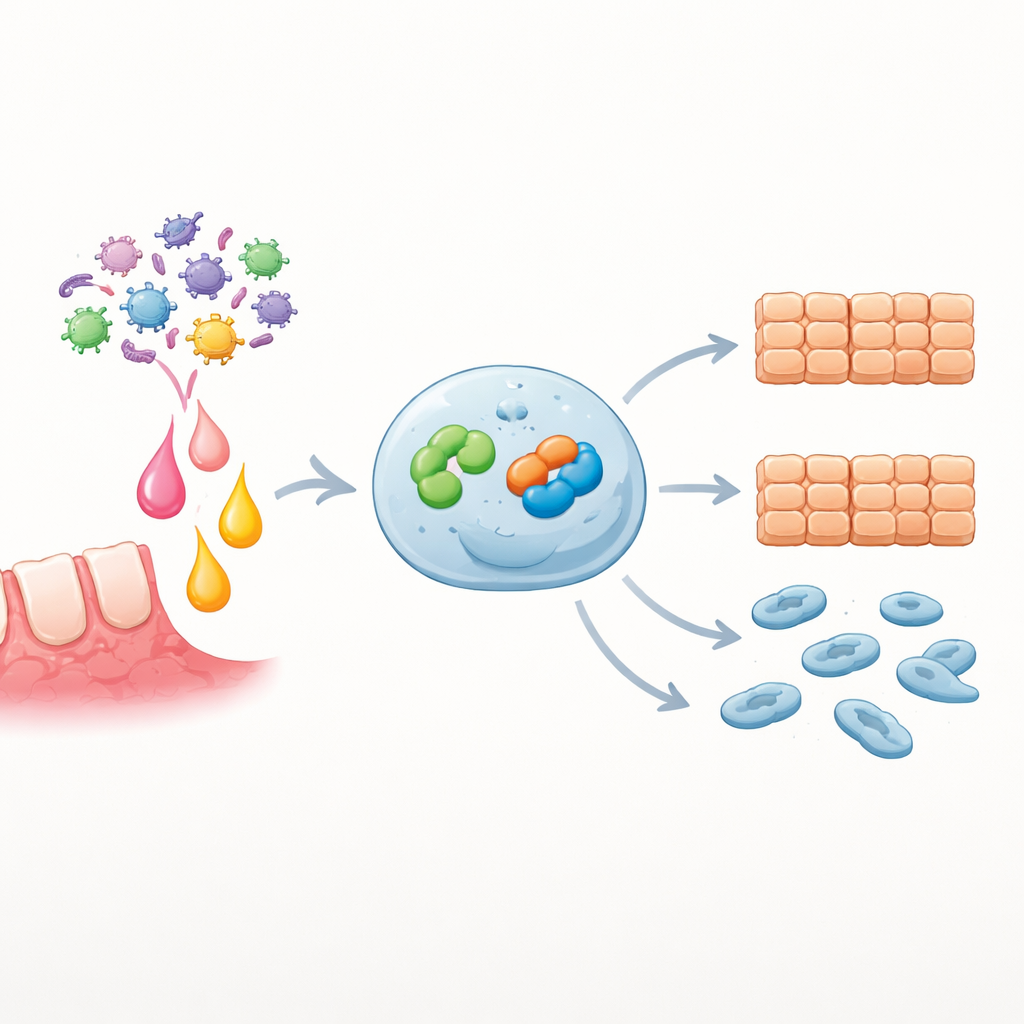
חסימת השרשרת מאטה תכונות סרטניות
כדי לבדוק האם SNAI2 נחוץ להשפעות של EZH2, החוקרים הגבירו EZH2 ובמקביל השתקו את SNAI2. בתנאים אלה, הגדילה התאית, סגירת פצעים וההגירה ירדו משמעותית בהשוואה להבעת יתר של EZH2 בלבד, מה שמעיד ש-SNAI2 הוא מנוע מרכזי של התכונות האגרסיביות המונעות על ידי EZH2. בתאי גידול ראשוניים שהגיבו ל-IL-6, הוספה של מדכא כימי ל-EZH2 או מולקולות RNA קטנות שדוכאות את SNAI2 הקטינו בחדות את ההתרבות וההגירה המועברות על ידי IL-6. ניתוחים ביואינפורמטיים של מאגרי נתונים רחבים של מטופלים חיזקו את הממצאים במעבדה: ביטוי גבוה של SNAI2 הועשר במסלולים הקשורים לזיהום ותנועת תאים, ומטופלים שלגידוליהם היה יותר SNAI2 נטו להישרדות גרועה יותר.
מה משמעות הדבר למטופלים ולמניעה
לסיכום, המחקר מציג סיפור ברור במונחים פשוטים: חיידק מחלות חניכיים מעלה רמות IL-6 בפה; IL-6 מפעיל את EZH2 בתאים הסמוכים של הגידול; EZH2 בתורו מעלה את SNAI2, שעוזר לתאי הסרטן להתנתק ולהתפשט. שרשרת IL-6/EZH2/Snai2 זו מקשרת בין זיהומי פה שכיחים להתנהגות סרטנית מסכנת חיים ומבליטה נקודות התערבות חדשות. בעתיד, שליטה טובה יותר בזיהום חניכיים כרוני, תרופות המחלישות את איתותי IL-6, או מעכבים ממוקדים של EZH2 או SNAI2 עשויים לעזור להאט התקדמות OSCC. למרות שממצאים אלו עדיין דורשים אישור במודלים חייתיים ובניסויים קליניים, הם מציעים גשר מולקולרי קונקרטי בין היגיינת הפה לסיכון לסרטן — וקבוצת מטרות מבטיחה לטיפולים מבוססי ביולוגיה יעילים יותר.
ציטוט: Liu, S., Guan, T., Xu, B. et al. Porphyromonas gingivalis promotes oral squamous cell carcinoma progression via the IL-6/EZH2/Snai2 axis. Sci Rep 16, 10296 (2026). https://doi.org/10.1038/s41598-026-41528-w
מילות מפתח: סרטן הפה, מחלות חניכיים, Porphyromonas gingivalis, דלקת, אותות סרטניים