Clear Sky Science · nl
Porphyromonas gingivalis bevordert de progressie van mondplaveiselcelcarcinoom via de IL-6/EZH2/Snai2-as
Waarom een tandvleesbacterie ertoe doet bij mondkanker
De meeste mensen zien bloedend tandvlees als een tandheelkundig ongemak, niet als een kankerrisico. Deze studie laat zien hoe een veelvoorkomende tandvleesbacterie, Porphyromonas gingivalis, de groei en verspreiding van mondplaveiselcelcarcinoom (OSCC), een veelvoorkomende en vaak dodelijke vorm van mondkanker, kan bevorderen. Door een keten van gebeurtenissen van infectie tot ontregeld celgedrag te volgen, identificeren de onderzoekers een moleculair zwak punt dat mogelijk aangegrepen kan worden om de tumorprogressie te vertragen of te voorkomen.
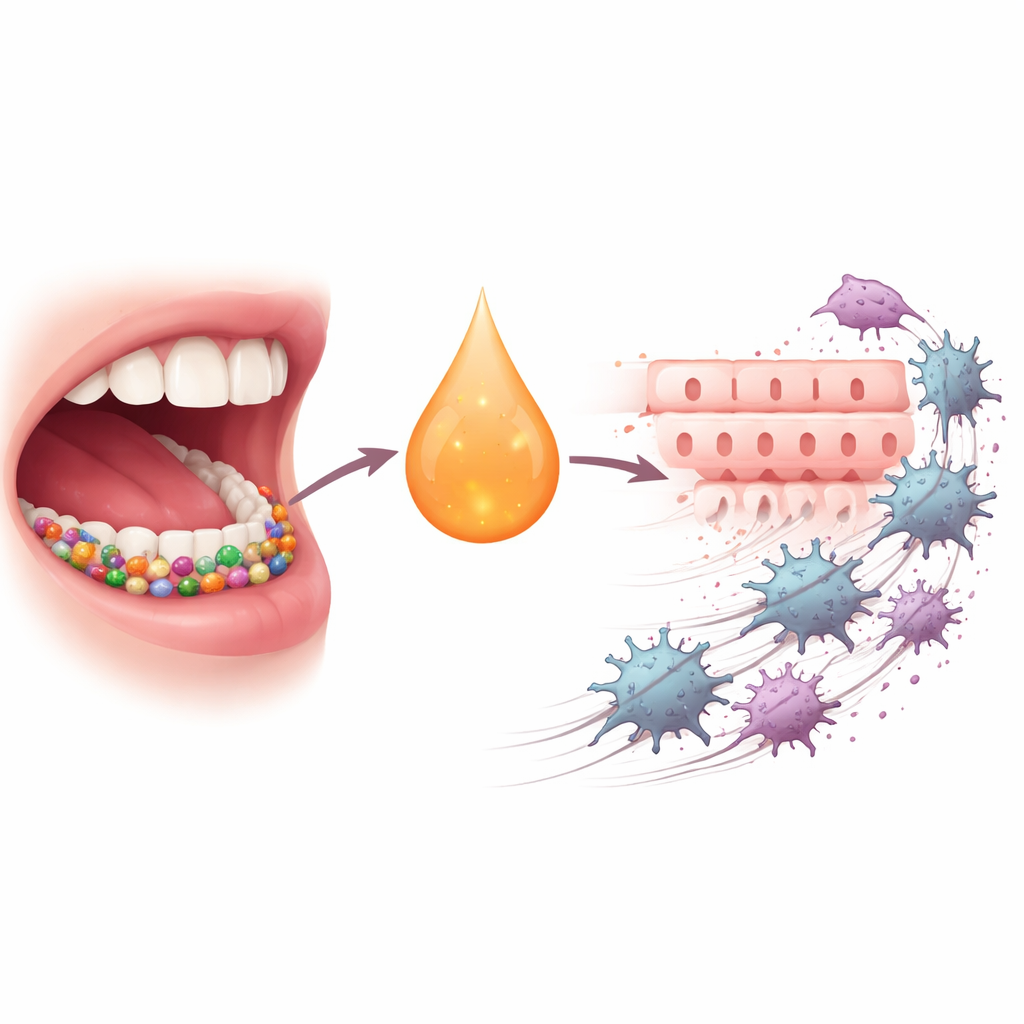
Een hardnekkige kanker met verborgen medestanders
Oral squamous cell carcinoma (OSCC) behoort tot de tien meest voorkomende kankers wereldwijd en is berucht moeilijk te genezen; ondanks chirurgie, bestraling, chemotherapie en nieuwere immunotherapieën is minder dan de helft van de patiënten vijf jaar na diagnose nog in leven. De laatste jaren beseffen wetenschappers dat de microbiegemeenschappen in onze mond meer doen dan alleen gaatjes of tandvleesontsteking veroorzaken. Wanneer hun balans verstoord raakt, kunnen bepaalde bacteriën chronische ontsteking aanwakkeren, de lokale immuniteit veranderen en cellen aanzetten tot agressievere, beweeglijkere toestanden. P. gingivalis, een belangrijke veroorzaker van parodontitis, is herhaaldelijk in verband gebracht met OSCC en met een cellulaire verschuiving die epithelial–mesenchymal transition wordt genoemd, waarbij orde- en oppervlakcelstructuren losser worden, zich verplaatsen en omliggend weefsel binnendringen.
Van tandvleesinfectie naar krachtige chemische signalen
De auteurs begonnen met de vraag of P. gingivalis-infectie de niveaus van de ontstekingsboodschapper IL-6 in de mond van patiënten verhoogt. Door vloeistof uit de tandvleesspleet te meten, vonden ze dat IL-6 veel hoger was zowel bij tandvleespatiënten die P. gingivalis droegen als bij mensen met OSCC dan bij gezonde vrijwilligers. Vervolgens isoleerden ze primaire tumorcellen van OSCC-patiënten en stelden die bloot aan IL-6. Veel van deze cellen verhoogden hun hoeveelheid van de IL-6-receptor, waardoor ze gevoeliger werden voor het signaal. De receptor-rijke cellen deelden sneller en migreerden gemakkelijker — duidelijke kenmerken van een gevaarlijker kankercelpopulatie.
Een driedelige relais binnen tumorcellen
Diepergaand richtte het team zich op twee eiwitten binnen kankercellen: EZH2, een enzym dat bepaalt hoe DNA wordt verpakt en welke genen aanstaan, en Snai2, een transcriptiefactor die cellen bekend staat te duwen naar een beweeglijkere, invasieve staat. Ze vonden dat OSCC-cellen al meer EZH2 en Snai2 hadden dan normale mondcellen, en dat IL-6-stimulatie beide eiwitten verder verhoogde op zowel RNA- als eiwitniveau. Wanneer ze EZH2 kunstmatig verhoogden in een standaard OSCC-celijn, groeiden de cellen sneller en bewogen ze meer. Het onderdrukken van EZH2 had het tegenovergestelde effect, maar het teruggeven van EZH2-eiwit herstelde het agressieve gedrag. Cruciaal was dat veranderingen in EZH2-niveaus rechtstreeks de activiteit van het SNAI2-gen in dezelfde richting verschoven, wat laat zien dat EZH2 boven SNAI2 in deze relais zit.
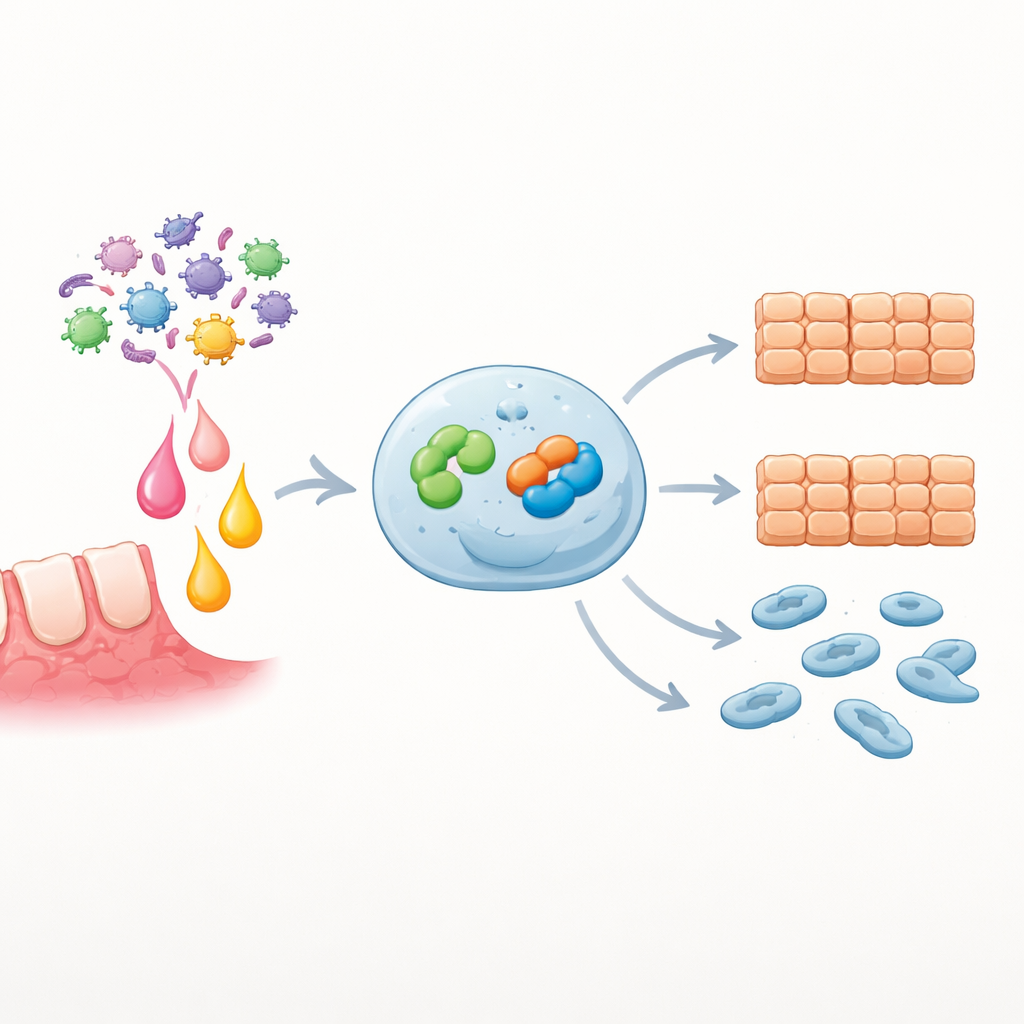
Het blokkeren van de relais remt kankereigenschappen
Om te testen of Snai2 nodig is voor de effecten van EZH2, verhoogden de onderzoekers EZH2 maar schakelden tegelijk Snai2 uit. Onder deze omstandigheden waren celgroei, wondsluiting en migratie allemaal significant verminderd vergeleken met enkel EZH2-overexpressie, wat aangeeft dat Snai2 een belangrijke motor is van de agressieve eigenschappen die door EZH2 worden gedreven. In primaire tumorcellen die op IL-6 reageerden, verminderde het toedienen van een chemische remmer van EZH2 of kleine RNA-moleculen die Snai2 onderdrukken de door IL-6 geïnduceerde proliferatie en migratie sterk. Bioinformatica-analyses van grote patiëntendatasets versterkten deze laboratoriumbevindingen: hoge SNAI2-expressie was verrijkt in routes die verband houden met infectie en celbeweging, en patiënten wiens tumoren meer SNAI2 hadden, hadden de neiging een slechtere overleving te hebben.
Wat dit betekent voor patiënten en preventie
Samengevat schetst het werk een helder verhaal in eenvoudige termen: een tandvleesbacterie verhoogt IL-6-niveaus in de mond; IL-6 schakelt EZH2 aan in nabijgelegen tumorcellen; EZH2 zet op zijn beurt Snai2 hoger, wat helpt dat kankercellen loskomen en zich verspreiden. Deze IL-6/EZH2/Snai2-keten koppelt alledaagse mondinfecties aan levensbedreigend kankergedrag en wijst op nieuwe interventiepunten. In de toekomst kan betere beheersing van chronische tandvleesinfectie, geneesmiddelen die IL-6-signalen dempen, of gerichte remmers van EZH2 of Snai2 helpen de progressie van OSCC te vertragen. Hoewel deze bevindingen nog bevestigd moeten worden in diermodellen en klinische studies, bieden ze een concreet moleculair brug tussen mondhygiëne en kankerrisico — en een veelbelovende set targets voor effectievere, op biologie gebaseerde behandelingen.
Bronvermelding: Liu, S., Guan, T., Xu, B. et al. Porphyromonas gingivalis promotes oral squamous cell carcinoma progression via the IL-6/EZH2/Snai2 axis. Sci Rep 16, 10296 (2026). https://doi.org/10.1038/s41598-026-41528-w
Trefwoorden: mondkanker, tandvleesontsteking, Porphyromonas gingivalis, ontsteking, kankersignalering