Clear Sky Science · sv
Porphyromonas gingivalis främjar progression av oralt skivepitelkarcinom via IL-6/EZH2/Snai2-axeln
Varför en tandköttsbakterie spelar roll för munncancer
De flesta ser blödande tandkött som ett tandvårdsproblem, inte en cancerrisk. Denna studie visar hur en vanlig bakterie vid tandköttssjukdom, Porphyromonas gingivalis, kan bidra till tillväxt och spridning av oralt skivepitelkarcinom, en vanlig och allvarlig form av munncancer. Genom att följa en kedja av händelser från infektion till okontrollerat cellbeteende identifierar forskarna en molekylär svag punkt som kan riktas för att bromsa eller förhindra cancerprogression.
En seglivad cancer med dolda medhjälpare
Oralt skivepitelkarcinom (OSCC) tillhör de tio vanligaste cancerformerna i världen och är beryktat svårt att bota; trots operation, strålning, cytostatika och nyare immunterapier är färre än hälften av patienterna vid liv fem år efter diagnos. Under senare år har forskare insett att mikrobiella samhällen i munnen gör mer än att orsaka karies eller tandköttssjukdom. När balansen rubbas kan vissa bakterier elda på kronisk inflammation, förändra lokal immunitet och driva celler mot mer aggressiva, rörliga tillstånd. P. gingivalis, en nyckelaktör vid parodontit, har gång på gång kopplats till OSCC och till en cellulär förskjutning kallad epitelial–mesenkymal övergång, där ordnade ytceller släpper taget, rör sig och invaderar omkringliggande vävnader.
Från tandköttsinfektion till kraftfulla kemiska signaler
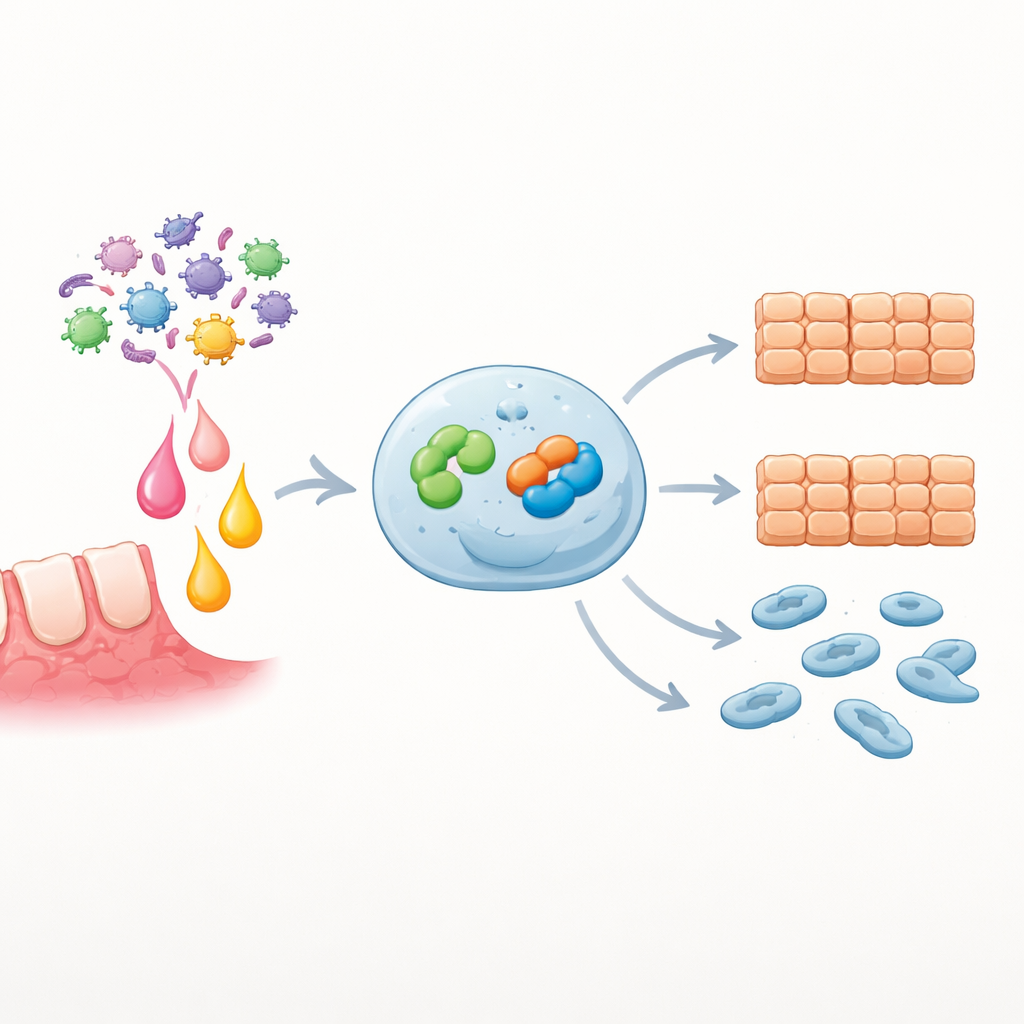
Författarna började med att undersöka om P. gingivalis-infektion höjer nivåerna av den inflammatoriska budbäraren IL-6 i patienternas munnar. Genom att mäta vätska från fickan runt tänderna fann de att IL-6 var mycket högre både hos tandköttssjuka patienter med P. gingivalis och hos personer med OSCC än hos friska frivilliga. De isolerade sedan primära tumörceller från OSCC-patienter och exponerade dem för IL-6. Många av dessa celler ökade uttrycket av IL-6-receptorn, vilket gjorde dem mer mottagliga för signalen. Receptorrika celler delade sig snabbare och migrerade lättare, tydliga kännetecken för en farligare cancercellspopulation.
En trestegssändning inne i tumörceller
Genom att gå djupare fokuserade teamet på två proteiner inne i cancerceller: EZH2, ett enzym som styr hur DNA paketeras och vilka gener som är aktiva, och Snai2, en transkriptionsfaktor känd för att driva celler mot ett mer rörligt, invasivt tillstånd. De fann att OSCC-celler redan hade mer EZH2 och Snai2 än normala munhåleceller, och att IL-6-stimulering ytterligare ökade båda proteinerna på RNA- och protein-nivå. När de konstgjort höjde EZH2 i en standard OSCC-cellinje växte cellerna snabbare och rörde sig mer. Nedreglering av EZH2 gav motsatt effekt, men återinförande av EZH2-protein återställde det aggressiva beteendet. Viktigt är att förändringar i EZH2-nivåer direkt försköt SNAI2-genens aktivitet i samma riktning, vilket visar att EZH2 ligger uppströms om Snai2 i denna sändningskedja.
Blockering av sändningen dämpar cancertendenser
För att testa om Snai2 är nödvändigt för EZH2:s effekter förstärkte forskarna EZH2 men tystade samtidigt Snai2. Under dessa förhållanden minskade celltillväxt, sårläkning och migration avsevärt jämfört med enbart EZH2-överuttryck, vilket indikerar att Snai2 är en central drivkraft för de aggressiva egenskaper som EZH2 framkallar. I primära tumörceller som svarade på IL-6 dämpade tillsats av antingen en kemisk hämmare av EZH2 eller små RNA-molekyler som slår ner Snai2 kraftigt den IL-6-inducerade proliferation och migrationen. Bioinformatiska analyser av stora patientdatamängder stärkade dessa laboratoriefynd: högt uttryck av SNAI2 var berikat i vägbanor relaterade till infektion och cellrörelse, och patienter vars tumörer hade mer SNAI2 tenderade att ha sämre överlevnad.
Vad detta betyder för patienter och förebyggande
Sammantaget beskriver arbetet en tydlig kedja i enkla termer: en tandköttssjukdomsbakterie höjer IL-6-nivåer i munnen; IL-6 slår på EZH2 inne i närliggande tumörceller; EZH2 i sin tur ökar Snai2, vilket hjälper cancerceller att bryta sig loss och sprida sig. Denna IL-6/EZH2/Snai2-kedja förenar vardagliga muninfektioner med livshotande cancerbeteenden och lyfter fram nya interventionspunkter. I framtiden kan bättre kontroll av kronisk tandköttsinflammation, läkemedel som dämpar IL-6-signaler eller riktade hämmare av EZH2 eller Snai2 bidra till att sakta OSCC-progression. Även om dessa fynd fortfarande behöver bekräftas i djurmodeller och kliniska studier erbjuder de en konkret molekylär brygga mellan munhygien och cancerrisk — och en lovande uppsättning mål för mer effektiva, biologibaserade behandlingar.
Citering: Liu, S., Guan, T., Xu, B. et al. Porphyromonas gingivalis promotes oral squamous cell carcinoma progression via the IL-6/EZH2/Snai2 axis. Sci Rep 16, 10296 (2026). https://doi.org/10.1038/s41598-026-41528-w
Nyckelord: munhålecancer, tandköttssjukdom, Porphyromonas gingivalis, inflammation, cancersignalering