Clear Sky Science · pl
Porphyromonas gingivalis wspomaga progresję płaskonabłonkowego raka jamy ustnej poprzez oś IL-6/EZH2/Snai2
Dlaczego bakteria dziąseł ma znaczenie dla raka jamy ustnej
Większość osób traktuje krwawiące dziąsła jako problem dentystyczny, a nie czynnik ryzyka raka. To badanie pokazuje, jak powszechna bakteria wywołująca choroby dziąseł, Porphyromonas gingivalis, może wspierać wzrost i rozprzestrzenianie się płaskonabłonkowego raka jamy ustnej (OSCC), częstej i groźnej odmiany tego nowotworu. Śledząc łańcuch zdarzeń od zakażenia do niekontrolowanego zachowania komórek, autorzy wskazują molekularny punkt wrażliwy, który mógłby być celem zahamowania lub zapobiegania progresji choroby.
Uporczywy nowotwór z ukrytymi wspomagaczami
Płaskonabłonkowy rak jamy ustnej (OSCC) należy do dziesięciu najczęstszych nowotworów na świecie i jest wyjątkowo trudny do wyleczenia; mimo operacji, radioterapii, chemioterapii i nowszych immunoterapii mniej niż połowa chorych przeżywa pięć lat od rozpoznania. W ostatnich latach naukowcy uświadomili sobie, że społeczności drobnoustrojów w ustach robią więcej niż tylko wywołują próchnicę czy zapalenie dziąseł. Gdy ich równowaga ulega zaburzeniu, niektóre bakterie mogą podsycać przewlekłe zapalenie, zmieniać miejscową odporność i przesuwać komórki w stronę bardziej agresywnych, ruchliwych stanów. P. gingivalis, kluczowy sprawca zapalenia przyzębia, wielokrotnie był powiązany z OSCC oraz ze zmianą komórkową zwaną przejściem nabłonkowo-mezenchymalnym, w którym uporządkowane komórki powierzchniowe rozluźniają się, przemieszczają i naciekają sąsiednie tkanki.
Od zakażenia dziąseł do silnych sygnałów chemicznych
Autorzy zaczęli od pytania, czy zakażenie P. gingivalis podnosi poziomy zapalnego przekaźnika IL-6 w jamach ustnych pacjentów. Mierząc płyn z kieszonek dziąsłowych, stwierdzili, że IL-6 był znacznie wyższy zarówno u pacjentów z chorobą dziąseł noszących P. gingivalis, jak i u osób z OSCC, w porównaniu ze zdrowymi ochotnikami. Następnie wyizolowali pierwotne komórki nowotworowe od pacjentów z OSCC i wystawili je na działanie IL-6. Wiele z tych komórek zwiększyło poziom receptora dla IL-6, co uczyniło je bardziej wrażliwymi na sygnał. Komórki o wysokiej ekspresji receptora dzieliły się szybciej i migrowały chętniej — oczywiste cechy bardziej niebezpiecznej populacji komórek nowotworowych.
Trzystopniowe przekazywanie wewnątrz komórek nowotworowych
Pogłębiając analizę, zespół skupił się na dwóch białkach wewnątrz komórek nowotworowych: EZH2, enzymie kontrolującym upakowanie DNA i aktywację genów, oraz Snai2, czynniku transkrypcyjnym znanym z popychania komórek w stronę bardziej ruchliwego, inwazyjnego stanu. Stwierdzili, że komórki OSCC miały już więcej EZH2 i Snai2 niż normalne komórki jamy ustnej, a stymulacja IL-6 dodatkowo zwiększała poziomy obu białek zarówno na poziomie RNA, jak i białka. Gdy sztucznie zwiększano EZH2 w standardowej linii komórkowej OSCC, komórki rosły szybciej i poruszały się więcej. Wyłączenie EZH2 dawało efekt przeciwny, ale przywrócenie białka EZH2 odtwarzało agresywne zachowanie. Co kluczowe, zmiany poziomu EZH2 bezpośrednio przesuwały aktywność genu Snai2 w tym samym kierunku, pokazując, że EZH2 działa nadrzędnie względem Snai2 w tym przekazie.
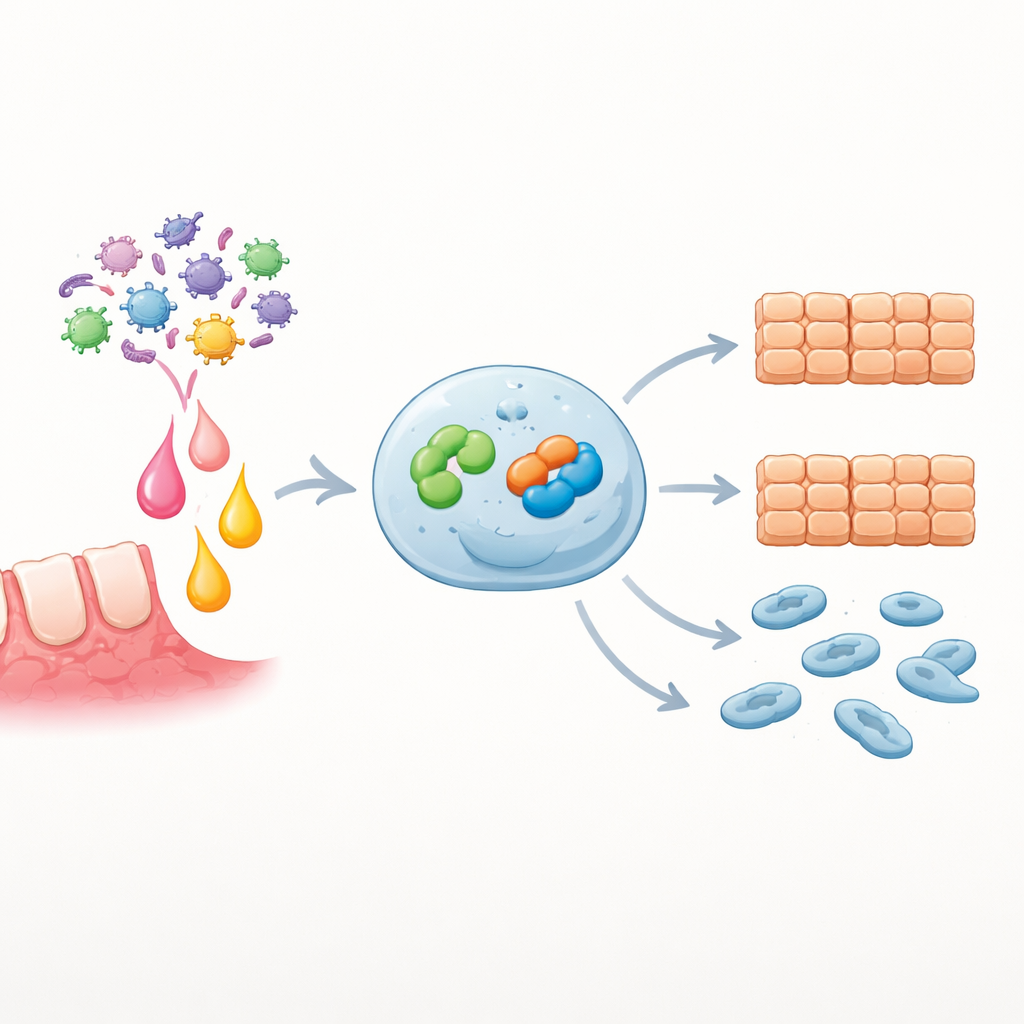
Blokowanie przekazu spowalnia cechy nowotworu
Aby sprawdzić, czy Snai2 jest konieczny dla efektów EZH2, badacze zwiększyli EZH2, ale jednocześnie stłumili Snai2. W tych warunkach wzrost komórek, zamykanie ran i migracja były wyraźnie zmniejszone w porównaniu z samym nadekspresją EZH2, co wskazuje, że Snai2 jest kluczowym silnikiem agresywnych cech napędzanych przez EZH2. W pierwotnych komórkach nowotworowych reagujących na IL-6 dodanie albo chemicznego inhibitora EZH2, albo krótkich cząsteczek RNA wyciszających Snai2 ostro stłumiło proliferację i migrację indukowaną przez IL-6. Analizy bioinformatyczne dużych zestawów danych pacjentów wzmocniły te wyniki laboratoryjne: wysoka ekspresja SNAI2 była wzbogacona w ścieżkach związanych z zakażeniem i ruchliwością komórek, a pacjenci, których guzy miały większe ilości SNAI2, mieli tendencję do gorszego przeżycia.
Co to oznacza dla pacjentów i profilaktyki
Podsumowując, praca przedstawia jasną historię w prostych słowach: bakteria powodująca chorobę dziąseł podnosi poziomy IL-6 w jamie ustnej; IL-6 włącza EZH2 w pobliskich komórkach nowotworowych; EZH2 z kolei zwiększa Snai2, które pomaga komórkom nowotworowym odrywać się i szerzyć. Ten łańcuch IL-6/EZH2/Snai2 łączy codzienne infekcje jamy ustnej ze zagrażającym życiu zachowaniem nowotworowym i uwydatnia nowe punkty interwencji. W przyszłości lepsza kontrola przewlekłych zakażeń przyzębia, leki tłumiące sygnały IL-6 albo celowane inhibitory EZH2 lub Snai2 mogą pomóc spowolnić progresję OSCC. Choć ustalenia te wymagają potwierdzenia w modelach zwierzęcych i badaniach klinicznych, oferują konkretne molekularne ogniwo między higieną jamy ustnej a ryzykiem raka — oraz obiecujący zestaw celów dla skuteczniejszych, opartych na biologii terapii.
Cytowanie: Liu, S., Guan, T., Xu, B. et al. Porphyromonas gingivalis promotes oral squamous cell carcinoma progression via the IL-6/EZH2/Snai2 axis. Sci Rep 16, 10296 (2026). https://doi.org/10.1038/s41598-026-41528-w
Słowa kluczowe: rak jamy ustnej, choroba dziąseł, Porphyromonas gingivalis, zapalenie, sygnalizacja nowotworowa