Clear Sky Science · zh
使用全基因组重亚硫酸盐测序数据检测癌症细胞系中的已知基因融合
为何“一次检测多项”很重要
肿瘤科医生越来越希望从单一 DNA 样本中获悉多种信息:哪些基因被开启或关闭、DNA 如何折叠或被复制,以及关键基因是否以有害方式被切接粘合。如今,这些问题通常需要多种实验室检测,每种都消耗宝贵的样本并增加成本。本研究探讨了一项广泛使用的检测 DNA 化学标记的方法——全基因组重亚硫酸盐测序(WGBS)是否也能揭示基因融合——即常驱动癌症并影响治疗选择的两个基因异常连接。
癌症中的奇异基因拼接
基因融合发生于染色体断裂并错误重连,将两种不同基因的片段拼接在一起。这类拼接可放大生长信号、沉默保护性基因或产生推动细胞走向癌变的杂合蛋白。著名例子包括慢性髓性白血病中的 BCR–ABL1 融合,以及决定前列腺癌和肺癌用药选择的各种融合。鉴于其临床重要性,实验室通常通过针对 RNA 的检测或全基因组扫描来寻找融合,而不是使用为读取 DNA 化学标记设计的方法。
一种强大但被低估的数据来源
全基因组重亚硫酸盐测序(WGBS)旨在绘制 DNA “甲基化”分布——这些小型化学标签帮助调控基因活性。它已成为基础研究和分析血液中游离 DNA 片段的液体活检检测的主力工具。从一次 WGBS 测序中,研究人员已经可以提取甲基化、拷贝数变化、单碱基突变以及 DNA 片段化特征等信息。然而,融合检测一直不在这张清单上。其障碍在于 WGBS 使用的化学处理会把 DNA 断成更短的片段并将许多胞嘧啶发生转化,使得所得序列更难准确比对到参考基因组上。
教会融合检测工具新把戏
作者们着手通过采用能理解重亚硫酸盐处理后 DNA 特征并能处理“分裂”读段(即部分比对到一个基因、部分比对到另一个基因的短序列)的软件,将 WGBS 数据改造为可用于发现融合的资源。他们侧重于已知的融合事件,而不是在整个基因组中盲目搜寻。首先,他们在携带广泛研究的 BCR–ABL1 融合的 K562 白血病细胞上测试了管线。来自 WGBS 的断点与传统全基因组测序所得结果高度一致,融合位点周围的覆盖度下降在两类数据中都能观察到。团队还表明,当样本中来自融合阳性细胞的 DNA 约占 8% 时,WGBS 就能可靠检测到该融合;在相对深度测序条件下,当该比例达到 10% 时检测达到完美。
扩大规模以同时检测多处融合
接着,研究人员考察了他们的方法是否能处理同一样本中的多个融合。他们将其应用于携带十几处已确认基因融合的 MCF-7 乳腺癌细胞。基于 WGBS 的方法恢复了其中 12 个融合中的 10 个,涵盖了单染色体内部的重排以及跨染色体的连接。支持融合的读段计数在重复实验间高度一致,表明该方法具有技术稳定性。同时,作者们也揭示了一个关键限制:当他们在感兴趣的特定基因区域之外检索时,类似假融合的背景信号比真实融合更常见。这表明 WGBS 更适合用于已知融合的有针对性检测,而不适合用于开放式的盲目筛查。
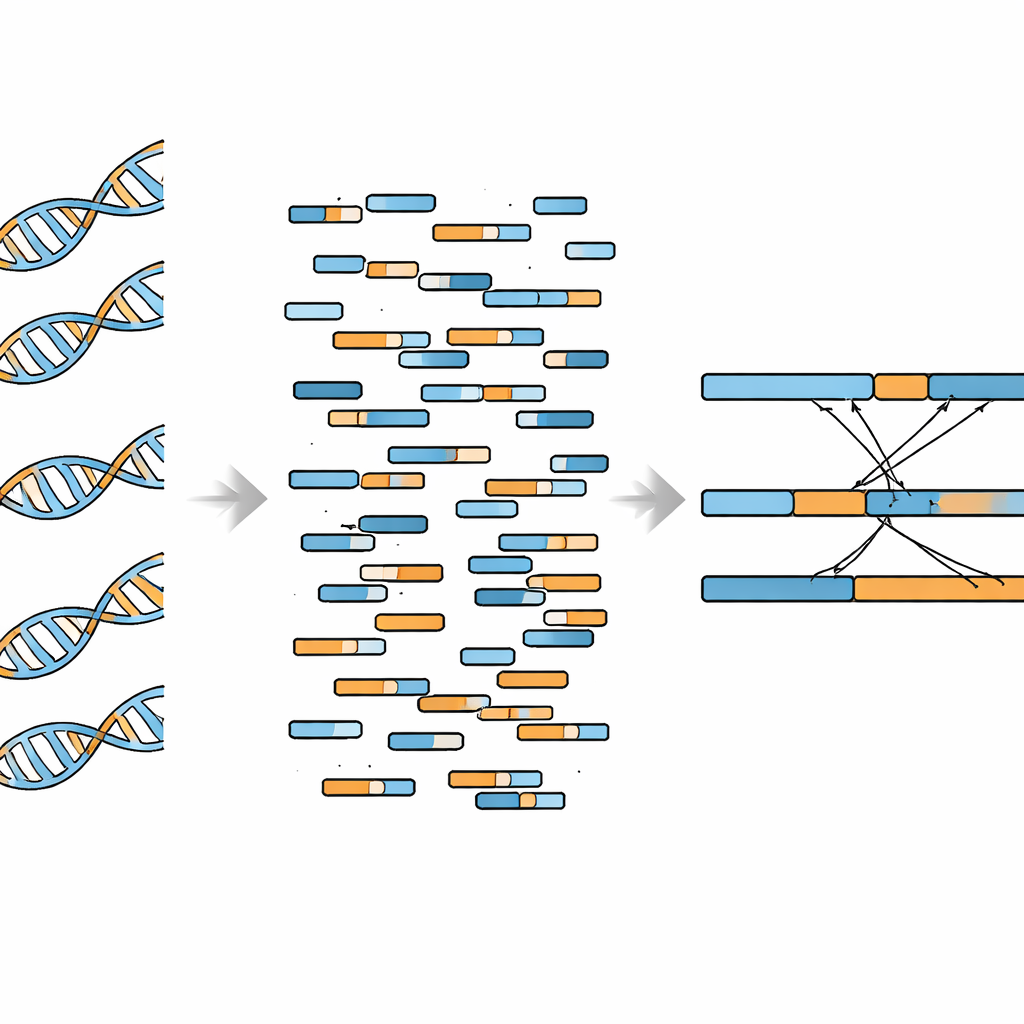
前景与实际限制
虽然结果令人鼓舞,但也指出了边界。实验在均一的细胞系中进行,而非真实的患者样本——在患者样本中癌细胞更为混杂,融合断点也可能因人而异。仅略高于 8% 的肿瘤来源 DNA 检出阈值适合于肿瘤细胞往往占优势的组织活检,但对于必须从微量肿瘤 DNA 中筛选的血液检测来说可能不足。此外,达到所需测序深度代价不菲,且那些位于已知基因边界之外的融合按设计仍会被漏检。
这对未来癌症检测意味着什么
本研究表明,原本用于读取 DNA 化学标记的数据集可以被重新利用来识别重要的基因融合,至少在这些融合是事先已知并存在于合理比例时适用。对于已经使用 WGBS 的研究者和临床医生而言,这意味着每次实验可提取更多价值:甲基化模式、其他基因改变以及现在的融合事件都可以从同一次测序中评估。通过进一步改进、在患者样本中验证并借助更智能的软件,WGBS 有望成为一个核心的多层次检测平台,从一个宝贵样本中提供关于癌症构成及最佳治疗路径的多重洞见。
引用: Kim, T., Bang, D. Detection of known gene fusions in cancer cell lines using whole-genome bisulfite sequencing data. Sci Rep 16, 13254 (2026). https://doi.org/10.1038/s41598-026-40803-0
关键词: 基因融合, DNA 甲基化, 全基因组重亚硫酸盐测序, 癌症基因组学, 液体活检