Clear Sky Science · es
Detección de fusiones génicas conocidas en líneas celulares cancerosas mediante secuenciación bisulfito del genoma completo
Por qué importa una prueba que haga más cosas
Los oncólogos cada vez quieren aprender más a partir de una única muestra de ADN: qué genes están encendidos o apagados, cómo se pliega o se copia el ADN y si genes clave han sido cortados y pegados de forma anómala. Hoy, esas preguntas suelen requerir varias pruebas de laboratorio diferentes, cada una consumiendo material valioso y elevando los costes. Este estudio pregunta si una prueba ampliamente utilizada para detectar marcas químicas en el ADN, llamada secuenciación bisulfito del genoma completo, también puede revelar fusiones génicas — las uniones anómalas de dos genes que con frecuencia impulsan el cáncer y orientan las decisiones terapéuticas.
Extrañas combinaciones génicas en el cáncer
Las fusiones génicas surgen cuando los cromosomas se rompen y se reensamblan en lugares equivocados, uniendo fragmentos de dos genes distintos. Estos empalmes pueden potenciar señales de crecimiento, silenciar genes protectores o crear proteínas híbridas que empujan a las células hacia el cáncer. Ejemplos famosos incluyen la fusión BCR–ABL1 en la leucemia mieloide crónica y fusiones en cánceres de próstata y pulmón que determinan qué fármacos serán eficaces. Debido a su importancia clínica, los laboratorios suelen buscar fusiones mediante pruebas dirigidas al ARN o escaneando todo el genoma, no con métodos diseñados para leer las marcas químicas del ADN.
Una fuente de datos potente pero infrautilizada
La secuenciación bisulfito del genoma completo (WGBS) fue concebida para mapear la "metilación" del ADN — pequeñas marcas químicas que ayudan a controlar qué genes están activos. Se ha convertido en una herramienta clave tanto para la investigación básica como para pruebas de biopsia líquida que analizan fragmentos de ADN en el torrente sanguíneo. A partir de una ejecución de WGBS, los científicos ya pueden extraer información sobre metilación, variaciones en el número de copias, mutaciones puntuales y cómo se fragmenta el ADN. Sin embargo, la detección de fusiones faltaba en esa lista. El obstáculo es que el tratamiento químico usado en WGBS rompe el ADN en piezas más cortas y convierte muchas bases de citosina, lo que dificulta alinear con precisión las secuencias resultantes con el genoma de referencia.
Enseñar a las herramientas de detección de fusiones un nuevo truco
Los autores se propusieron adaptar los datos de WGBS para el descubrimiento de fusiones usando software que comprende las particularidades del ADN tratado con bisulfito y puede manejar lecturas "divididas" — secuencias cortas que se alinean en parte con un gen y en parte con otro. Se centraron en eventos de fusión ya conocidos en lugar de buscar a ciegas en todo el genoma. Primero probaron su canalización en células de leucemia K562, que portan la bien estudiada fusión BCR–ABL1. Los puntos de ruptura identificados por WGBS coincidieron estrechamente con los obtenidos mediante secuenciación del genoma completo tradicional, y en ambos tipos de datos se observaron caídas de cobertura alrededor del sitio de fusión. El equipo también mostró que WGBS podía detectar la fusión de forma fiable cuando apenas alrededor del 8% del ADN en una muestra procedía de células con la fusión, con detección perfecta una vez que esta fracción alcanzaba el 10% con una profundidad de secuenciación relativamente alta.
Escalar para detectar muchas fusiones a la vez
A continuación, los investigadores preguntaron si su enfoque podía manejar varias fusiones en la misma muestra. Lo aplicaron a las células de cáncer de mama MCF-7, que albergan una docena de fusiones génicas previamente confirmadas. Su método basado en WGBS recuperó 10 de esas 12 fusiones, abarcando tanto reordenamientos dentro de un mismo cromosoma como aquellos que unen dos cromosomas distintos. Los recuentos de lecturas de apoyo fueron muy consistentes entre experimentos repetidos, lo que demuestra que el método es técnicamente estable. Al mismo tiempo, los autores identificaron una limitación clave: cuando miraron fuera de las regiones génicas específicas de interés, las señales de fondo que se asemejaban a fusiones falsas eran mucho más comunes que las verdaderas. Esto sugiere que WGBS funciona mejor para comprobaciones dirigidas de fusiones conocidas en lugar de búsquedas abiertas y exploratorias.
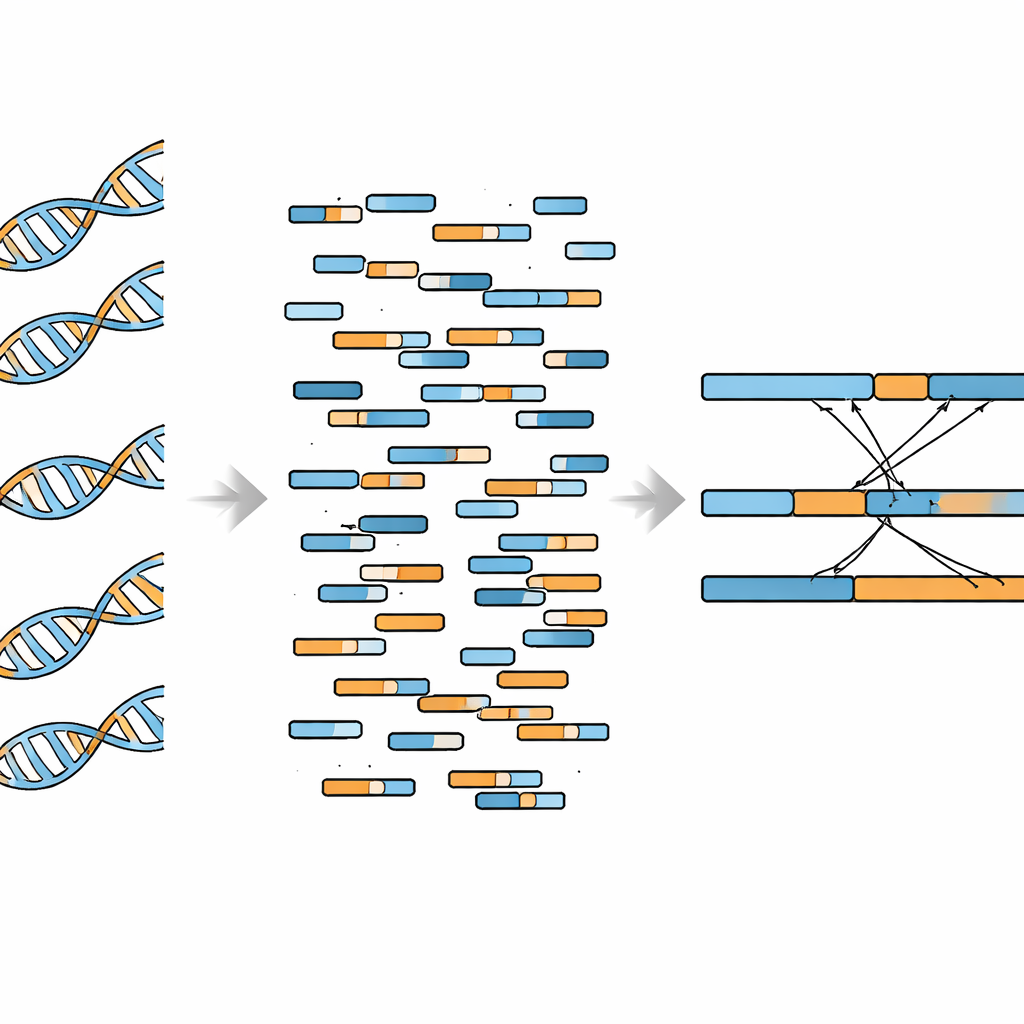
Promesa y límites prácticos
Aunque los resultados son alentadores, también resaltan sus límites. Las pruebas se realizaron en líneas celulares homogéneas, no en muestras de pacientes reales donde las células tumorales están más mezcladas y los puntos de ruptura de las fusiones pueden variar entre individuos. El umbral de detección de poco más del 8% de ADN derivado del tumor es adecuado para biopsias tisulares, donde las células cancerosas suelen predominar, pero puede quedarse corto para pruebas en sangre que deben detectar rastros mínimos de ADN tumoral. Alcanzar la profundidad de secuenciación requerida también resulta costoso, y algunas fusiones que caen fuera de los límites de los genes conocidos seguirán pasando desapercibidas por diseño.
Qué significa esto para las futuras pruebas del cáncer
Este estudio demuestra que un conjunto de datos recogido originalmente para leer marcas químicas en el ADN puede reutilizarse para detectar fusiones génicas importantes, al menos cuando esas fusiones son conocidas de antemano y están presentes en niveles razonables. Para investigadores y clínicos que ya usan WGBS, esto significa extraer más valor de cada experimento: patrones de metilación, otros cambios genéticos y ahora eventos de fusión pueden evaluarse desde la misma corrida. Con más refinamiento, validación en muestras de pacientes y software más inteligente, WGBS podría convertirse en un ensayo central que alimente muchas capas de información sobre cómo está constituido un cáncer — y cómo tratarlo mejor — a partir de una muestra valiosa.
Cita: Kim, T., Bang, D. Detection of known gene fusions in cancer cell lines using whole-genome bisulfite sequencing data. Sci Rep 16, 13254 (2026). https://doi.org/10.1038/s41598-026-40803-0
Palabras clave: fusión génica, metilación del ADN, secuenciación bisulfito del genoma completo, genómica del cáncer, biopsia líquida