Clear Sky Science · fr
Détection de fusions géniques connues dans des lignées cellulaires cancéreuses à l’aide de données de séquençage du génome entier après traitement au bisulfite
Pourquoi un test qui en fait plus est important
Les oncologues veulent de plus en plus tirer de nombreuses informations d’un seul prélèvement d’ADN : quels gènes sont activés ou réprimés, comment l’ADN est organisé ou dupliqué, et si des gènes clés ont été coupés et recollés de manière pathogène. Aujourd’hui, ces questions exigent généralement plusieurs tests de laboratoire différents, chacun consommant du matériel précieux et augmentant les coûts. Cette étude examine si un test largement utilisé pour repérer les marques chimiques sur l’ADN, appelé séquençage du génome entier après bisulfite (WGBS), peut également révéler des fusions géniques — des jonctions anormales de deux gènes qui conduisent souvent au cancer et orientent le choix des traitements.
Curieuses recombinaisons de gènes dans le cancer
Les fusions géniques apparaissent lorsque des chromosomes se cassent et se rattachent aux mauvais endroits, accolant des segments de deux gènes différents. Ces recombinaisons peuvent amplifier des signaux de croissance, faire taire des gènes protecteurs ou créer des protéines hybrides qui favorisent la transformation tumorale. Des exemples célèbres incluent la fusion BCR–ABL1 dans la leucémie myéloïde chronique et des fusions dans les cancers de la prostate et du poumon qui déterminent l’efficacité de certains médicaments. En raison de leur importance clinique, les laboratoires cherchent généralement les fusions avec des tests ciblant l’ARN ou en analysant l’ensemble du génome, plutôt qu’avec des méthodes conçues pour lire les marques chimiques de l’ADN.
Une source de données puissante mais sous-exploitée
Le WGBS a été conçu pour cartographier la « méthylation » de l’ADN — de petites étiquettes chimiques qui contribuent au contrôle de l’activité des gènes. Il est devenu un outil de référence pour la recherche fondamentale et pour les tests de biopsie liquide qui analysent des fragments d’ADN circulant dans le sang. À partir d’une seule expérience WGBS, les chercheurs peuvent déjà extraire des informations sur la méthylation, les variations du nombre de copies, les mutations ponctuelles et la fragmentation de l’ADN. Cependant, la détection de fusions faisait défaut à cette panoplie. L’obstacle tient au fait que le traitement chimique utilisé en WGBS fragmente l’ADN en morceaux plus courts et convertit de nombreux résidus de cytosine, rendant les séquences résultantes plus difficiles à aligner précisément sur le génome de référence.
Apprendre aux outils de détection de fusions une nouvelle astuce
Les auteurs ont cherché à adapter les données WGBS à la découverte de fusions en utilisant des logiciels capables de prendre en compte les particularités de l’ADN traité au bisulfite et de gérer les « reads fractionnés » — des lectures courtes qui s’alignent partiellement sur un gène et partiellement sur un autre. Ils se sont concentrés sur des événements de fusion connus plutôt que de chercher aveuglément à l’échelle du génome. D’abord, ils ont testé leur chaîne de traitement sur les cellules leucémiques K562, qui portent la fusion BCR–ABL1 bien étudiée. Les points de rupture identifiés à partir du WGBS correspondaient étroitement à ceux trouvés par séquençage classique du génome entier, et des creux de couverture autour du site de fusion apparaissaient dans les deux types de données. L’équipe a également montré que le WGBS pouvait détecter la fusion de façon fiable lorsque seulement environ 8 % de l’ADN d’un échantillon provenait de cellules porteuses de la fusion, avec une détection parfaite dès que cette fraction atteignait 10 % à des profondeurs de séquençage relativement élevées.
Passer à l’échelle : plusieurs fusions à la fois
Puis, les chercheurs ont évalué si leur approche pouvait gérer plusieurs fusions dans un même échantillon. Ils l’ont appliquée aux cellules mammaires cancéreuses MCF-7, qui abritent une douzaine de fusions géniques préalablement confirmées. Leur méthode basée sur le WGBS en a retrouvé 10 sur ces 12 fusions, couvrant à la fois des réarrangements à l’intérieur d’un même chromosome et des jonctions entre deux chromosomes différents. Le nombre de lectures supportant chaque fusion était très cohérent entre les répétitions expérimentales, montrant que la méthode est techniquement stable. Dans le même temps, les auteurs ont mis en évidence une limite importante : lorsqu’ils examinaient des régions génomiques en dehors des gènes ciblés, des signaux de fond ressemblant à de fausses fusions étaient beaucoup plus fréquents que les vraies. Cela suggère que le WGBS est mieux adapté aux vérifications ciblées de fusions connues qu’aux recherches exploratoires à grande échelle.
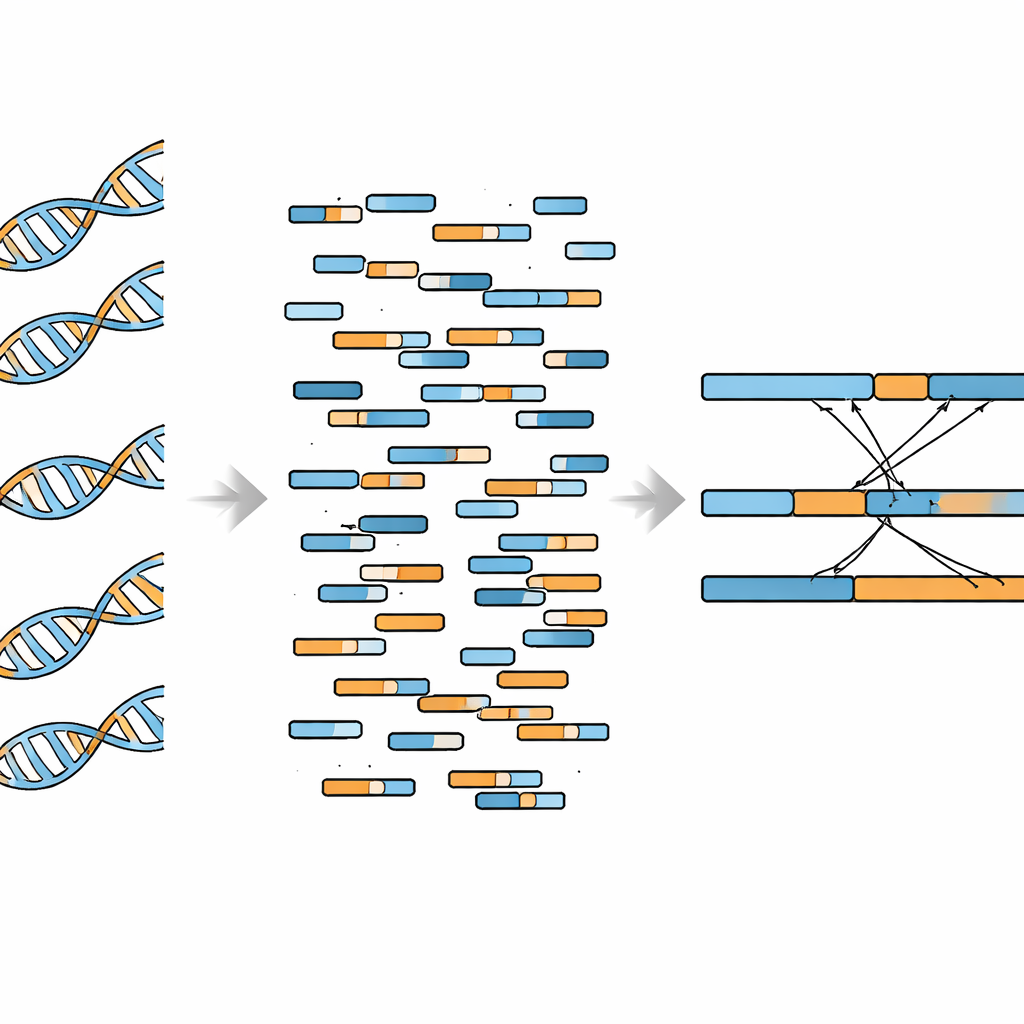
Promesses et limites pratiques
Si les résultats sont encourageants, ils soulignent aussi des limites. Les tests ont été réalisés sur des lignées cellulaires homogènes, et non sur des échantillons de patients où les cellules tumorales sont plus mélangées et où les points de rupture des fusions peuvent varier d’un individu à l’autre. Le seuil de détection, un peu supérieur à 8 % d’ADN d’origine tumorale, convient bien aux biopsies tissulaires où les cellules cancéreuses sont souvent abondantes, mais peut être insuffisant pour des tests sanguins qui doivent repérer de très faibles quantités d’ADN tumoral. Atteindre la profondeur de séquençage requise est aussi coûteux, et certaines fusions situées en dehors des frontières géniques connues resteront manquées par conception.
Ce que cela implique pour les tests du cancer à venir
Cette étude montre qu’un jeu de données initialement collecté pour lire les marques chimiques de l’ADN peut être réutilisé pour repérer des fusions géniques importantes, du moins lorsque ces fusions sont connues à l’avance et présentes à des niveaux raisonnables. Pour les chercheurs et cliniciens qui utilisent déjà le WGBS, cela signifie qu’on peut tirer plus de valeur d’une même expérience : profils de méthylation, autres altérations génétiques et désormais événements de fusion peuvent tous être évalués à partir d’un seul séquençage. Avec des raffinements supplémentaires, une validation sur des échantillons de patients et des logiciels plus avancés, le WGBS pourrait devenir un test central fournissant plusieurs couches d’informations sur la constitution d’un cancer — et sur la meilleure façon de le traiter — à partir d’un échantillon unique et précieux.
Citation: Kim, T., Bang, D. Detection of known gene fusions in cancer cell lines using whole-genome bisulfite sequencing data. Sci Rep 16, 13254 (2026). https://doi.org/10.1038/s41598-026-40803-0
Mots-clés: fusion génique, méthylation de l’ADN, séquençage du génome entier après bisulfite, génomique du cancer, biopsie liquide