Clear Sky Science · pt
Detecção de fusões gênicas conhecidas em linhagens celulares cancerosas usando dados de sequenciamento bisulfito de genoma inteiro
Por que um teste que faz mais é importante
Médicos oncologistas cada vez mais querem extrair muitas informações de uma única amostra de DNA: quais genes estão ligados ou desligados, como o DNA está dobrado ou copiado e se genes-chave foram cortados e colados de forma prejudicial. Hoje, essas questões normalmente exigem vários testes laboratoriais diferentes, cada um consumindo material precioso e aumentando o custo. Este estudo pergunta se um teste amplamente usado para marcar quimicamente o DNA, chamado sequenciamento bisulfito de genoma inteiro, também pode revelar fusões gênicas — as junções anormais de dois genes que frequentemente impulsionam o câncer e orientam escolhas de tratamento.
Estranhas misturas gênicas no câncer
Fusões gênicas surgem quando cromossomos se quebram e se religam em locais errados, emendando pedaços de dois genes diferentes. Essas misturas podem superestimular sinais de crescimento, silenciar genes protetores ou criar proteínas híbridas que empurram células em direção ao câncer. Exemplos famosos incluem a fusão BCR–ABL1 na leucemia mieloide crônica e fusões em cânceres de próstata e pulmão que determinam quais medicamentos serão eficazes. Devido à sua importância clínica, laboratórios normalmente procuram fusões usando testes voltados especificamente para RNA ou varrendo o genoma inteiro, não com métodos projetados para ler marcas químicas no DNA.
Uma fonte de dados poderosa, mas subutilizada
O sequenciamento bisulfito de genoma inteiro (WGBS) foi projetado para mapear a “metilação” do DNA — pequenas marcas químicas que ajudam a controlar quais genes estão ativos. Tornou-se uma ferramenta central tanto para pesquisa básica quanto para testes de biópsia líquida que analisam fragmentos de DNA na corrente sanguínea. A partir de uma execução de WGBS, cientistas já podem extrair informações sobre metilação, alterações no número de cópias, mutações pontuais e como o DNA é fragmentado. No entanto, a detecção de fusões estava ausente dessa lista. O obstáculo é que o tratamento químico usado no WGBS quebra o DNA em pedaços mais curtos e converte muitas bases de citosina, tornando as sequências resultantes mais difíceis de alinhar com precisão ao genoma de referência.
Ensinando às ferramentas de busca de fusões um novo truque
Os autores propuseram adaptar dados de WGBS para descoberta de fusões usando softwares que compreendam as peculiaridades do DNA tratado com bisulfito e que possam lidar com leituras “split” — sequências curtas que mapeiam parcialmente para um gene e parcialmente para outro. Eles se concentraram em eventos de fusão conhecidos em vez de buscar cegamente por todo o genoma. Primeiro, testaram seu fluxo de trabalho em células de leucemia K562, que carregam a bem-estudada fusão BCR–ABL1. Os pontos de quebra identificados a partir do WGBS coincidiram de perto com os obtidos por sequenciamento genômico tradicional, e quedas de cobertura ao redor do local da fusão apareceram em ambos os tipos de dado. A equipe também demonstrou que o WGBS podia detectar a fusão de forma confiável quando apenas cerca de 8% do DNA na amostra vinha de células com a fusão, com detecção perfeita uma vez que essa fração atingia 10% em profundidade de sequenciamento relativamente alta.
Escalando para muitas fusões ao mesmo tempo
Em seguida, os pesquisadores questionaram se sua abordagem poderia lidar com várias fusões na mesma amostra. Aplicaram-na a células de câncer de mama MCF-7, que abrigam uma dúzia de fusões gênicas previamente confirmadas. Seu método baseado em WGBS recuperou 10 dessas 12 fusões, abrangendo tanto rearranjos dentro de um mesmo cromossomo quanto aqueles que ligam dois cromossomos diferentes. As contagens de leituras de suporte foram altamente consistentes entre experimentos repetidos, mostrando que o método é tecnicamente estável. Ao mesmo tempo, os autores revelaram uma limitação chave: quando olharam fora das regiões gênicas específicas de interesse, sinais de fundo que se pareciam com fusões falsas eram bem mais comuns do que sinais verdadeiros. Isso sugere que o WGBS funciona melhor para checagens direcionadas de fusões conhecidas do que para expedições de pesca exploratória.
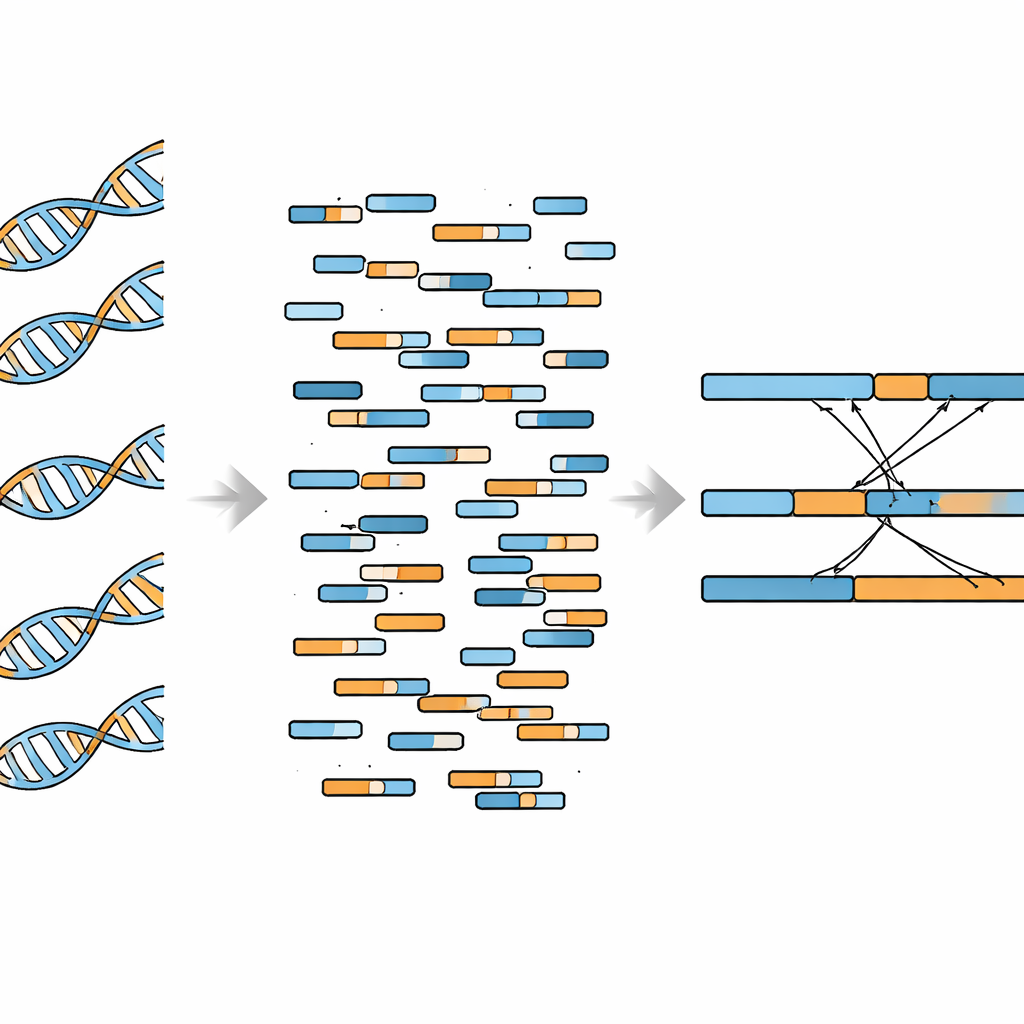
Promessa e limites práticos
Embora encorajadores, os resultados também destacam limites. Os testes foram realizados em linhagens celulares uniformes, não em amostras de pacientes reais, onde as células cancerosas estão mais misturadas e os pontos de quebra das fusões podem variar entre indivíduos. O limiar de detecção de pouco mais de 8% de DNA derivado do tumor é bem adequado para biópsias de tecido, onde as células cancerosas frequentemente predominam, mas pode ser insuficiente para testes baseados em sangue que precisam separar quantidades vestigiais de DNA tumoral. Alcançar a profundidade de sequenciamento necessária também é caro, e algumas fusões que ocorrem fora de limites gênicos conhecidos ainda serão perdidas por design.
O que isso significa para o futuro dos testes contra o câncer
Este estudo mostra que um conjunto de dados originalmente coletado para ler marcas químicas no DNA pode ser reaproveitado para detectar fusões gênicas importantes, pelo menos quando essas fusões são conhecidas antecipadamente e estão presentes em níveis razoáveis. Para pesquisadores e clínicos que já usam WGBS, isso significa que mais valor pode ser extraído de cada experimento: padrões de metilação, outras alterações genéticas e agora eventos de fusão podem ser avaliados a partir da mesma corrida. Com refinamentos adicionais, validação em amostras de pacientes e softwares mais inteligentes, o WGBS poderia se tornar um ensaio central que forneça múltiplas camadas de insight sobre como um câncer é construído — e como tratá-lo melhor — a partir de uma única amostra preciosa.
Citação: Kim, T., Bang, D. Detection of known gene fusions in cancer cell lines using whole-genome bisulfite sequencing data. Sci Rep 16, 13254 (2026). https://doi.org/10.1038/s41598-026-40803-0
Palavras-chave: fusão gênica, metilação do DNA, sequenciamento bisulfito de genoma inteiro, genômica do câncer, biópsia líquida