Clear Sky Science · nl
Detectie van bekende genfusies in kankercellijnen met behulp van whole-genome bisulfietsequencinggegevens
Waarom één test die meer kan belangrijk is
Kankerartsen willen steeds vaker veel informatie uit één DNA‑monster halen: welke genen aan of uit staan, hoe het DNA is gevouwen of gekopieerd, en of belangrijke genen op schadelijke wijze aan elkaar zijn geplakt. Vandaag vereisen die vragen meestal meerdere laboratoriumtests, die elk kostbaar materiaal verbruiken en extra kosten met zich meebrengen. Deze studie onderzoekt of één veelgebruikte test voor chemische labels op DNA, namelijk whole‑genome bisulfietsequencing, ook genfusies kan onthullen — de abnormale samensmelting van twee genen die vaak kanker aandrijven en de behandelingskeuze beïnvloeden.
Vreemde genmixen in kanker
Genfusies ontstaan wanneer chromosomen breken en op de verkeerde plaats weer aan elkaar worden gekoppeld, waardoor stukken van twee verschillende genen worden samengevoegd. Deze mixen kunnen groeisignalen versterken, beschermende genen stilleggen of hybride eiwitten maken die cellen naar kanker duwen. Bekende voorbeelden zijn de BCR–ABL1‑fusie bij chronische myeloïde leukemie en fusies in prostaat‑ en longkanker die bepalen welke geneesmiddelen effectief zijn. Vanwege hun klinische relevantie zoeken laboratoria doorgaans naar fusies met tests die specifiek op RNA gericht zijn of door het hele genoom te scannen, en niet met methoden die bedoeld zijn om chemische merktekens op DNA te lezen.
Een krachtige maar onderbenutte gegevensbron
Whole‑genome bisulfietsequencing (WGBS) is ontwikkeld om DNA‑"methylering" in kaart te brengen — kleine chemische labels die helpen bepalen welke genen actief zijn. Het is een werkpaard geworden voor zowel fundamenteel onderzoek als liquid‑biopsytests die fragmenten van DNA in het bloed analyseren. Uit één WGBS‑run kunnen onderzoekers al informatie halen over methyleringspatronen, kopie‑aantalsveranderingen, enkellettermutaties en hoe DNA in fragmenten wordt geknipt. Detectie van fusies ontbrak echter op die lijst. De hobbel is dat de chemische behandeling in WGBS DNA in kortere stukjes breekt en veel cytosines omzet, waardoor de resulterende sequenties moeilijker nauwkeurig op het referentiegenoom kunnen worden uitgelijnd.
Fusion‑detectietools een nieuwe truc leren
De auteurs probeerden WGBS‑gegevens geschikt te maken voor fusieontdekking door software te gebruiken die de eigenaardigheden van bisulfietbehandeld DNA begrijpt en "split" reads aankan — korte sequenties die deels op het ene gen en deels op het andere gen uitlijnen. Ze concentreerden zich op bekende fusiegebeurtenissen in plaats van blind het hele genoom te doorzoeken. Eerst testten ze hun pijplijn op K562‑leukemiecellen, die de goed bestudeerde BCR–ABL1‑fusie dragen. De breukpunten die uit WGBS werden afgeleid, kwamen nauw overeen met die uit traditionele whole‑genome sequencing, en er traden dekkingdips rond de fusieplaats op in beide datatypes. Het team toonde ook aan dat WGBS de fusie betrouwbaar kon detecteren wanneer slechts ongeveer 8% van het DNA in een monster afkomstig was van fusie‑positieve cellen, met perfecte detectie zodra deze fractie 10% bereikte bij relatief diepe sequencing.
Opschalen naar meerdere fusies tegelijk
Vervolgens onderzochten de onderzoekers of hun aanpak meerdere fusies in hetzelfde monster aankon. Ze pasten het toe op MCF‑7‑borstkankercellen, die een dozijn eerder bevestigde genfusies herbergen. Hun WGBS‑gebaseerde methode herwon 10 van deze 12 fusies, variërend van herschikkingen binnen één chromosoom tot fusies tussen twee verschillende chromosomen. Aantallen ondersteunende reads waren zeer consistent over herhaalde experimenten, wat aantoont dat de methode technisch stabiel is. Tegelijk ontdekten de auteurs een belangrijke beperking: wanneer ze buiten de specifieke genregio’s keken, waren achtergrondsignalen die lijken op valse fusies veel vaker aanwezig dan echte. Dit suggereert dat WGBS het best geschikt is voor gerichte checks op bekende fusies in plaats van voor open eindige zoektochten.
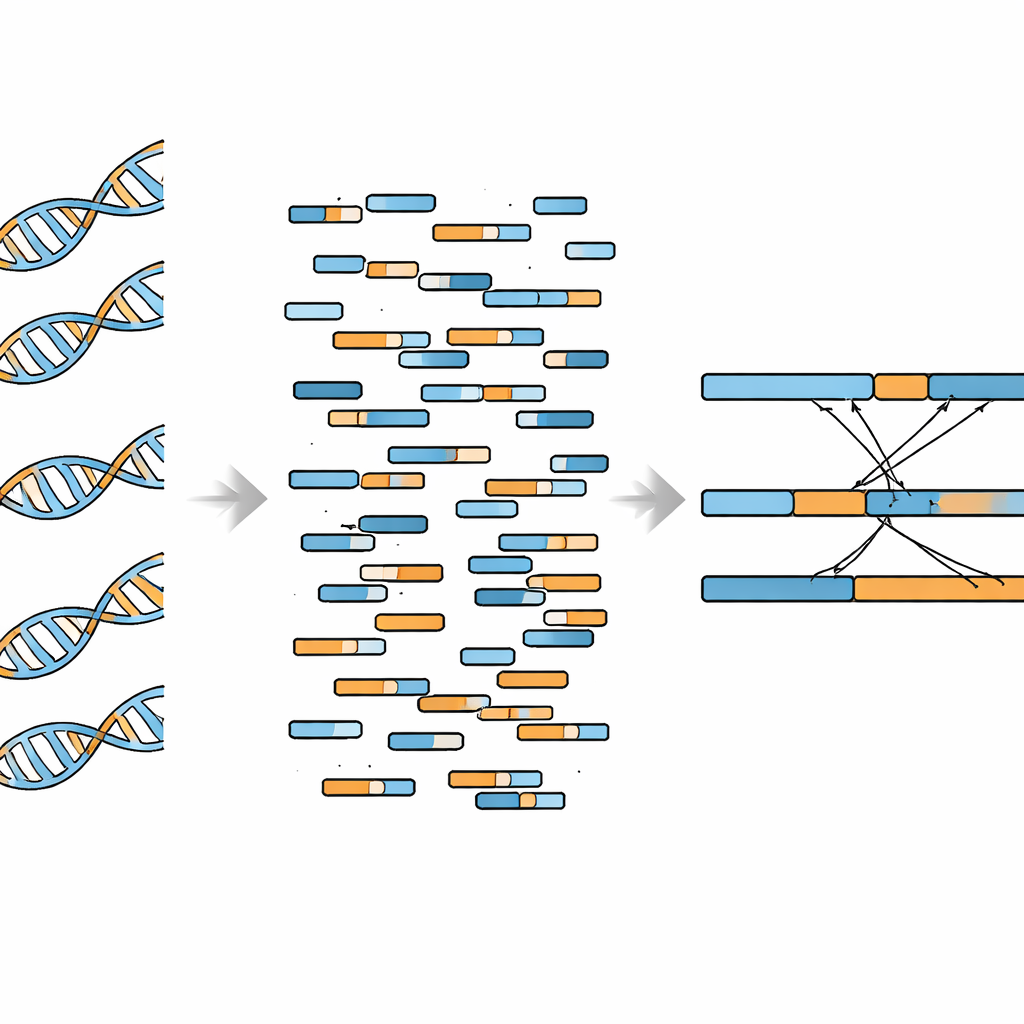
Belofte en praktische grenzen
Hoewel bemoedigend, benadrukken de resultaten ook grenzen. De tests werden uitgevoerd in uniforme cellijnen, niet in echte patiëntmonsters waar kankercellen meer gemengd zijn en fusiebreukpunten van persoon tot persoon kunnen variëren. De detectiedrempel van net boven 8% tumorafgeleid DNA is goed geschikt voor weefselbiopten, waar kankercellen vaak domineren, maar kan tekortschieten voor bloedtests die door sporenhoeveelheden tumor‑DNA moeten ziften. Het bereiken van de vereiste sequenceringsdiepte is bovendien duur, en sommige fusies die buiten bekende gengrenzen vallen, zullen door ontwerp alsnog gemist worden.
Wat dit betekent voor toekomstige kankertests
Deze studie toont aan dat een dataset die oorspronkelijk is verzameld om chemische labels op DNA te lezen, kan worden hergebruikt om belangrijke genfusies op te sporen, althans wanneer die fusies van tevoren bekend zijn en in redelijke hoeveelheden aanwezig. Voor onderzoekers en clinici die al WGBS gebruiken, betekent dit dat meer waarde uit elk experiment kan worden gehaald: methyleringspatronen, andere genetische veranderingen en nu ook fusiegebeurtenissen kunnen allemaal uit dezelfde run worden beoordeeld. Met verdere verfijning, validatie in patiëntmonsters en slimmere software zou WGBS een centraal hulpprotocol kunnen worden dat veel lagen van inzicht levert over hoe een kanker is opgebouwd — en hoe deze het beste behandeld kan worden — uit één kostbaar monster.
Bronvermelding: Kim, T., Bang, D. Detection of known gene fusions in cancer cell lines using whole-genome bisulfite sequencing data. Sci Rep 16, 13254 (2026). https://doi.org/10.1038/s41598-026-40803-0
Trefwoorden: genfusie, DNA-methylering, whole-genome bisulfietsequencing, kanker-genomica, liquid biopsy