Clear Sky Science · ru
Обнаружение известных генетических слияний в линиях раковых клеток с помощью данных бисульфитного секвенирования всего генома
Почему важен один тест, который делает больше
Онкологи всё чаще хотят получить множество сведений из одного образца ДНК: какие гены включены или выключены, как упакована и копируется ДНК, и были ли ключевые гены соединены друг с другом пагубным образом. Сегодня на эти вопросы обычно требуется несколько разных лабораторных тестов, каждый из которых расходует драгоценный материал и увеличивает затраты. В этом исследовании ставится вопрос, может ли один широко используемый тест на химические метки ДНК, называемый бисульфитным секвенированием всего генома, также выявлять слияния генов — аномальные соединения двух генов, которые часто ведут к раку и влияют на выбор лечения.
Странные генетические «мэшапы» в раке
Слияния генов возникают, когда хромосомы ломаются и неправильно переподключаются, сшивая части двух разных генов. Такие мэшапы могут усиливать сигналы роста, выключать защитные гены или создавать гибридные белки, подталкивающие клетки к онкогенному состоянию. Известные примеры включают слияние BCR–ABL1 при хроническом миелоидном лейкозе и слияния в раке предстательной железы и лёгких, определяющие, какие препараты будут эффективны. Из-за клинического значения лаборатории обычно ищут слияния с помощью тестов, нацеленных специально на РНК, или сканируя весь геном, а не методами, разработанными для чтения химических меток на ДНК.
Мощный, но недоиспользуемый источник данных
Бисульфитное секвенирование всего генома (WGBS) было разработано для картирования метилирования ДНК — небольших химических меток, которые помогают контролировать активность генов. Этот метод стал рабочей лошадкой и для фундаментальных исследований, и для тестов жидкостной биопсии, анализирующих фрагменты ДНК в кровотоке. Из одного запуска WGBS учёные уже могут получить информацию о метилировании, изменениях числа копий, одиночных нуклеотидных мутациях и о том, как ДНК расщепляется на фрагменты. Однако обнаружение слияний ранее отсутствовало в этом наборе возможностей. Препятствием является то, что химическая обработка, применяемая в WGBS, ломает ДНК на более короткие фрагменты и преобразует многие цитозины, из-за чего получившиеся последовательности сложнее точно выровнять на эталонный геном.
Обучение инструментов поиска слияний новой приспособленности
Авторы решили адаптировать данные WGBS для обнаружения слияний, использовав программное обеспечение, учитывающее особенности бисульфит-обработанной ДНК и умеющее работать с «сплит»-риды — короткими последовательностями, которые частично выравниваются на один ген, а частично — на другой. Они сосредоточились на известных событиях слияния, а не на слепом сканировании всего генома. Сначала они протестировали конвейер на клетках лейкемии K562, которые несут хорошо изученное слияние BCR–ABL1. Точки разрыва, определённые по WGBS, хорошо совпали с найденными традиционным секвенированием всего генома, а провалы покрытия вокруг места слияния наблюдались в обоих типах данных. Команда также показала, что WGBS способен обнаруживать слияние надёжно, когда около 8% ДНК в образце происходят от клеток с слиянием, с идеальным обнаружением при достижении этой доли в 10% при относительно глубоком секвенировании.
Масштабирование до множественных слияний одновременно
Далее исследователи проверили, справится ли их подход с несколькими слияниями в одном образце. Они применили его к клеткам рака молочной железы MCF-7, в которых имеется около десятка ранее подтверждённых слияний. Метод на основе WGBS восстановил 10 из этих 12 слияний, охватывая как реаранжировки внутри одной хромосомы, так и события между разными хромосомами. Число ридов в поддержку слияний было высоко согласовано между повторными экспериментами, что показывает техническую стабильность метода. Вместе с тем авторы выявили ключевое ограничение: при проверке вне конкретных интересующих генных регионов фоновые сигналы, напоминающие ложные слияния, были гораздо более частыми, чем истинные. Это указывает на то, что WGBS лучше подходит для целевых проверок известных слияний, а не для открытого поиска без заданных ориентиров.
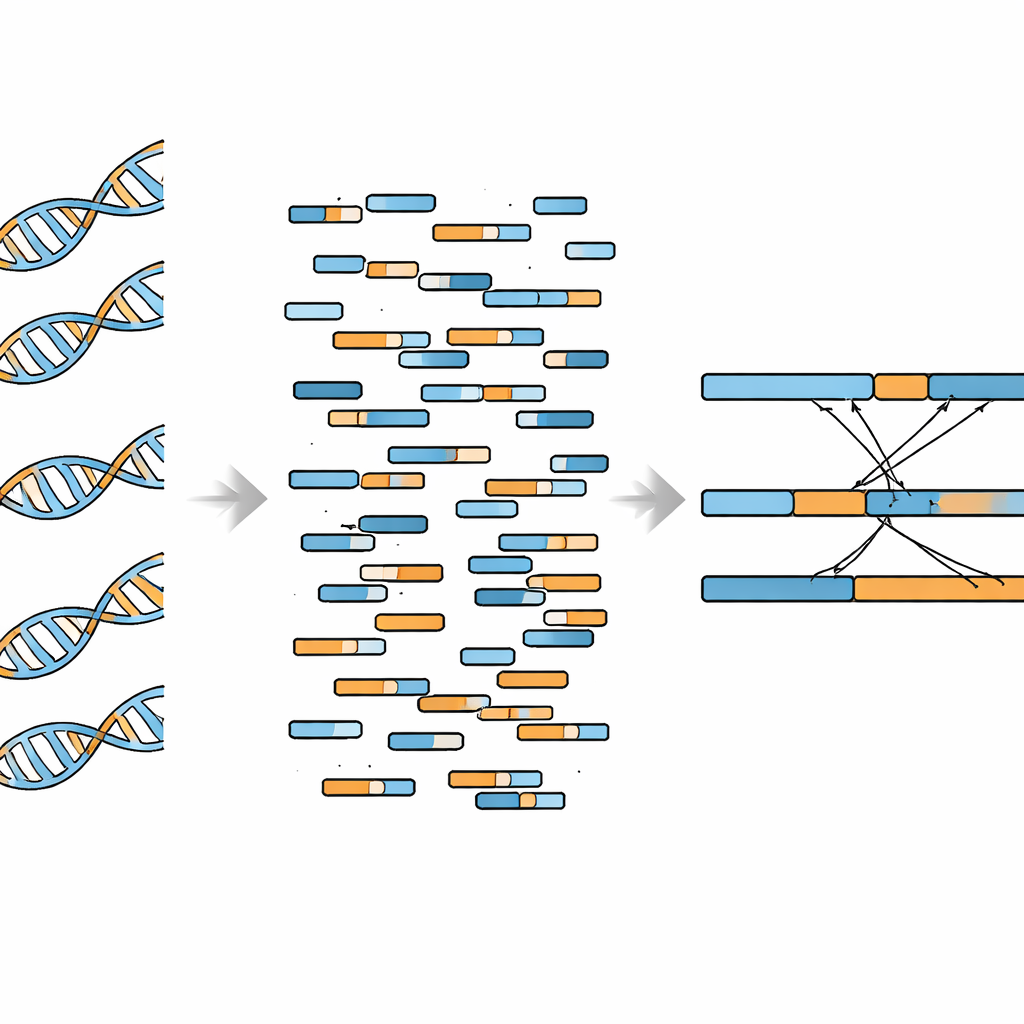
Перспективы и практические ограничения
Хотя результаты обнадёживают, они также подчёркивают границы подхода. Тесты выполнялись на однородных клеточных линиях, а не на реальных образцах пациентов, где раковые клетки более смешаны, и точки разрыва слияний могут варьировать между людьми. Порог обнаружения чуть выше 8% ДНК опухолевого происхождения хорошо подходит для тканевых биопсий, где клетки опухоли часто доминируют, но может оказаться недостаточным для анализов крови, которым приходится искать следовые количества опухолевой ДНК. Достижение требуемой глубины секвенирования также дорого, и некоторые слияния, выходящие за пределы известных генных границ, по замыслу останутся невыявленными.
Что это значит для будущих онкотестов
Это исследование демонстрирует, что набор данных, изначально собранный для чтения химических меток на ДНК, можно перепрофилировать для выявления важных генетических слияний, по крайней мере когда эти слияния известны заранее и присутствуют на допустимом уровне. Для исследователей и клиницистов, уже использующих WGBS, это означает, что из каждого эксперимента можно извлечь больше пользы: паттерны метилирования, другие генетические изменения и теперь события слияний можно оценивать в рамках одного запуска. При дальнейшей доработке, валидации на образцах пациентов и улучшении программного обеспечения WGBS может стать центральным универсальным тестом, дающим многослойные представления о структуре опухоли — и о том, как её лучше лечить — из одного ценного образца.
Цитирование: Kim, T., Bang, D. Detection of known gene fusions in cancer cell lines using whole-genome bisulfite sequencing data. Sci Rep 16, 13254 (2026). https://doi.org/10.1038/s41598-026-40803-0
Ключевые слова: слияние генов, метилирование ДНК, бисульфитное секвенирование всего генома, онкогеномика, жидкостная биопсия