Clear Sky Science · zh
5-甲基噻唑基席夫碱及其金属螯合物的结构阐明及其抗菌与抗肿瘤活性评价
为何微小的金属连接分子重要
抗生素耐药性和癌症是现代医学面临的两大挑战。化学家正在寻找能够进入细胞、与生物靶标结合并以更少副作用抑制有害微生物或肿瘤生长的小而智能的分子。本研究探索了一类由含硫和含氮环(称为噻唑)构建、并通过引入金属离子强化的此类分子。研究者展示了经过精心设计的金属—有机颗粒如何成为对抗细菌、真菌和癌细胞的有效武器,同时借助先进的计算方法理解它们的作用机制。
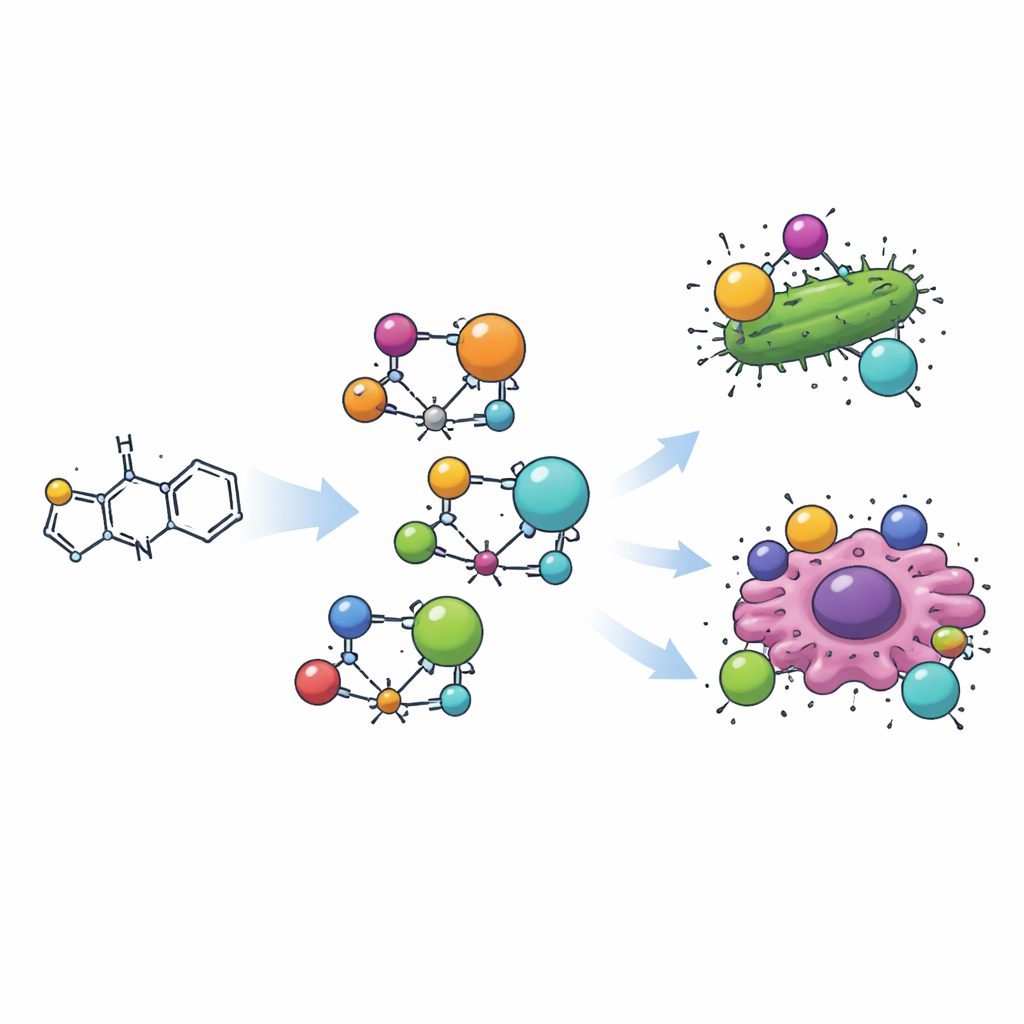
构建一种可用于药物的全新分子
研究小组首先通过经典的“席夫碱”反应,将噻唑环与一个小的芳香(环状)片段连接,合成了一个有机分子。该新分子称为 H2L,随后与四种不同的金属离子——锰、铜、锆和镉——配位,形成四种不同的金属—有机配合物。每种配合物中,基于噻唑的配体通过一个氮原子和邻近的一个氧原子抓握金属,像爪子一样包裹金属。通过对颜色、磁性和光吸收的精确测量,揭示了这些金属采用不同的三维构型:锰和镉形成四面体结构,铜形成平面方形单元,而锆则处于八面体排列。
从原子到纳米颗粒看结构
为了确认这些配合物的构建方式,研究者结合了多种表征手段。红外光谱和核磁共振谱显示,当金属与配体结合时配体中某些键发生位移,证明了碳—氮双键及邻近的氧原子参与了对金属的抓握。质谱证实了预期的分子量,而热学测试表明配合物在分解时何时释放水和有机框架的部分。X 射线衍射和透射电子显微镜表明所得材料具有晶体或近晶体结构,且关键是尺寸达到纳米级。颗粒尺寸大致在 7 到 34 纳米之间,小到比块体材料更容易穿过生物屏障。
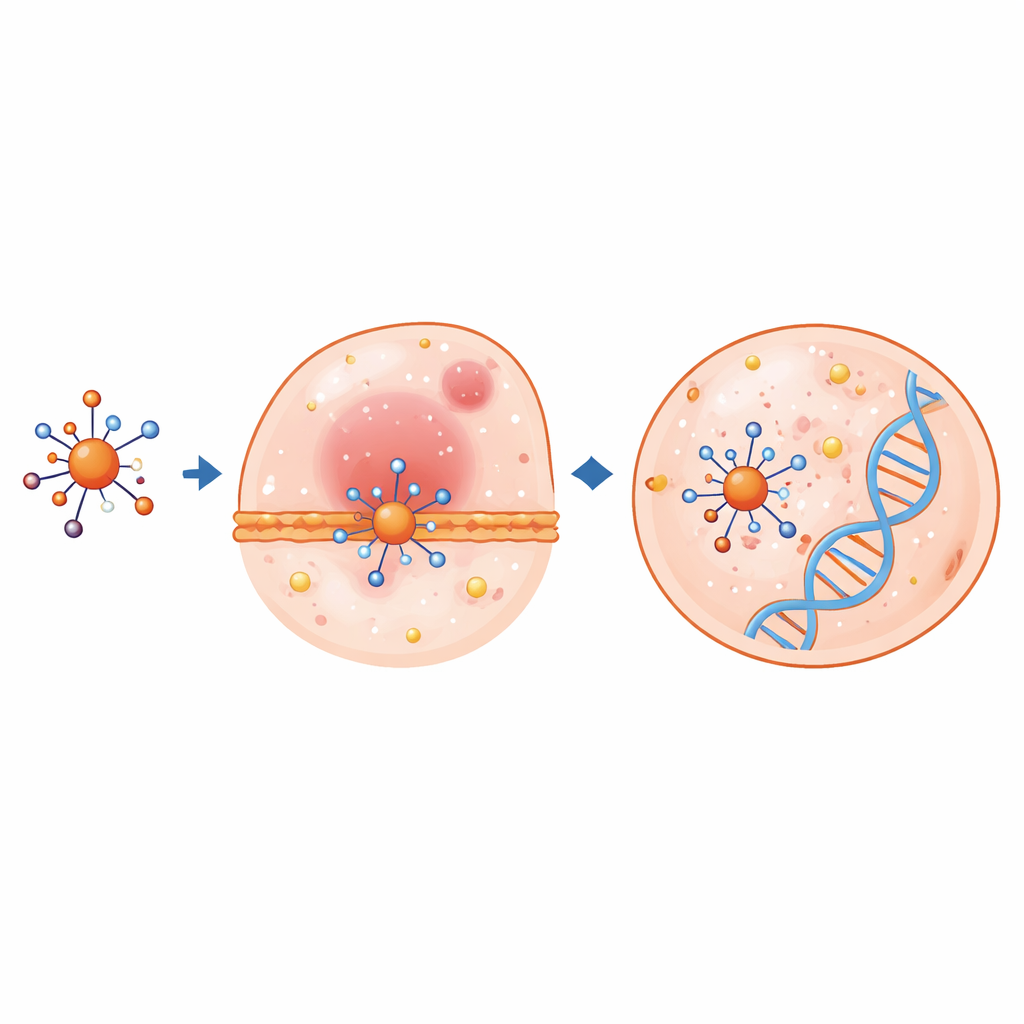
计算机揭示电子与细胞的响应
先进的量子化学计算帮助解释了这些配合物在体内可能的行为。研究者使用密度泛函理论优化原子结构,并考察了最高占据分子轨道与最低未占轨道,这些轨道表明电子移动或共享的难易程度。当配体与金属结合时,关键键长和键角发生变化,且占据轨道与空轨道之间的能隙常常减小——这意味着化学反应性提高。尤其是铜配合物表现出非常小的能隙和强烈的受电子倾向,这些特性通常与显著的生物活性相关。静电势图则突出显示了分子上最可能与蛋白质或 DNA 带电部分相互作用的区域。
对抗病原体并攻击肿瘤细胞
真正的考验来自生物学实验。游离配体及其四种金属配合物使用标准平板法对常见细菌和真菌进行了挑战测试。所有样品均显示出显著的抗菌活性,且在许多情况下这些金属配合物的表现优于已知药物如庆大霉素和两性霉素 B。例如,部分配合物对革兰氏阳性和革兰氏阴性细菌以及问题性真菌如白色念珠菌产生了更大的抑菌圈。研究者还在人体肝癌(HepG‑2)和乳腺癌(MCF‑7)细胞系上测试了这些化合物。在这些测试中,金属配位同样显著增强了活性。铜配合物对乳腺癌细胞尤其有效,其抑制生长所需浓度低于常用化疗药 5‑氟尿嘧啶。计算机对接研究支持了这些发现,显示配体与配合物能够紧密嵌入癌症相关蛋白和 DNA 螺旋的口袋中,形成稳定相互作用,从而可能干扰其正常功能。
这项工作对未来治疗的意义
对非专业读者而言,主要信息是:在原子层面的小幅设计改变——加入金属中心、调节形状和重新分配电子——可以将一个平庸的有机分子转变为具有强大、靶向生物活性的纳米级配合物。本研究表明,基于噻唑的席夫碱配体与诸如铜等金属配对时,在实验室测试中可与甚至超越常规药物在抗微生物和抗肿瘤活性上的表现。尽管要将这些配合物发展为药物还需大量工作,但实验测量与计算建模的结合为开发下一代既高效又选择性的金属—有机疗法提供了路线图。
引用: Wahdan, K.M., Mandour, H.S.A., El-Ghamry, H.A. et al. Structure elucidation and evaluation of the antimicrobial and antitumor activities of 5-methylthiazole-based Schiff base and its metal chelates. Sci Rep 16, 10738 (2026). https://doi.org/10.1038/s41598-026-40320-0
关键词: 噻唑金属配合物, 纳米颗粒抗癌剂, 席夫碱配体, 抗菌配位化合物, 分子对接药物设计