Clear Sky Science · de
Strukturaufklärung und Bewertung der antimikrobiellen und antitumoralen Aktivitäten einer 5‑Methylthiazol‑basierten Schiff‑Base und ihrer Metallchelate
Warum winzige, metallverknüpfte Moleküle wichtig sind
Antibiotikaresistenzen und Krebs gehören zu den größten Herausforderungen der modernen Medizin. Chemiker suchen nach kleinen, gezielt wirkenden Molekülen, die in Zellen eindringen, an biologische Ziele binden und schädliche Mikroben oder Tumorwachstum mit weniger Nebenwirkungen ausschalten können. Diese Studie untersucht eine Familie solcher Moleküle, die auf einem schwefel‑ und stickstoffhaltigen Ring namens Thiazol basieren und durch Bindung von Metallionen verstärkt werden. Die Forscher zeigen, wie sorgfältig gestaltete metall‑organische Partikel zu wirksamen Gegnern von Bakterien, Pilzen und Krebszellen werden können, und verwenden gleichzeitig moderne Rechnungen, um zu verstehen, warum sie wirken.
Aufbau eines neuen, medizintauglichen Moleküls
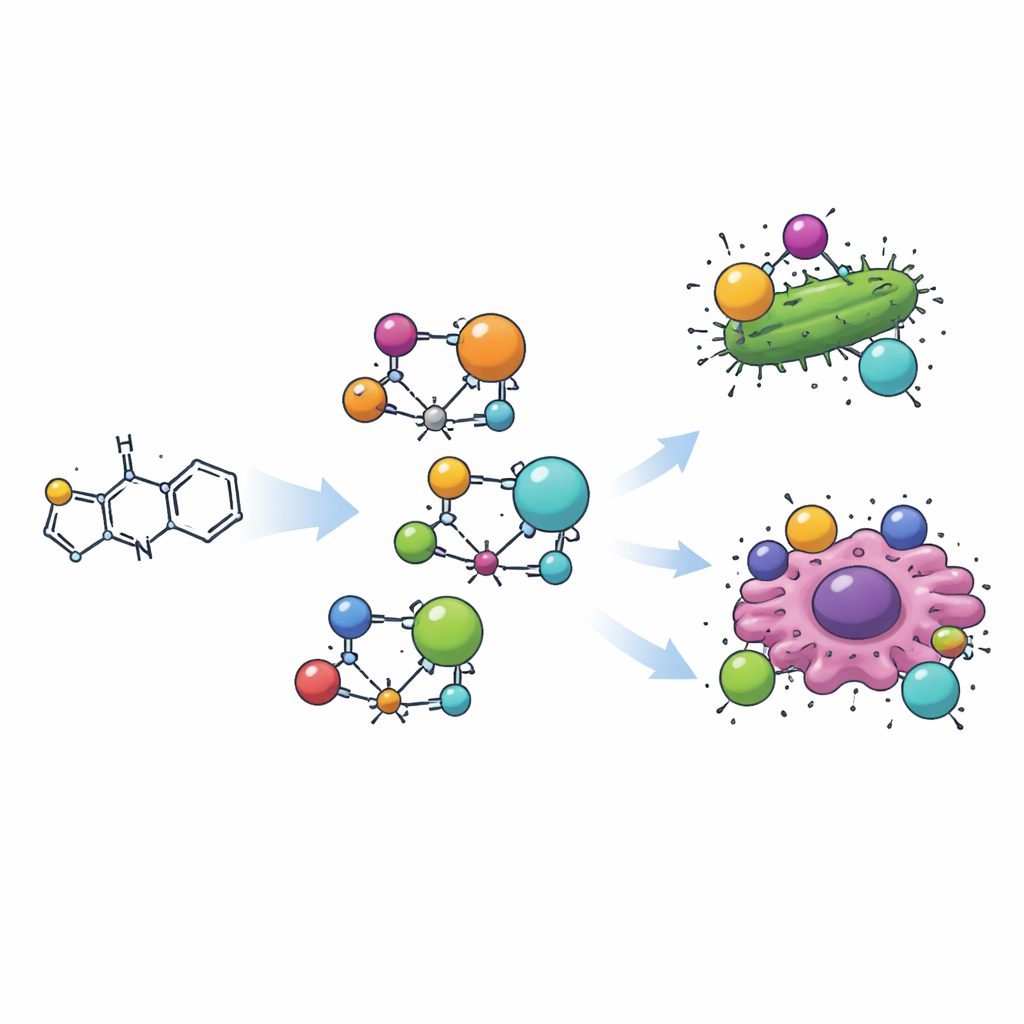
Das Team stellte zunächst ein organisches Molekül her, indem es einen Thiazolring mit einem kleinen aromatischen (ringförmigen) Fragment durch eine klassische „Schiff‑Base“-Reaktion verband. Dieses neue Molekül, H2L genannt, wurde anschließend mit vier verschiedenen Metallionen — Mangan, Kupfer, Zirkonium und Cadmium — kombiniert, um vier unterschiedliche metall‑organische Komplexe zu bilden. Jeder Komplex lässt den thiazolbasierten Liganden das Metall über ein Stickstoffatom und ein benachbartes Sauerstoffatom greifen und umschließt es wie eine Klaue. Messungen von Farbe, Magnetismus und Lichtabsorption zeigten, dass die Metalle unterschiedliche dreidimensionale Geometrien annehmen: Mangan und Cadmium bilden tetraedrische (vier‑eckige) Strukturen, Kupfer bildet eine flache quadratisch‑planare Einheit, und Zirkonium liegt in einer oktaedrischen (sechs‑eckigen) Anordnung vor.
Struktur erkennen — von Atomen bis zu Nanopartikeln
Um zu bestätigen, wie diese Komplexe aufgebaut sind, kombinierten die Forscher viele Methoden. Infrarot‑ und Kernspinresonanzspektren zeigten, dass bestimmte Bindungen im Liganden sich verschieben, wenn das Metall gebunden ist, was beweist, dass die Stickstoff‑Kohlenstoff‑Doppelbindung und ein benachbartes Sauerstoffatom am Metallgriff beteiligt sind. Massenspektrometrie bestätigte die erwarteten Molekulargewichte, während thermische Tests zeigten, wann Wasser und Teile des organischen Gerüsts beim Zerfall der Komplexe freigesetzt werden. Röntgenbeugung und Transmissionselektronenmikroskopie demonstrierten, dass die resultierenden Materialien kristallin oder nahezu kristallin sind und — entscheidend — Nanometer‑groß. Die Partikelgrößen lagen ungefähr zwischen 7 und 34 Nanometern, klein genug, um biologische Barrieren leichter passieren zu können als makroskopische Materialien.
Computer zeigen, wie Elektronen und Zellen reagieren
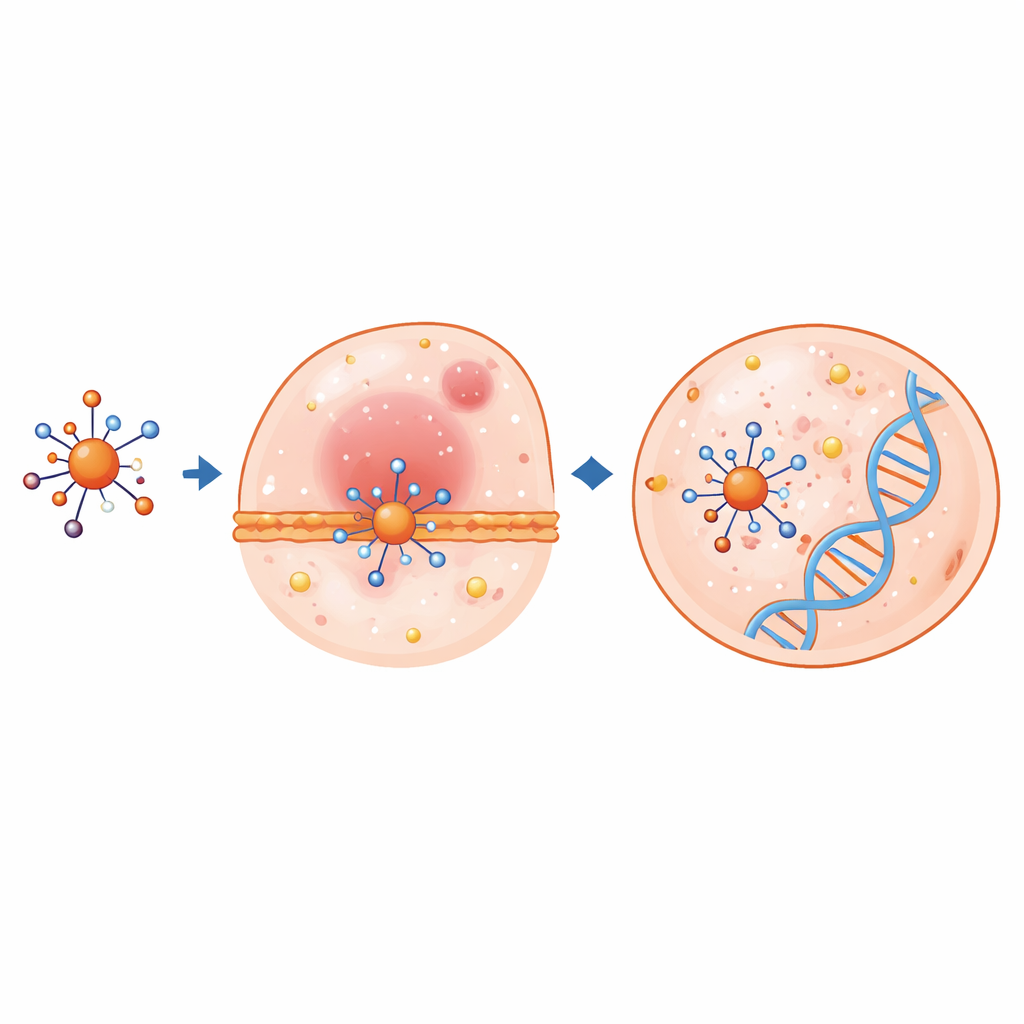
Fortgeschrittene quantenchemische Berechnungen halfen zu erklären, wie sich diese Komplexe im Körper verhalten könnten. Mit Hilfe der Dichtefunktionaltheorie optimierten die Wissenschaftler die atomaren Strukturen und untersuchten das höchstbesetzte und das niedrigstunbesetzte Molekülorbital, die anzeigen, wie leicht Elektronen sich bewegen oder geteilt werden können. Wenn der Ligand Metalle bindet, ändern sich wichtige Bindungslängen und -winkel, und die Energielücke zwischen besetzten und unbesetzten Orbitalen verkleinert sich oft — ein Hinweis auf erhöhte chemische Reaktivität. Der Kupferkomplex zeigt besonders eine sehr kleine Lücke und eine starke Neigung, Elektronen aufzunehmen, Eigenschaften, die häufig mit starken biologischen Effekten korrelieren. Karten des elektrostatischen Potentials heben Regionen der Moleküle hervor, die am wahrscheinlichsten mit geladenen Bereichen von Proteinen oder DNA interagieren.
Gegen Keime kämpfen und Tumorzellen angreifen
Die biologische Prüfung war der eigentliche Test. Der freie Ligand und seine vier Metallkomplexe wurden mittels Standard‑Plattentests gegen häufige Bakterien und Pilze geprüft. Alle zeigten bemerkenswerte antimikrobielle Aktivität, und in vielen Fällen übertrafen die Metallkomplexe etablierte Wirkstoffe wie Gentamicin und Amphotericin B. Beispielsweise erzeugten einige Komplexe größere Hemmhofe gegen sowohl grampositive als auch gramnegative Bakterien sowie gegen problematische Pilze wie Candida albicans. Die Verbindungen wurden auch gegen humane Leberkrebs‑ (HepG‑2) und Brustkrebs‑(MCF‑7) Zelllinien getestet. Auch hier steigerte die Metallbindung die Wirksamkeit deutlich. Der Kupferkomplex war besonders beeindruckend gegen Brustkrebszellen und hemmte das Wachstum bei niedrigeren Konzentrationen als das häufig verwendete Chemotherapeutikum 5‑Fluorouracil. Computersimuliertes Docking untermauerte diese Ergebnisse und zeigte, dass der Ligand und die Komplexe gut in Taschen krebsrelevanter Proteine und DNA‑Helices passen können und stabilisierende Wechselwirkungen bilden, die die normale Funktion stören könnten.
Was diese Arbeit für zukünftige Behandlungen bedeutet
Für Nicht‑Fachleute lautet die Kernbotschaft, dass kleine Designänderungen auf Atomniveau — das Hinzufügen eines Metallzentrums, die Formanpassung und die Umverteilung von Elektronen — ein bescheidenes organisches Molekül in einen nanometergroßen Komplex mit starker, zielgerichteter biologischer Aktivität verwandeln können. Die Studie zeigt, dass thiazolbasierte Schiff‑Basen, kombiniert mit Metallen wie Kupfer, in Labortests gegen Mikroben und Krebszellen mit Standardwirkstoffen konkurrieren oder diese sogar übertreffen können. Obwohl noch viel Arbeit nötig ist, bevor einer dieser Komplexe zu einem Arzneimittel wird, bietet die Kombination aus experimentellen Messungen und computergestützter Modellierung eine Roadmap zur Entwicklung einer nächsten Generation von metall‑organischen Therapien, die sowohl wirkstark als auch selektiv sind.
Zitation: Wahdan, K.M., Mandour, H.S.A., El-Ghamry, H.A. et al. Structure elucidation and evaluation of the antimicrobial and antitumor activities of 5-methylthiazole-based Schiff base and its metal chelates. Sci Rep 16, 10738 (2026). https://doi.org/10.1038/s41598-026-40320-0
Schlüsselwörter: Thiazol‑Metallkomplexe, Nanopartikel als Antikrebsmittel, Schiff‑Basen‑Liganden, antimikrobielle Koordinationsverbindungen, molekulares Docking Wirkstoffdesign