Clear Sky Science · pt
Elucidação da estrutura e avaliação das atividades antimicrobianas e antitumorais de uma base de Schiff à base de 5‑metiltiazol e seus quelatos metálicos
Por que moléculas pequenas ligadas a metais importam
A resistência a antibióticos e o câncer são dois dos maiores desafios da medicina moderna. Químicos procuram moléculas pequenas e inteligentes que possam penetrar em células, se ligar a alvos biológicos e desativar microrganismos nocivos ou o crescimento tumoral com menos efeitos colaterais. Este estudo explora uma família de tais moléculas construída a partir de um anel contendo enxofre e nitrogênio chamado tiazol, e depois reforçada pela ligação a íons metálicos. Os pesquisadores mostram como partículas metal–orgânicas cuidadosamente projetadas podem se tornar combatentes poderosos contra bactérias, fungos e células cancerígenas, ao mesmo tempo em que usam cálculos avançados para entender por que funcionam.
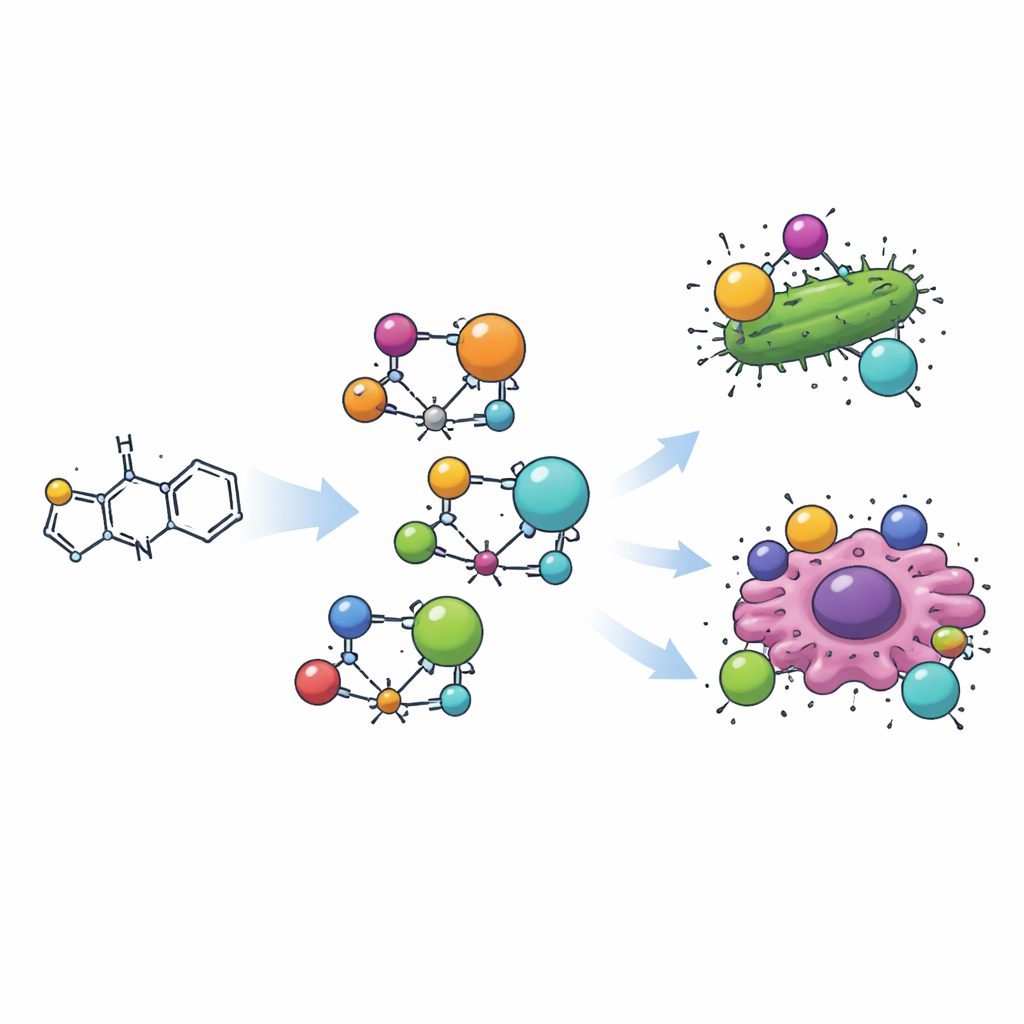
Construindo uma nova molécula pronta para uso medicinal
A equipe primeiro criou uma molécula orgânica ao unir um anel de tiazol a um pequeno fragmento aromático (em forma de anel) usando uma reação clássica de "base de Schiff". Essa nova molécula, chamada H2L, foi então combinada com quatro íons metálicos diferentes — manganês, cobre, zircônio e cádmio — para formar quatro complexos metal–orgânicos distintos. Cada complexo tem o ligante à base de tiazol prendendo o metal através de um átomo de nitrogênio e de um oxigênio próximo, envolvendo o metal como uma garra. Medições cuidadosas de cor, magnetismo e absorção de luz revelaram que os metais adotam formas tridimensionais diferentes: manganês e cádmio formam estruturas tetraédricas (quatro vértices), cobre forma uma unidade plana quadrada e zircônio ocupa uma organização octaédrica (seis vértices).
Vendo a estrutura desde os átomos até as nanopartículas
Para confirmar como esses complexos são construídos, os pesquisadores combinaram várias técnicas. Espectros de infravermelho e ressonância magnética nuclear mostraram que ligações específicas no ligante se deslocam quando o metal está ligado, provando que a dupla ligação nitrogênio–carbono e um oxigênio próximo estão envolvidos na fixação do metal. Espectrometria de massa confirmou os pesos moleculares esperados, enquanto testes térmicos revelaram quando água e partes da estrutura orgânica são liberadas à medida que os complexos se decompõem. Difração de raios X e microscopia eletrônica de transmissão demonstraram que os materiais resultantes são cristalinos ou quase cristalinos e — crucialmente — de tamanho nanométrico. Os tamanhos das partículas variaram aproximadamente de 7 a 34 nanômetros, pequenos o suficiente para atravessar barreiras biológicas mais facilmente do que materiais em grande escala.
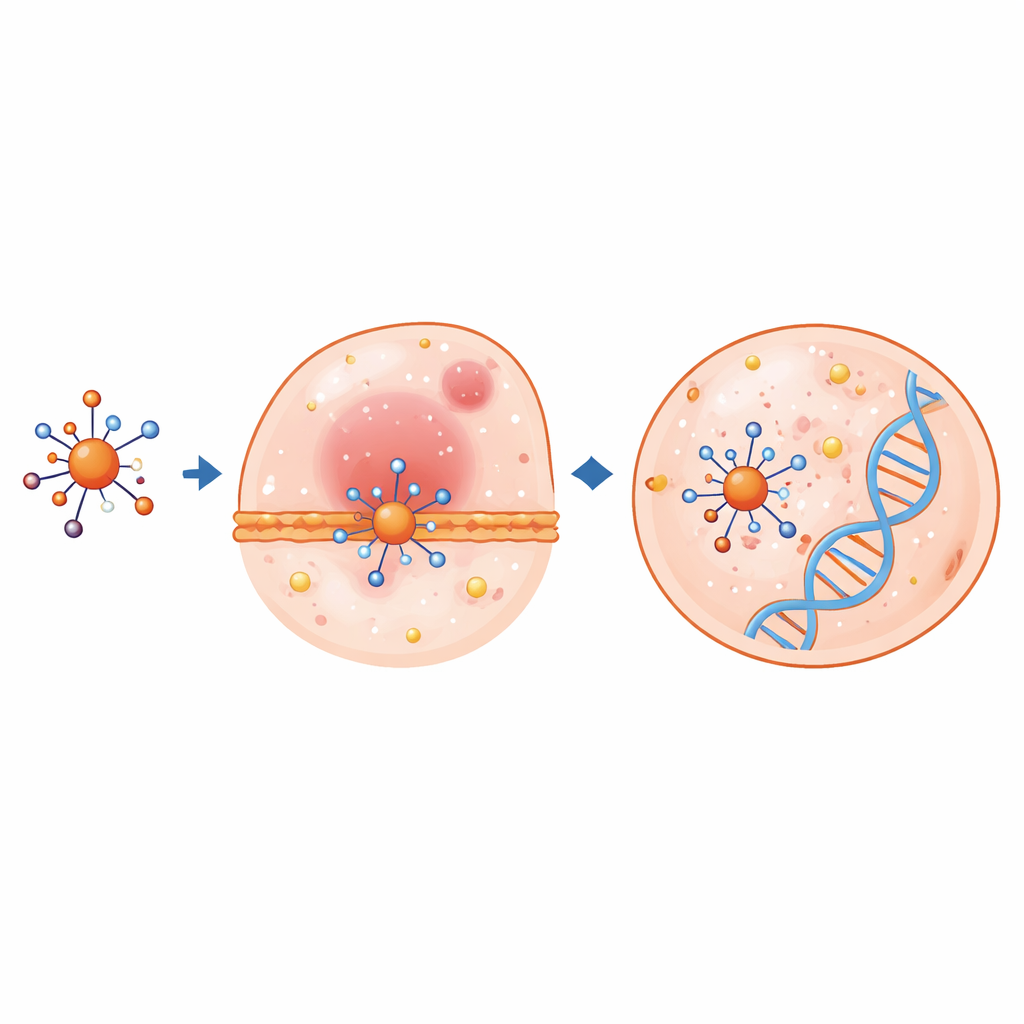
Computadores revelam como elétrons e células respondem
Cálculos quânticos avançados ajudaram a explicar como esses complexos podem se comportar dentro do corpo. Usando teoria do funcional da densidade, os cientistas otimizaram as estruturas atômicas e examinaram os orbitais moleculares mais ocupados e menos ocupados, que indicam com que facilidade os elétrons podem se mover ou ser compartilhados. Quando o ligante se liga aos metais, comprimentos e ângulos de ligação chave mudam, e a lacuna de energia entre orbitais ocupados e vazios frequentemente encolhe — sinalizando maior reatividade química. O complexo de cobre em particular mostra uma lacuna muito pequena e forte tendência a aceitar elétrons, características que frequentemente se correlacionam com efeitos biológicos intensos. Mapas de potencial eletrostático destacaram regiões nas moléculas mais propensas a interagir com partes carregadas de proteínas ou hélices de DNA.
Combatendo germes e atacando células tumorais
O teste real foi biológico. O ligante livre e seus quatro complexos metálicos foram desafiados contra bactérias e fungos comuns usando ensaios padrão em placas. Todos mostraram atividade antimicrobiana notável e, em muitos casos, os complexos metálicos superaram fármacos estabelecidos como gentamicina e anfotericina B. Por exemplo, alguns complexos produziram zonas de inibição maiores contra bactérias Gram‑positivas e Gram‑negativas, assim como contra fungos problemáticos como Candida albicans. Os compostos também foram testados contra linhas celulares de câncer humano do fígado (HepG‑2) e de mama (MCF‑7). Aqui também a ligação ao metal aumentou muito a potência. O complexo de cobre foi especialmente impressionante contra células de câncer de mama, inibindo o crescimento em concentrações menores do que o fármaco quimioterápico amplamente usado 5‑fluorouracil. Estudos de docking por computador apoiaram essas descobertas, mostrando que o ligante e os complexos podem encaixar-se bem em bolsões de proteínas relacionadas ao câncer e hélices de DNA, formando interações estabilizadoras que poderiam interromper a função normal.
O que este trabalho significa para tratamentos futuros
Para um não especialista, a mensagem principal é que pequenas mudanças de projeto em nível atômico — adicionar um centro metálico, ajustar a forma e redistribuir elétrons — podem transformar uma molécula orgânica modesta em um complexo em escala nanométrica com forte atividade biológica direcionada. Este estudo mostra que bases de Schiff à base de tiazol, quando combinadas com metais como o cobre, podem rivalizar ou até superar medicamentos padrão em testes de laboratório contra microrganismos e células cancerígenas. Embora seja necessário muito mais trabalho antes que qualquer um desses complexos se torne um medicamento, a combinação de medições experimentais e modelagem por computador oferece um roteiro para criar terapias metal–orgânicas de próxima geração que sejam ao mesmo tempo potentes e seletivas.
Citação: Wahdan, K.M., Mandour, H.S.A., El-Ghamry, H.A. et al. Structure elucidation and evaluation of the antimicrobial and antitumor activities of 5-methylthiazole-based Schiff base and its metal chelates. Sci Rep 16, 10738 (2026). https://doi.org/10.1038/s41598-026-40320-0
Palavras-chave: complexos metálicos de tiazol, agentes anticâncer em nanopartículas, ligantes de base de Schiff, compostos de coordenação antimicrobianos, projeto de fármacos por docking molecular