Clear Sky Science · nl
Structuurbepaling en evaluatie van de antimicrobiële en antitumorale werking van een 5‑methylthiazool‑gebaseerde Schiff‑base en haar metaalchelaten
Waarom kleine metaalgebonden moleculen ertoe doen
Antibioticaresistentie en kanker behoren tot de grootste uitdagingen in de moderne geneeskunde. Chemici zoeken naar kleine, slimme moleculen die cellen kunnen binnendringen, zich aan biologische doelwitten kunnen hechten en schadelijke microben of tumorgroei kunnen uitschakelen met minder bijwerkingen. Deze studie onderzoekt een familie van dergelijke moleculen opgebouwd uit een zwavel‑ en stikstofhoudende ring, thiazool, en vervolgens versterkt door binding van metaalionen. De onderzoekers tonen aan hoe zorgvuldig ontworpen metaal‑organische deeltjes krachtige strijders kunnen worden tegen bacteriën, schimmels en kankercellen, terwijl geavanceerde berekeningen worden gebruikt om te begrijpen waarom ze werken.
Een nieuw medicijnklaar molecuul bouwen
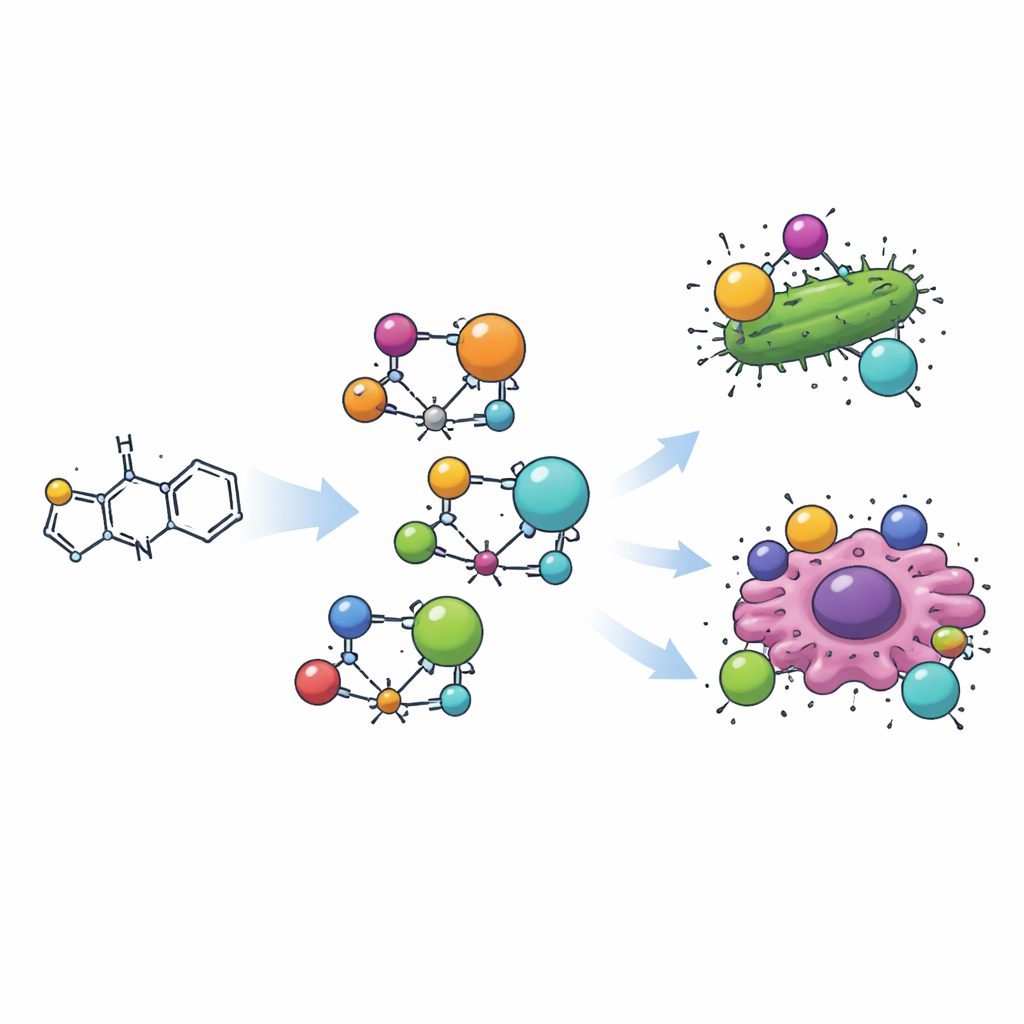
Het team maakte eerst een organisch molecuul door een thiazoolring te verbinden met een klein aromatisch (ringvormig) fragment via een klassieke "Schiff‑base" reactie. Dit nieuwe molecuul, genoemd H2L, werd vervolgens gecombineerd met vier verschillende metaalionen—mangaan, koper, zirconium en cadmium—om vier onderscheidende metaal‑organische complexen te vormen. Elk complex laat het thiazoolgebaseerde ligand het metaal grijpen via een stikstofatoom en een naburig zuurstofatoom, als een klauw om het metaal heen. Zorgvuldige metingen van kleur, magnetisme en lichtabsorptie toonden dat de metalen verschillende driedimensionale vormen aannemen: mangaan en cadmium vormen tetraëdrische (vierhoekige) structuren, koper vormt een vlak vierkant‑planair eenheid, en zirconium zit in een oktaëdrische (zeshoekige) omgeving.
Structuur zien van atomen tot nanodeeltjes
Om te bevestigen hoe deze complexen zijn opgebouwd, combineerden de onderzoekers veel verschillende technieken. Infrarood‑ en kernspinresonantiespectra toonden dat specifieke bindingen in het ligand verschuiven wanneer het metaal gebonden is, wat bewijst dat de stikstof‑koolstof dubbele binding en een nabijgelegen zuurstofatoom betrokken zijn bij het grijpen van het metaal. Massaspectrometrie bevestigde de verwachte molecuulgewichten, terwijl warmte‑gebaseerde testen aangaven wanneer water en delen van het organische raamwerk vrijkomen bij ontleding van de complexen. Röntgendiffractie en transmissie-elektronenmicroscopie toonden aan dat de resulterende materialen kristallijn of bijna kristallijn zijn en—cruciaal—nanometer‑groot. De deeltjesgroottes varieerden ruwweg van 7 tot 34 nanometer, klein genoeg om gemakkelijker door biologische barrières te bewegen dan bulkmaterialen.
Computers onthullen hoe elektronen en cellen reageren
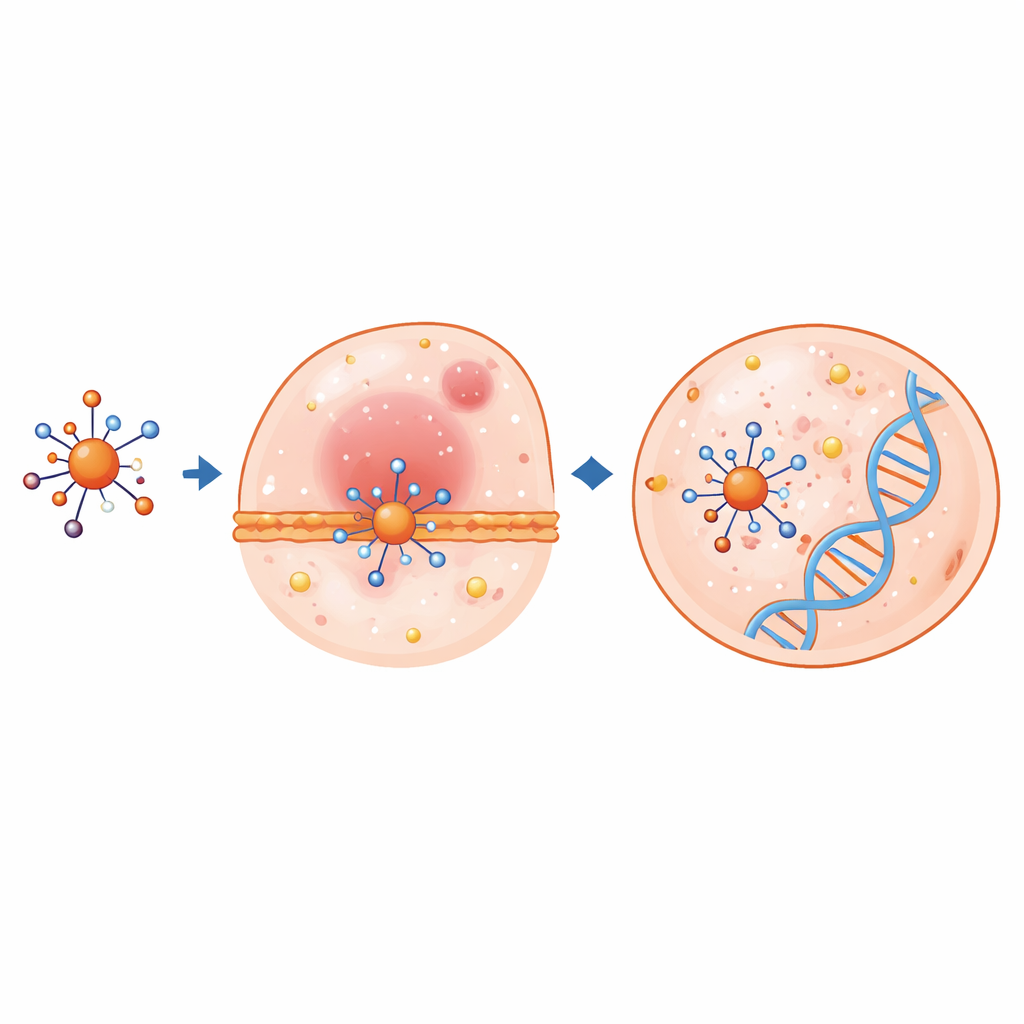
Geavanceerde kwantumchemische berekeningen hielpen verklaren hoe deze complexen zich mogelijk in het lichaam gedragen. Met behulp van dichtheidsfunctionaaltheorie optimaliseerden de wetenschappers de atomaire structuren en onderzochten ze de hoogste bezette en laagste onvervulde moleculaire orbitalen, die aangeven hoe gemakkelijk elektronen kunnen bewegen of gedeeld worden. Wanneer het ligand aan metalen bindt, veranderen belangrijke bindingslengtes en hoeken, en de energiekloof tussen bezette en lege orbitalen krimpt vaak—wat wijst op een hogere chemische reactiviteit. Het kopercomplex toont in het bijzonder een zeer kleine kloof en een sterke neiging om elektronen te accepteren, eigenschappen die vaak correleren met sterke biologische effecten. Kaarten van elektrostatisch potentiaal benadrukten regio’s op de moleculen die het meest waarschijnlijk zullen interageren met geladen delen van eiwitten of DNA.
Germen bestrijden en tumorcellen aanvallen
De echte proef was biologisch. Het vrije ligand en zijn vier metaalcomplexen werden getest tegen veelvoorkomende bacteriën en schimmels met standaard plaatassays. Alle stoffen toonden noemenswaardige antimicrobiële activiteit, en in veel gevallen presteerden de metaalcomplexen beter dan gevestigde geneesmiddelen zoals gentamicine en amphotericine B. Sommige complexen produceerden bijvoorbeeld grotere remzones tegen zowel Gram‑positieve als Gram‑negatieve bacteriën, evenals tegen problematische schimmels zoals Candida albicans. De verbindingen werden ook getest tegen menselijke leverkankercellen (HepG‑2) en borstkankercellen (MCF‑7). Ook hier verhoogde metaalbinding de werkzaamheid aanzienlijk. Het kopercomplex was bijzonder indrukwekkend tegen borstkankercellen en remde de groei bij lagere concentraties dan het veelgebruikte chemotherapiemiddel 5‑fluorouracil. Computer‑dockingstudies ondersteunden deze bevindingen door te laten zien dat het ligand en de complexen goed in zakjes van kankergarende eiwitten en DNA‑helixen passen en stabiliserende interacties vormen die de normale functie kunnen verstoren.
Wat dit werk betekent voor toekomstige behandelingen
Voor niet‑specialisten is de kernboodschap dat kleine ontwerponder wijzigingen op atomair niveau—een metaalcentrum toevoegen, de vorm afstemmen en elektronen herverdelen—een bescheiden organisch molecuul kunnen veranderen in een nanometer‑groot complex met sterke, gerichte biologische activiteit. Deze studie toont aan dat thiazool‑gebaseerde Schiff‑bases, gekoppeld aan metalen zoals koper, in laboratoriumtesten tegen microben en kankercellen kunnen concurreren met of zelfs beter kunnen zijn dan standaardmiddelen. Hoewel er nog veel werk nodig is voordat een van deze complexen medicijnen kan worden, biedt de combinatie van experimentele metingen en computermodeling een routekaart voor het creëren van next‑generation metaal‑organische therapieën die zowel krachtig als selectief zijn.
Bronvermelding: Wahdan, K.M., Mandour, H.S.A., El-Ghamry, H.A. et al. Structure elucidation and evaluation of the antimicrobial and antitumor activities of 5-methylthiazole-based Schiff base and its metal chelates. Sci Rep 16, 10738 (2026). https://doi.org/10.1038/s41598-026-40320-0
Trefwoorden: thiazool-metaalcomplexen, nanodeeltjes als anticancerogene middelen, Schiff‑base ligand, antimicrobiële coördinatieverbindingen, moleculair docken geneesmiddelenontwerp