Clear Sky Science · es
Determinación de la estructura y evaluación de las actividades antimicrobianas y antitumorales de una base de Schiff derivada de 5‑metiltiazol y sus quelatos metálicos
Por qué importan las moléculas diminutas ligadas a metales
La resistencia a los antibióticos y el cáncer son dos de los mayores desafíos de la medicina moderna. Los químicos buscan pequeñas moléculas inteligentes que puedan penetrar en las células, unirse a dianas biológicas y detener microbios dañinos o el crecimiento tumoral con menos efectos secundarios. Este estudio explora una familia de tales moléculas construidas a partir de un anillo que contiene azufre y nitrógeno llamado tiazol, y luego reforzadas mediante la incorporación de iones metálicos. Los investigadores muestran cómo partículas metal-orgánicas bien diseñadas pueden convertirse en potentes combatientes contra bacterias, hongos y células cancerosas, al tiempo que emplean cálculos avanzados para entender por qué funcionan.
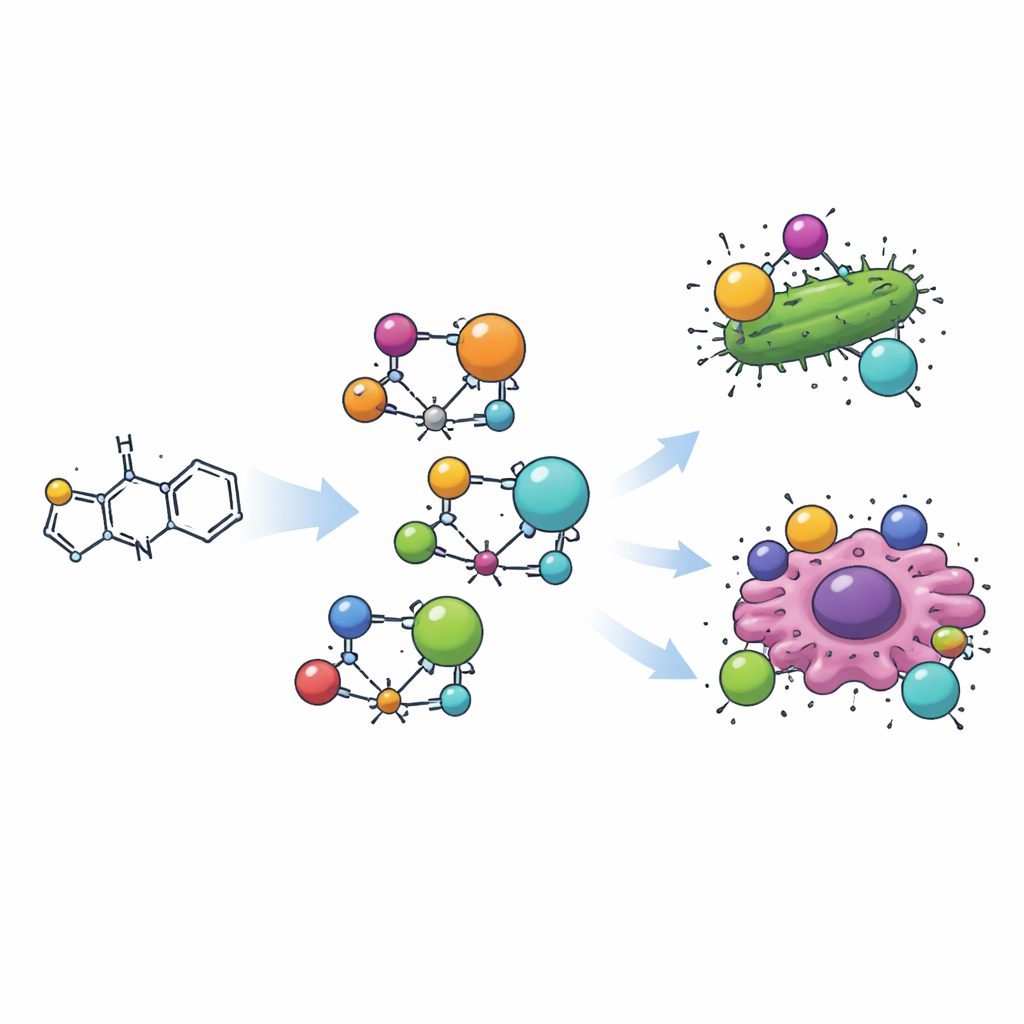
Construyendo una nueva molécula con potencial medicinal
El equipo primero creó una molécula orgánica al unir un anillo de tiazol a un pequeño fragmento aromático mediante la clásica reacción de “base de Schiff”. Esta nueva molécula, denominada H2L, se combinó luego con cuatro iones metálicos diferentes —manganeso, cobre, circonio y cadmio— para formar cuatro complejos metal-orgánicos distintos. Cada complejo presenta el ligando a base de tiazol sujetando el metal a través de un átomo de nitrógeno y un oxígeno cercano, envolviendo al metal como una garra. Mediciones cuidadosas de color, magnetismo y absorción de luz revelaron que los metales adoptan diferentes geometrías tridimensionales: manganeso y cadmio forman estructuras tetraédricas, el cobre forma una unidad cuadrado‑planar y el circonio se sitúa en una disposición octaédrica.
Ver la estructura desde los átomos hasta las nanopartículas
Para confirmar cómo se construyen estos complejos, los investigadores combinaron muchas técnicas. Espectros infrarrojos y de resonancia magnética nuclear mostraron que enlaces específicos en el ligando se desplazan cuando el metal se une, lo que prueba que el doble enlace nitrógeno‑carbono y un oxígeno cercano participan en la coordinación del metal. La espectrometría de masas confirmó los pesos moleculares esperados, mientras que ensayos térmicos revelaron cuándo se libera agua y partes del armazón orgánico a medida que los complejos se descomponen. Difracción de rayos X y microscopía electrónica de transmisión demostraron que los materiales resultantes son cristalinos o casi cristalinos y, crucialmente, de tamaño nanométrico. Los tamaños de partícula oscilaron aproximadamente entre 7 y 34 nanómetros, lo bastante pequeños para atravesar barreras biológicas más fácilmente que los materiales a granel.
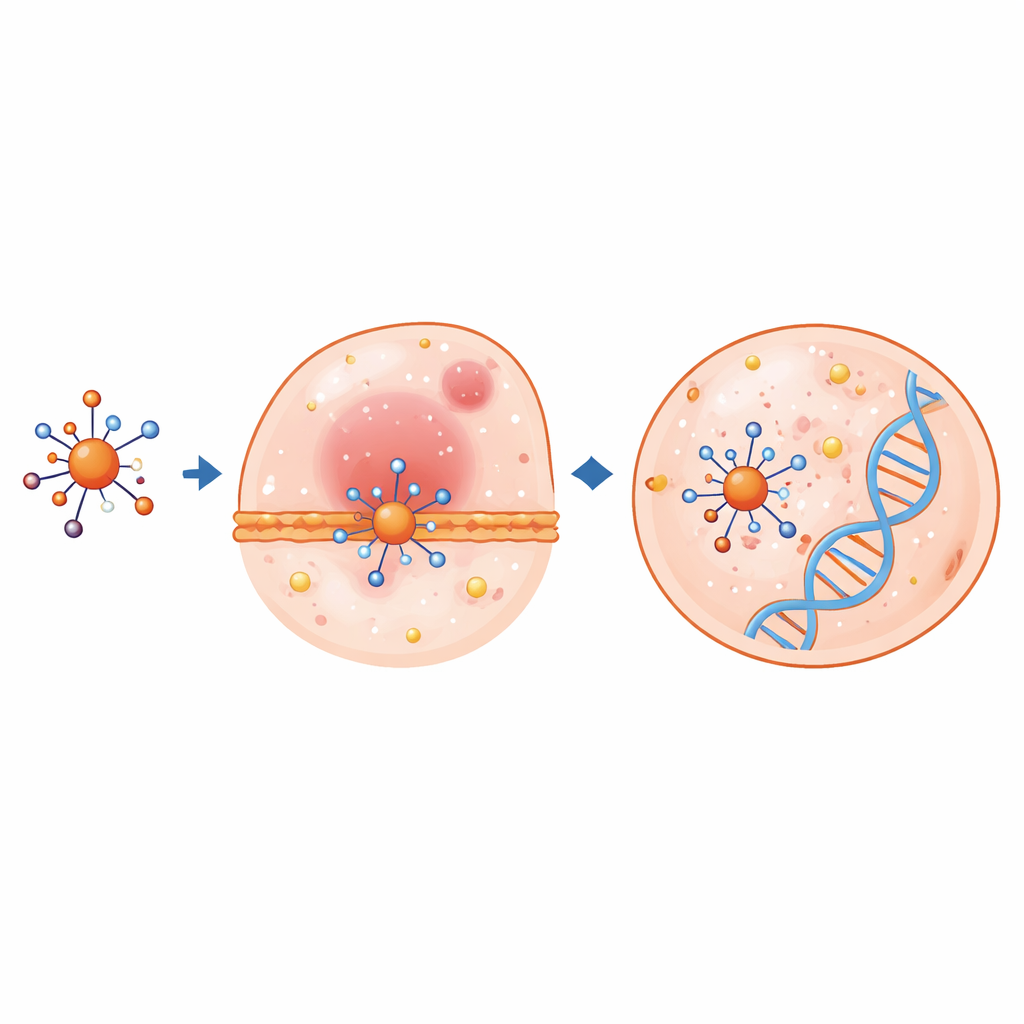
Los ordenadores revelan cómo responden los electrones y las células
Cálculos cuánticos avanzados ayudaron a explicar cómo podrían comportarse estos complejos dentro del organismo. Usando la teoría del funcional de la densidad, los científicos optimizaron las estructuras atómicas y examinaron los orbitales moleculares de mayor ocupación y menor ocupación, que indican cuán fácilmente pueden moverse o compartirse los electrones. Cuando el ligando coordina metales, cambian longitudes y ángulos de enlace clave, y la brecha energética entre orbitales ocupados y vacíos a menudo se reduce, señalando una mayor reactividad química. El complejo de cobre en particular muestra una brecha muy pequeña y una fuerte tendencia a aceptar electrones, rasgos que suelen correlacionarse con efectos biológicos potentes. Mapas de potencial electrostático destacaron las regiones de las moléculas más propensas a interactuar con partes cargadas de proteínas o del ADN.
Combatiendo gérmenes y atacando células tumorales
La prueba real fue biológica. El ligando libre y sus cuatro complejos metálicos se enfrentaron a bacterias y hongos comunes mediante ensayos estándar en placas. Todos mostraron actividad antimicrobiana notable, y en muchos casos los complejos metálicos superaron a fármacos establecidos como la gentamicina y la anfotericina B. Por ejemplo, algunos complejos produjeron zonas de inhibición mayores frente a bacterias Gram‑positivas y Gram‑negativas, así como frente a hongos problemáticos como Candida albicans. Los compuestos también se evaluaron frente a líneas celulares humanas de cáncer de hígado (HepG‑2) y de mama (MCF‑7). Aquí, de nuevo, la unión al metal incrementó mucho la potencia. El complejo de cobre fue especialmente notable contra las células de cáncer de mama, inhibiendo el crecimiento a concentraciones más bajas que el fármaco quimioterápico ampliamente usado 5‑fluorouracilo. Estudios de acoplamiento molecular apoyaron estos hallazgos, mostrando que el ligando y los complejos pueden encajar en bolsillos de proteínas relacionadas con el cáncer y hélices de ADN, formando interacciones estabilizadoras que podrían alterar su función normal.
Qué significa este trabajo para futuros tratamientos
Para un no especialista, el mensaje clave es que pequeños cambios de diseño a nivel atómico —añadir un centro metálico, ajustar la forma y redistribuir electrones— pueden convertir una molécula orgánica modesta en un complejo de escala nanométrica con una actividad biológica fuerte y dirigida. Este estudio muestra que las bases de Schiff basadas en tiazol, cuando se asocian con metales como el cobre, pueden rivalizar o incluso superar a fármacos estándar en pruebas de laboratorio contra microbios y células cancerosas. Aunque hace falta mucho más trabajo antes de que cualquiera de estos complejos se convierta en un medicamento, la combinación de mediciones experimentales y modelado por ordenador ofrece una hoja de ruta para crear terapias metal‑orgánicas de próxima generación que sean a la vez potentes y selectivas.
Cita: Wahdan, K.M., Mandour, H.S.A., El-Ghamry, H.A. et al. Structure elucidation and evaluation of the antimicrobial and antitumor activities of 5-methylthiazole-based Schiff base and its metal chelates. Sci Rep 16, 10738 (2026). https://doi.org/10.1038/s41598-026-40320-0
Palabras clave: complejos metálicos de tiazol, agentes anticancerígenos nanoparticulados, ligandos de base de Schiff, compuestos de coordinación antimicrobianos, diseño de fármacos por acoplamiento molecular