Clear Sky Science · sv
Strukturuppklarning och utvärdering av antimikrobiella och antitumöreffekter av 5-metylthiazol-baserad Schiff-bas och dess metallkomplex
Varför små metallkopplade molekyler spelar roll
Antibiotikaresistens och cancer är två av de största utmaningarna inom modern medicin. Kemister söker efter små, intelligenta molekyler som kan ta sig in i celler, fästa vid biologiska mål och hämma skadliga mikrober eller tumörtillväxt med färre biverkningar. Denna studie undersöker en familj sådana molekyler uppbyggda kring en svavel‑ och kväveinnehållande ring kallad thiazol, som sedan förstärks genom att fästa metalljoner. Forskarna visar hur noggrant designade metall‑organiska partiklar kan bli kraftfulla bekämpare av bakterier, svampar och cancerceller, samtidigt som avancerade beräkningar används för att förstå varför de fungerar.
Att bygga en ny läkemedelskandidat
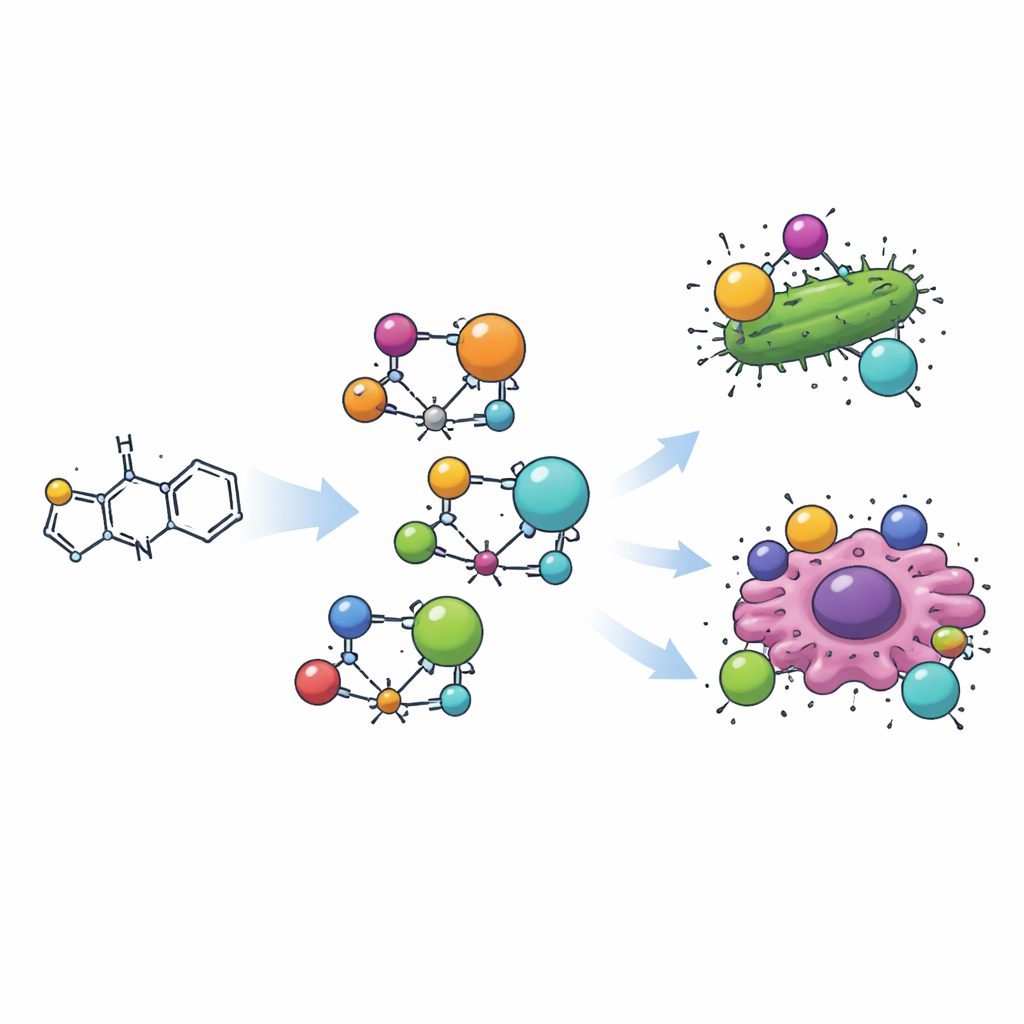
Gruppen skapade först en organisk molekyl genom att förena en thiazolring med en liten aromatisk (ringsluten) fragment via en klassisk "Schiff‑bas"‑reaktion. Denna nya molekyl, kallad H2L, kombinerades sedan med fyra olika metaljoner—mangan, koppar, zirkonium och kadmium—för att bilda fyra distinkta metall‑organiska komplex. Varje komplex har den thiazolbaserade liganden som griper tag i metallen genom en kväveatom och en närliggande syreatom, och omsluter metallen som en klo. Noggranna mätningar av färg, magnetism och ljusabsorption visade att metallerna antar olika tredimensionella former: mangan och kadmium bildar tetraedriska (fyrahörniga) strukturer, koppar bildar en plan fyrkantig enhet, och zirkonium sitter i en oktaedrisk (sexhörnig) arrangemang.
Att se struktur från atomer till nanopartiklar
För att bekräfta hur dessa komplex är uppbyggda kombinerade forskarna flera verktyg. Infraröd och kärnmagnetisk resonansspektroskopi visade att specifika bindningar i liganden förskjuts när metallen binds, vilket bevisar att kväve‑kol dubbelbindningen och en närliggande syreatom är involverade i metallbindningen. Massspektrometri bekräftade de förväntade molekylvikterna, medan termiska tester avslöjade när vatten och delar av den organiska ramen frigörs när komplexen sönderfaller. Röntgendiffraktion och transmissionselektronmikroskopi demonstrerade att de resulterande materialen är kristallina eller nästan kristallina och—avgörande—nanometerstora. Partikelstorlekarna varierade ungefär från 7 till 34 nanometer, små nog att lättare passera biologiska barriärer än bulkmaterial.
Datorer visar hur elektroner och celler reagerar
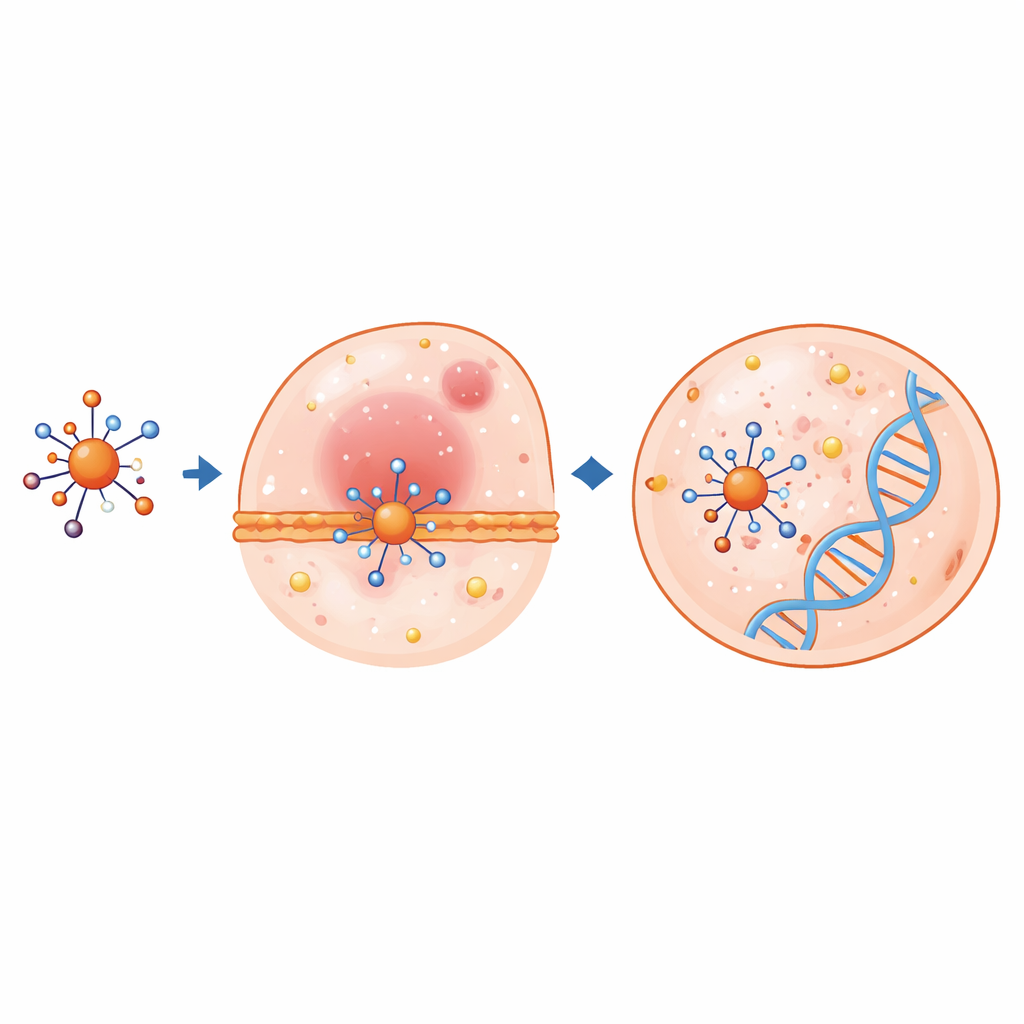
Avancerade kvantkemiska beräkningar hjälpte till att förklara hur dessa komplex kan bete sig i kroppen. Med hjälp av densitetsfunktionalteori optimerade forskarna atomstrukturerna och undersökte den högst ockuperade respektive lägst ockuperade molekylorbitalen, vilka indikerar hur lätt elektroner kan röra sig eller delas. När liganden binder metaller ändras viktiga bindningslängder och vinklar, och energi‑gapet mellan ockuperade och tomma orbitaler krymper ofta—vilket signalerar högre kemisk reaktivitet. Särskilt kopparkomplexet visar ett mycket litet gap och en stark tendens att ta upp elektroner, egenskaper som ofta korrelerar med kraftiga biologiska effekter. Kartor över elektrostatisk potential belyste områden på molekylerna som sannolikt interagerar med laddade delar av proteiner eller DNA.
Bekämpa mikrober och angripa tumörceller
Det verkliga testet var biologiskt. Den fria liganden och dess fyra metallkomplex utmanades mot vanliga bakterier och svampar med standardiserade plattmetoder. Samtliga visade märkbar antimikrobiell aktivitet, och i många fall överträffade metallkomplexen etablerade läkemedel såsom gentamicin och amphotericin B. Till exempel gav vissa komplex större hämmningszoner mot både Gram‑positiva och Gram‑negativa bakterier, liksom problematiska svampar som Candida albicans. Föreningarna testades även mot mänskliga levercancerceller (HepG‑2) och bröstcancerceller (MCF‑7). Även här ökade metallbindning avsevärt effekten. Kopparkomplexet var särskilt imponerande mot bröstcancerceller och hämmade tillväxt vid lägre koncentrationer än det mycket använda cytostatikumet 5‑fluorouracil. Datorbaserade dockningsstudier stödde dessa resultat och visade att liganden och komplexen kan passa väl in i fickor på cancerrelaterade proteiner och DNA‑spiraler, och bilda stabiliserande interaktioner som kan störa normal funktion.
Vad detta arbete betyder för framtida behandlingar
För en icke‑specialist är huvudbudskapet att små designförändringar på atomnivå—att lägga till ett metallcentrum, justera formen och omfördela elektroner—kan förvandla en blygsam organisk molekyl till ett nanometerstort komplex med stark, riktad biologisk aktivitet. Denna studie visar att thiazolbaserade Schiff‑baser, i kombination med metaller som koppar, kan mäta sig med eller till och med överträffa standardläkemedel i laboratorietester mot mikrober och cancerceller. Även om mycket mer arbete krävs innan något av dessa komplex blir läkemedel, erbjuder kombinationen av experimentella mätningar och datorbaserad modellering en färdplan för att skapa nästa generations metall‑organiska terapier som är både potenta och selektiva.
Citering: Wahdan, K.M., Mandour, H.S.A., El-Ghamry, H.A. et al. Structure elucidation and evaluation of the antimicrobial and antitumor activities of 5-methylthiazole-based Schiff base and its metal chelates. Sci Rep 16, 10738 (2026). https://doi.org/10.1038/s41598-026-40320-0
Nyckelord: thiazolmetallkomplex, nanopartikel mot cancer, Schiff-basligander, antimikrobiella koordinationsföreningar, molekylär dockning läkemedelsdesign