Clear Sky Science · pl
Ujawnienie struktury i ocena aktywności przeciwbakteryjnej i przeciwnowotworowej zasady Schiffa opartej na 5‑metylotiazolu oraz jej chelatów metali
Dlaczego małe cząsteczki związane z metalami są ważne
Oporność na antybiotyki i rak to jedne z największych wyzwań współczesnej medycyny. Chemicy poszukują małych, inteligentnych molekuł, które potrafią wnikać do komórek, wiązać się z biologicznymi celami i hamować szkodliwe mikroby lub wzrost guza przy mniejszych skutkach ubocznych. W tym badaniu zbadano rodzinę takich związków z pierścieniem zawierającym siarkę i azot — tiazolem — dodatkowo wzmocnionych poprzez związanie jonów metalu. Autorzy pokazują, jak starannie zaprojektowane cząstki metal‑organiczne mogą stać się skutecznymi środkami przeciw bakteriom, grzybom i komórkom nowotworowym, a także wykorzystują zaawansowane obliczenia, by wyjaśnić mechanizmy ich działania.
Budowanie nowej molekuły gotowej do zastosowań medycznych
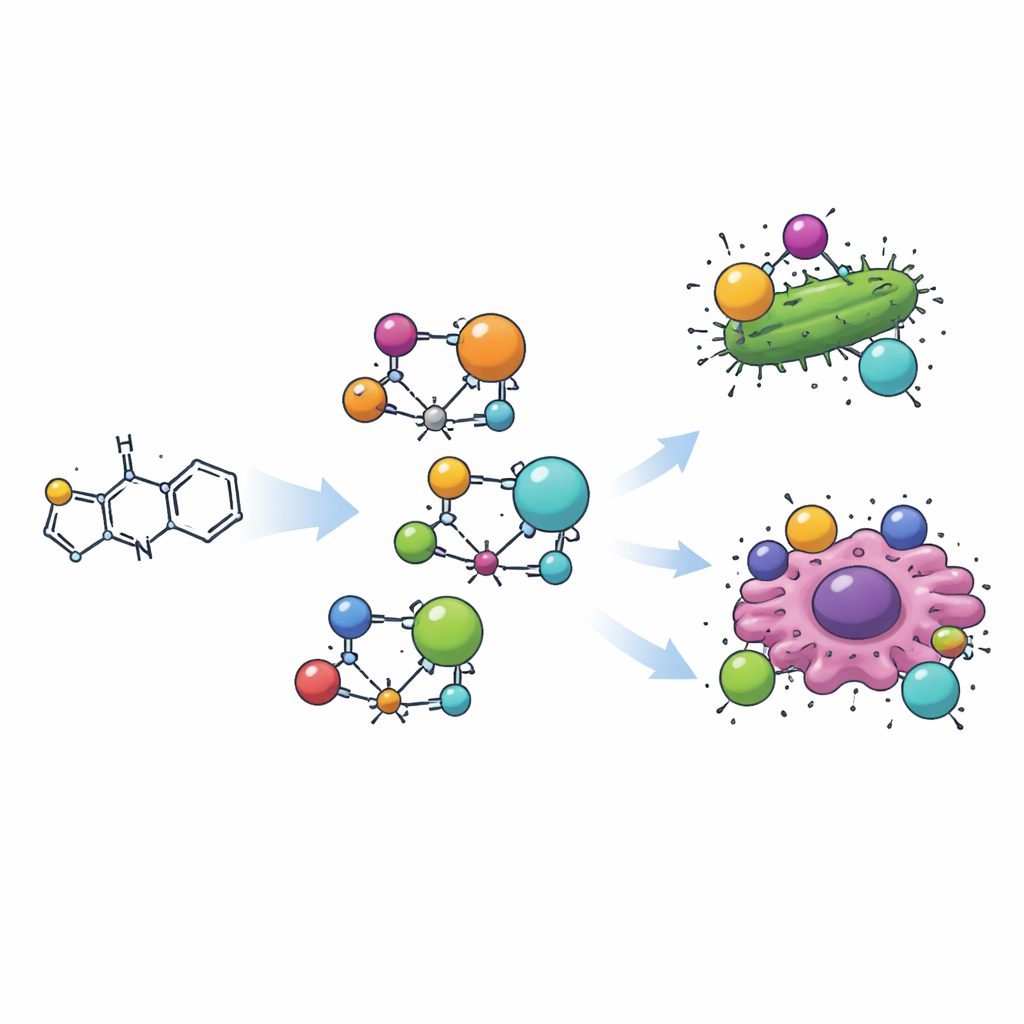
Zespół najpierw otrzymał związek organiczny przez połączenie pierścienia tiazolowego z niewielkim fragmentem aromatycznym przy użyciu klasycznej reakcji tworzenia zasady Schiffa. Nowa molekuła, oznaczona jako H2L, została następnie kompleksowana z czterema różnymi jonami metali — manganem, miedzią, cyrkonem i kadmem — tworząc cztery odrębne kompleksy metal‑organiczne. W każdym kompleksie ligand oparty na tiazolu chwyta metal przez atom azotu i pobliski atom tlenu, owijając się wokół metalu niczym szczypce. Pomiary barwy, magnetyzmu i absorpcji światła wykazały, że metale przyjmują różne geometrie trójwymiarowe: mangan i kadm tworzą struktury tetraedryczne, miedź tworzy płaską geometrię kwadratowo‑planarną, a cyrkon zajmuje pozycję w układzie oktaedrycznym.
Widzenie struktury od atomów po nanocząstki
Aby potwierdzić budowę tych kompleksów, badacze wykorzystali zestaw technik. Spektroskopia w podczerwieni i rezonansu magnetycznego jądrowego pokazały, że określone wiązania w ligancie przesuwają się po związaniu metalu, co dowodzi, że wiązanie azot‑węgiel podwójne i pobliski atom tlenu uczestniczą w koordynacji metalu. Spektrometria mas potwierdziła oczekiwane masy cząsteczkowe, a badania termiczne ujawniły temperatury, przy których odparowuje woda i ulegają rozkładowi fragmenty ramy organicznej. Dyfrakcja rentgenowska i transmisyjna mikroskopia elektronowa wykazały, że powstałe materiały są krystaliczne lub niemal krystaliczne i — co kluczowe — mają rozmiary nanometrowe. Wielkości cząstek mieściły się w przybliżeniu w zakresie od 7 do 34 nanometrów, co jest wystarczająco małe, by łatwiej pokonywać bariery biologiczne niż materiały w masowej skali.
Komputery ujawniają, jak reagują elektrony i komórki
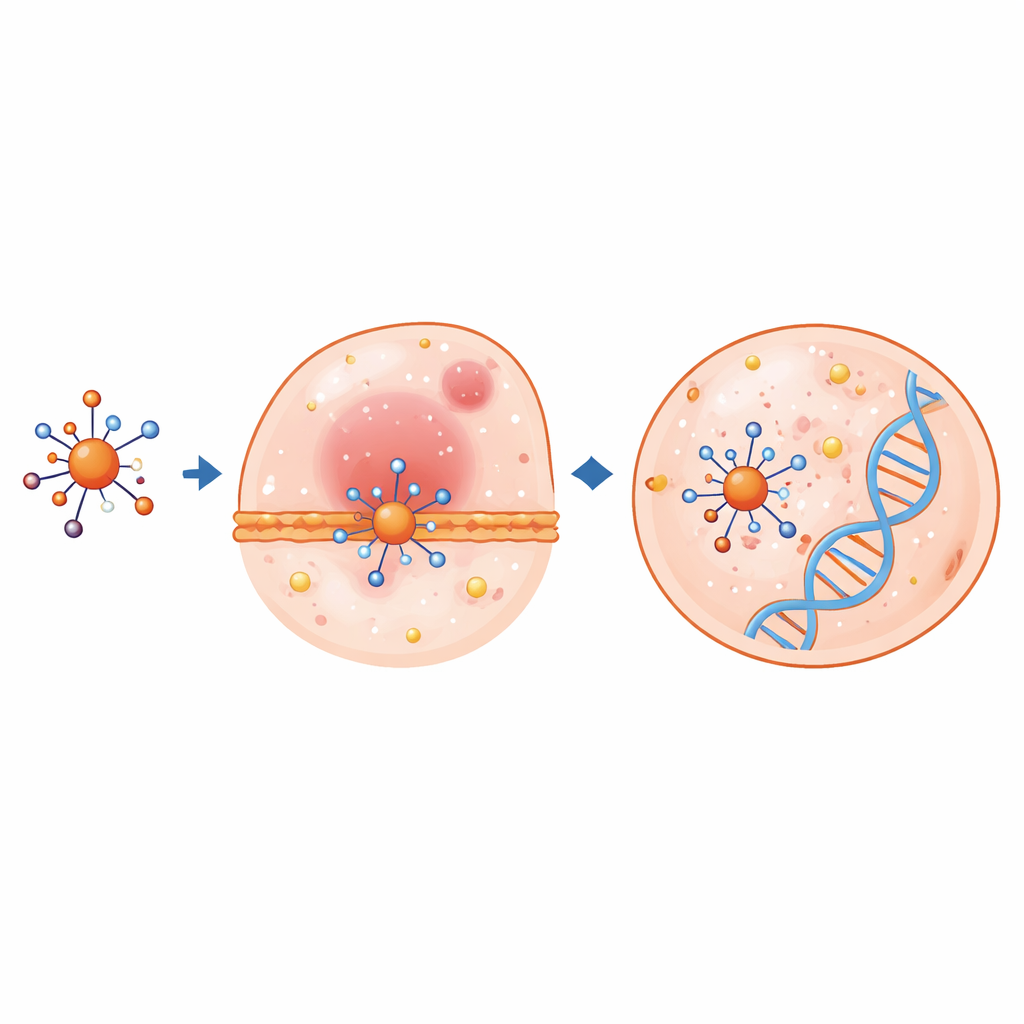
Zaawansowane obliczenia chemii kwantowej pomogły wyjaśnić, jak te kompleksy mogą zachowywać się w organizmie. Przy użyciu teorii funkcjonału gęstości naukowcy zoptymalizowali struktury atomowe i przeanalizowali najwyższe obsadzone oraz najniższe nieobsadzone orbitale molekularne, które wskazują, jak łatwo elektrony mogą się przemieszczać lub być współdzielone. Po związaniu metalu z ligandem istotne długości i kąty wiązań ulegają zmianie, a przerwa energetyczna między orbitalami obsadzonymi i pustymi często maleje — co sygnalizuje zwiększoną reaktywność chemiczną. Szczególnie kompleks miedzi wykazuje bardzo małą przerwę i silną tendencję do przyjmowania elektronów, cechy często korelujące z silnymi efektami biologicznymi. Mapy potencjału elektrostatycznego uwidoczniły obszary na molekułach najprawdopodobniej wchodzące w interakcje z naładowanymi częściami białek lub DNA.
Walka z drobnoustrojami i atak na komórki nowotworowe
Prawdziwym testem były badania biologiczne. Wolny ligand i jego cztery kompleksy metaliczne poddano próbom przeciw powszechnym bakteriom i grzybom przy użyciu standardowych testów płytkowych. Wszystkie wykazały znaczącą aktywność przeciwmikrobiową, a w wielu przypadkach kompleksy metali przewyższały znane leki, takie jak gentamycyna i amfoterycyna B. Na przykład niektóre kompleksy dały większe strefy hamowania wzrostu zarówno wobec bakterii Gram‑dodatnich, jak i Gram‑ujemnych, a także wobec problematycznych grzybów, takich jak Candida albicans. Związki testowano także przeciw liniom komórkowym ludzkiego raka wątroby (HepG‑2) i raka piersi (MCF‑7). Tu także związanie metalu znacząco zwiększyło aktywność. Kompleks miedzi był szczególnie imponujący wobec komórek raka piersi, hamując wzrost przy niższych stężeniach niż szeroko stosowany lek chemioterapeutyczny 5‑fluorouracyl. Badania dokowania komputerowego potwierdziły te wyniki, pokazując, że ligand i kompleksy mogą ciasno dopasowywać się do kieszeni białek związanych z rakiem i helis DNA, tworząc stabilizujące interakcje, które mogłyby zaburzać ich normalne funkcje.
Co to oznacza dla przyszłych terapii
Dla osoby niebędącej specjalistą kluczowy wniosek jest taki, że drobne zmiany projektowe na poziomie atomowym — dodanie centrum metalicznego, dostosowanie kształtu i redystrybucja elektronów — mogą przekształcić skromną molekułę organiczną w kompleks o rozmiarach nanometrów o silnej, ukierunkowanej aktywności biologicznej. Badanie pokazuje, że zasady Schiffa oparte na tiazolu, po sparowaniu z metalami takimi jak miedź, mogą dorównywać lub nawet przewyższać standardowe leki w testach laboratoryjnych przeciw drobnoustrojom i komórkom nowotworowym. Chociaż przed ewentualnym zastosowaniem terapeutycznym konieczne są dalsze prace, połączenie pomiarów eksperymentalnych i modelowania komputerowego daje plan działania do tworzenia kolejnej generacji terapii metal‑organicznych, które będą jednocześnie silne i selektywne.
Cytowanie: Wahdan, K.M., Mandour, H.S.A., El-Ghamry, H.A. et al. Structure elucidation and evaluation of the antimicrobial and antitumor activities of 5-methylthiazole-based Schiff base and its metal chelates. Sci Rep 16, 10738 (2026). https://doi.org/10.1038/s41598-026-40320-0
Słowa kluczowe: kompleksy metali z tiazolem, nanocząsteczkowe środki przeciwnowotworowe, ligandy zasadowe Schiffa, koordynacyjne związki przeciwmikrobowe, projektowanie leków poprzez dokowanie molekularne