Clear Sky Science · fr
Élucidation de la structure et évaluation des activités antimicrobienne et antitumorale d’une base de Schiff à base de 5‑méthylthiazole et de ses chélates métalliques
Pourquoi les petites molécules liées aux métaux comptent
La résistance aux antibiotiques et le cancer sont deux des principaux défis de la médecine moderne. Les chimistes recherchent de petites molécules intelligentes capables de pénétrer dans les cellules, de se lier à des cibles biologiques et d’arrêter des microbes nuisibles ou la croissance tumorale avec moins d’effets secondaires. Cette étude explore une famille de telles molécules construites autour d’un noyau contenant du soufre et de l’azote appelé thiazole, puis renforcées par l’association d’ions métalliques. Les chercheurs montrent comment des particules métal‑organiques soigneusement conçues peuvent devenir des agents puissants contre les bactéries, les champignons et les cellules cancéreuses, tout en utilisant des calculs avancés pour comprendre pourquoi elles sont efficaces.
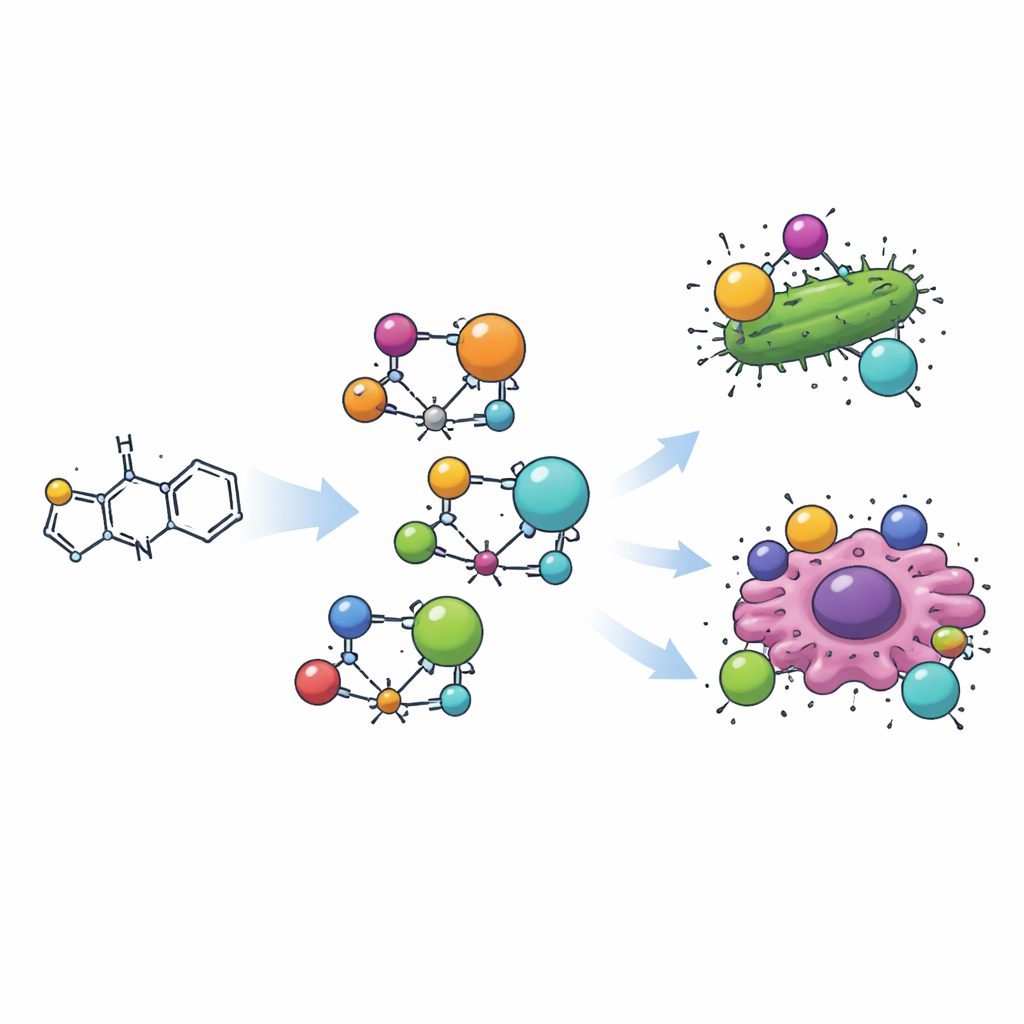
Construire une nouvelle molécule prête pour la médecine
L’équipe a d’abord synthétisé une molécule organique en joignant un noyau thiazole à un petit fragment aromatique (en forme d’anneau) via une réaction classique de « base de Schiff ». Cette nouvelle molécule, nommée H2L, a ensuite été combinée avec quatre ions métalliques différents — manganèse, cuivre, zirconium et cadmium — pour former quatre complexes métal‑organiques distincts. Dans chaque complexe, le ligand à base de thiazole saisit le métal via un atome d’azote et un atome d’oxygène voisin, enserrant le métal comme une pince. Des mesures de couleur, de magnétisme et d’absorption de la lumière ont révélé que les métaux adoptent des géométries tridimensionnelles différentes : le manganèse et le cadmium forment des structures tétraédriques, le cuivre adopte une configuration plane carrée, et le zirconium occupe une disposition octaédrique.
Voir la structure de l’atome aux nanoparticules
Pour confirmer l’architecture de ces complexes, les chercheurs ont combiné de nombreux outils. Les spectres infrarouges et de résonance magnétique nucléaire ont montré que des liaisons spécifiques du ligand se déplacent lorsque le métal est lié, prouvant que la liaison azote‑carbone double et un atome d’oxygène voisin participent à la coordination du métal. La spectrométrie de masse a confirmé les masses moléculaires attendues, tandis que des tests thermiques ont révélé à quelles températures l’eau et des fragments de la structure organique sont libérés lors de la décomposition des complexes. La diffraction des rayons X et la microscopie électronique en transmission ont montré que les matériaux obtenus sont cristallins ou quasi‑cristallins et, surtout, de taille nanométrique. Les tailles de particules variaient approximativement de 7 à 34 nanomètres, assez petites pour franchir plus facilement des barrières biologiques que des matériaux en vrac.
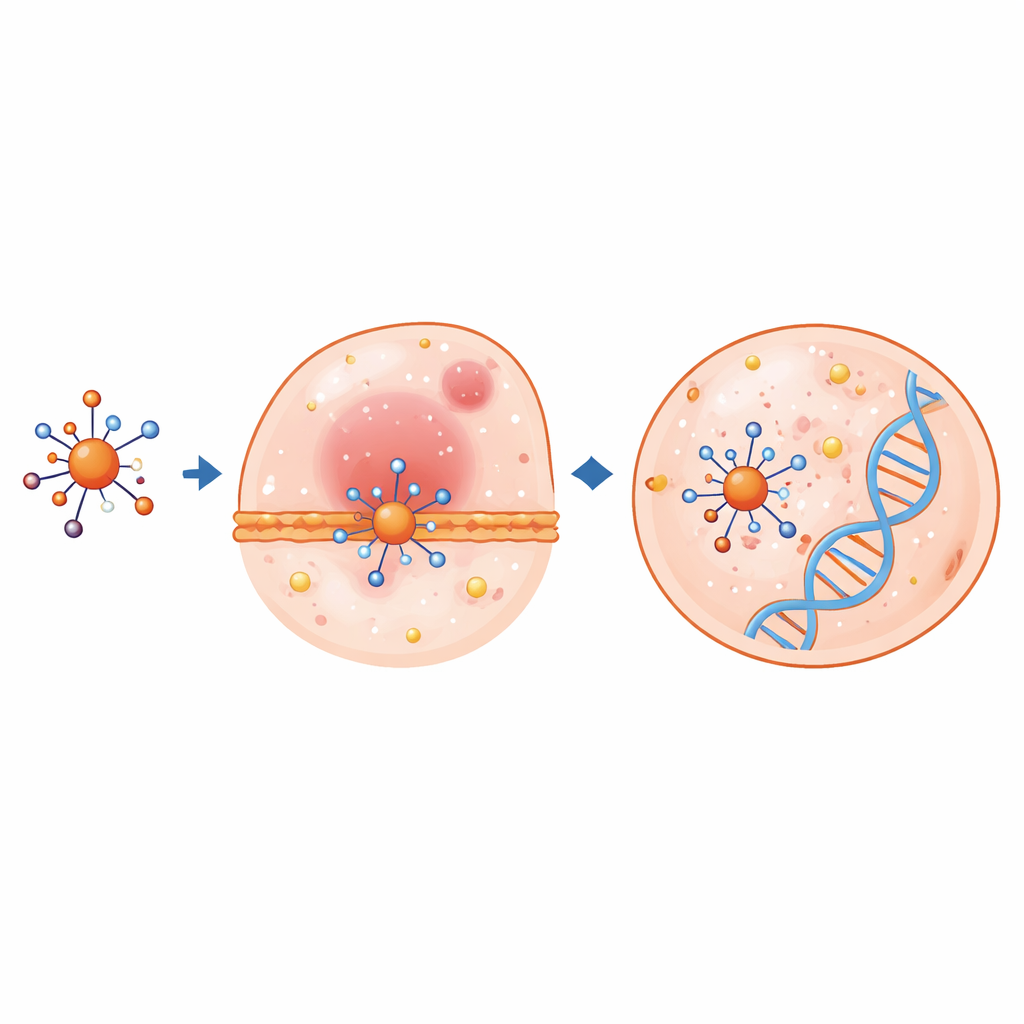
Les ordinateurs révèlent la réponse des électrons et des cellules
Des calculs quantiques avancés ont aidé à expliquer le comportement potentiel de ces complexes dans l’organisme. En utilisant la théorie de la fonctionnelle de la densité, les scientifiques ont optimisé les structures atomiques et examiné les orbitales moléculaires les plus hautes occupées et les plus basses vacantes, qui indiquent la facilité de déplacement ou de partage des électrons. Lors de la coordination du ligand aux métaux, des longueurs et des angles de liaison clés changent, et l’écart d’énergie entre les orbitales occupées et vides se réduit souvent — signalant une réactivité chimique accrue. Le complexe de cuivre montre en particulier un écart très faible et une forte tendance à accepter des électrons, des caractéristiques souvent corrélées à des effets biologiques marqués. Des cartes de potentiel électrostatique ont mis en évidence les régions des molécules les plus susceptibles d’interagir avec des parties chargées de protéines ou d’ADN.
Combattre les germes et attaquer les cellules tumorales
Le test décisif était biologique. Le ligand libre et ses quatre complexes métalliques ont été mis au défi contre des bactéries et des champignons courants à l’aide d’essais sur gélose standard. Tous ont montré une activité antimicrobienne notable, et dans de nombreux cas les complexes métalliques ont surpassé des médicaments établis tels que la gentamicine et l’amphotéricine B. Par exemple, certains complexes ont produit des zones d’inhibition plus importantes contre des bactéries Gram‑positives et Gram‑négatives, ainsi que contre des champignons problématiques comme Candida albicans. Les composés ont également été testés sur des lignées cellulaires de cancer humain du foie (HepG‑2) et du sein (MCF‑7). Là encore, la coordination métallique a considérablement augmenté la puissance. Le complexe de cuivre s’est montré particulièrement impressionnant contre les cellules du cancer du sein, inhibant la croissance à des concentrations plus faibles que la chimiothérapie couramment utilisée 5‑fluorouracile. Des études de docking informatique ont étayé ces résultats, montrant que le ligand et ses complexes peuvent s’insérer de façon ajustée dans des poches de protéines liées au cancer et des hélices d’ADN, formant des interactions stabilisantes susceptibles de perturber leur fonction normale.
Ce que cela signifie pour les traitements futurs
Pour un non‑spécialiste, le message clé est que de petites modifications de conception au niveau atomique — ajouter un centre métallique, ajuster la forme et redistribuer les électrons — peuvent transformer une molécule organique modeste en un complexe de taille nanométrique présentant une activité biologique forte et ciblée. Cette étude montre que les bases de Schiff à base de thiazole, associées à des métaux comme le cuivre, peuvent rivaliser ou même surpasser des médicaments standards dans des tests en laboratoire contre des microbes et des cellules cancéreuses. Bien qu’il reste beaucoup de travail avant que l’un de ces complexes ne devienne un médicament, la combinaison de mesures expérimentales et de modélisation informatique offre une feuille de route pour créer des thérapies métal‑organiques de nouvelle génération à la fois puissantes et sélectives.
Citation: Wahdan, K.M., Mandour, H.S.A., El-Ghamry, H.A. et al. Structure elucidation and evaluation of the antimicrobial and antitumor activities of 5-methylthiazole-based Schiff base and its metal chelates. Sci Rep 16, 10738 (2026). https://doi.org/10.1038/s41598-026-40320-0
Mots-clés: complexes métalliques de thiazole, agents anticancéreux nanoparticulaires, ligands base de Schiff, composés de coordination antimicrobiens, conception de médicaments par docking moléculaire