Clear Sky Science · ar
تحديد البنية وتقييم الفعاليات المضادة للميكروبات والمضادة للأورام لقاعدة شيف المبنية على 5-ميثيلثيازول ومُعقّداتها الأيونية
لماذا تهم الجزيئات المرتبطة بالمعادن الصغيرة
المقاومة للمضادات الحيوية والسرطان هما من أكبر التحديات في الطب الحديث. يبحث الكيميائيون عن جزيئات صغيرة وذكية يمكنها دخول الخلايا، والالتصاق بالأهداف البيولوجية، وإيقاف الكائنات الممرِضة أو نمو الأورام مع آثار جانبية أقل. تستكشف هذه الدراسة عائلة من هذه الجزيئات المبنية على حلقة تحتوي الكبريت والنيتروجين تُدعى ثيازول، ثم تقوَّى بربط أيونات معدنية. يوضح الباحثون كيف يمكن للجسيمات المعدنية العضوية المصممة بعناية أن تصبح مقاتِلات فعالة ضد البكتيريا والفطريات وخلايا السرطان، مع الاستفادة من حسابات متقدمة لفهم سبب فعاليتها.
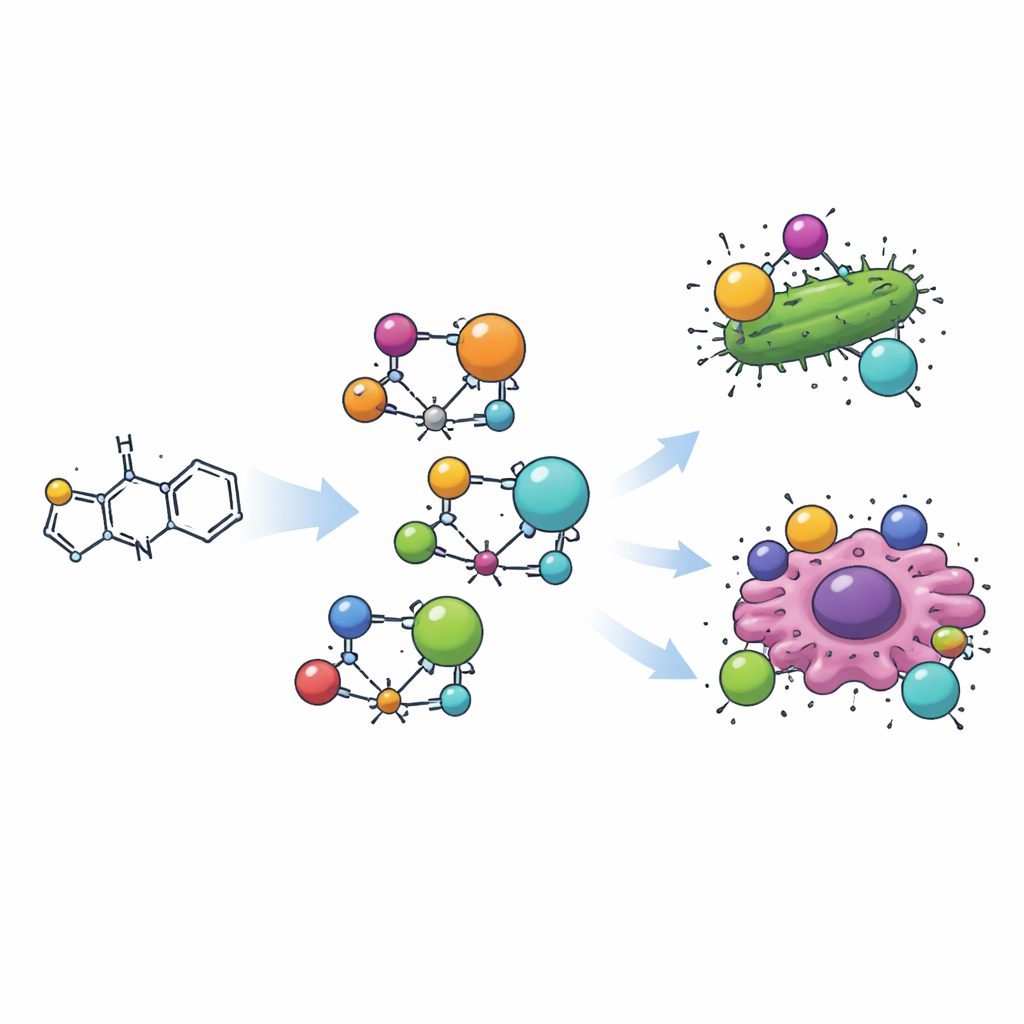
بناء جزيء جديد جاهز للاستخدام الدوائي
أنشأ الفريق أولاً جزيئًا عضويًا بربط حلقة ثيازول بمقطع عطري صغير باستخدام تفاعل «قاعدة شيف» التقليدي. سُمي هذا الجزيء الجديد H2L، ثم أُدمج مع أربعة أيونات معدنية مختلفة — المنغنيز والنحاس والزركونيوم والكادميوم — لتشكيل أربعة مُعقّدات معدنية عضوية مميزة. يمسك كل مُعقّد بالربط المشتق من الثيازول بالمعدن عبر ذرة نيتروجين وذرة أكسجين مجاورة، ملفوفًا حول المعدن كالمخلب. أظهرت قياسات دقيقة للون والمغناطيسية وامتصاص الضوء أن المعادن تعتمد أشكالًا ثلاثية الأبعاد مختلفة: يشكل المنغنيز والكادميوم هياكل رباعية السطوح، ويكوّن النحاس وحدة مسطحة مربعة المستوي، ويجلس الزركونيوم في ترتيب ثُماني السطوح.
رؤية البنية من الذرات حتى الجسيمات النانوية
لتأكيد كيفية بناء هذه المُعقّدات، جمع الباحثون العديد من الأدوات. أظهرت أطياف الأشعة تحت الحمراء والرنين المغناطيسي النووي أن روابط محددة في الليجاند تتحول عند ارتباط المعدن، مثبتةً أن رابطة النيتروجين–الكربون المزدوجة وذرة الأكسجين المجاورة متورطتان في الإمساك بالمعدن. أكدت مطيافية الكتلة الأوزان الجزيئية المتوقعة، بينما كشفت اختبارات تعتمد على الحرارة متى يُطلق الماء وأجزاء من الإطار العضوي أثناء تحلل المُعقّدات. أظهرت حيود الأشعة السينية والمجهر الإلكتروني النافذ أن المواد الناتجة بلورية أو شبه بلورية، والأهم — ذات أحجام نانومترية. تراوحت أحجام الجسيمات تقريبًا من 7 إلى 34 نانومتر، صغيرة بما يكفي لاجتياز الحواجز البيولوجية بسهولة أكبر من المواد السائبة.
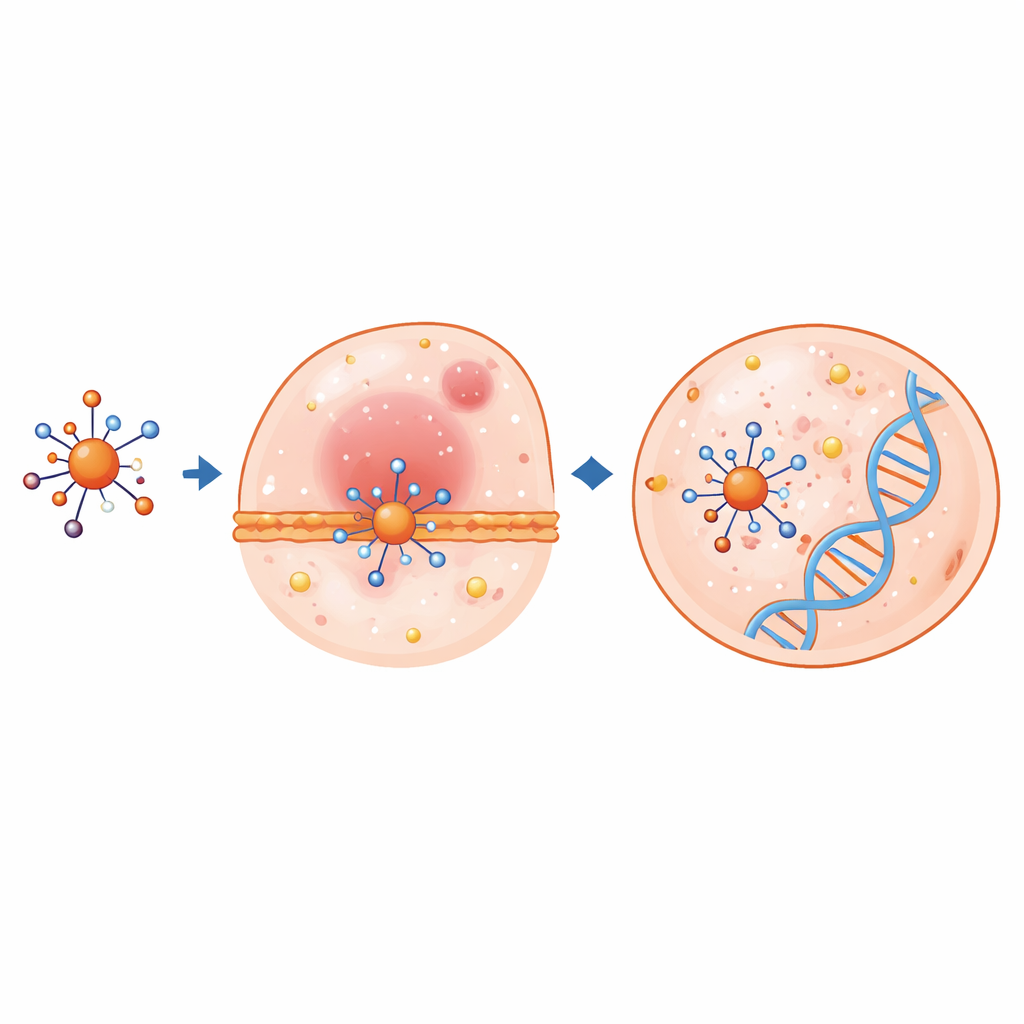
تشرح الحواسيب كيفية استجابة الإلكترونات والخلايا
ساعدت حسابات كيمياء الكم المتقدمة في تفسير كيفية سلوك هذه المُعقّدات داخل الجسم. باستخدام نظرية الدوال الكثافة، قام العلماء بتحسين الهياكل الذرية وفحصوا أعلى المدارات الجزيئية المشغولة وأدنى المدارات الجزيئية الخالية، والتي تشير إلى سهولة حركة الإلكترونات أو مشاركتها. عند ارتباط الليجاند بالمعادن، تتغير أطوال وزوايا الروابط الأساسية، وغالبًا ما يتقلص الفارق الطاقي بين المدارات المشغولة والخالية — ما يشير إلى تفاعلية كيميائية أعلى. يظهر المُعقّد النحاسي على وجه الخصوص فجوة طاقية صغيرة جدًا وميل قوي لقبول الإلكترونات، صفات غالبًا ما تتوافق مع تأثيرات بيولوجية قوية. سلطت خرائط الجهد الكهروستاتيكي الضوء على المناطق في الجزيئات الأكثر احتمالًا للتفاعل مع الأجزاء المشحونة في البروتينات أو الـDNA.
محاربة الجراثيم ومهاجمة خلايا الورم
كان الاختبار الحقيقي بيولوجيًا. تعرض الليجاند الحر ومُعقّداته الأربعة لاختبارات ضد بكتيريا وفطريات شائعة باستخدام اختبارات الصفيحة القياسية. أظهرت جميعها نشاطًا مضادًا للميكروبات ملحوظًا، وفي العديد من الحالات تفوّقت المُعقّدات المعدنية على أدوية معروفة مثل الجنتاميسين والأمفوتيريسين ب. على سبيل المثال، أنتجت بعض المُعقّدات مناطق تثبيط أكبر ضد كلٍ من البكتيريا إيجابية وسالبة الغرام، وكذلك فطريات مشكلة مثل Candida albicans. اختُبرت المركبات أيضًا ضد خطوط خلايا سرطان الكبد البشري (HepG-2) وسرطان الثدي (MCF-7). هنا أيضًا عزز الارتباط المعدني الفاعلية بشكل كبير. أظهر المُعقّد النحاسي أداءً مميزًا ضد خلايا سرطان الثدي، مع تثبيط للنمو عند تراكيز أقل من دواء العلاج الكيميائي واسع الاستخدام 5‑فلورويوراسيل. دعمت دراسات المحاكاة الجزيئية هذه النتائج، مبيّنة أن الليجاند والمُعقّدات يمكن أن تتوائم جيدًا مع جيوب البروتينات المرتبطة بالسرطان وحلزونات الـDNA، مكوِّنةً تفاعلات مُثبِّطة قد تعطل الوظيفة الطبيعية.
ماذا يعني هذا العمل للعلاجات المستقبلية
لغير المتخصص، الرسالة الأساسية هي أن تغييرات تصميم صغيرة على المستوى الذري — إضافة مركز معدني، ضبط الشكل، وإعادة توزيع الإلكترونات — يمكن أن تحول جزيئًا عضويًا متواضعًا إلى مُعقّد بحجم نانومتر يمتلك نشاطًا بيولوجيًا قويًا ومُوجَّهًا. تُظهر هذه الدراسة أن قواعد شيف المبنية على الثيازول، عند اقترانها بمعادن مثل النحاس، يمكن أن تضاهِي أو تتفوّق على أدوية معيارية في اختبارات المختبر ضد الميكروبات وخلايا السرطان. ومع حاجة الكثير من العمل قبل أن تتحول أي من هذه المُعقّدات إلى أدوية، يوفر الجمع بين القياسات التجريبية والنمذجة الحاسوبية خارطة طريق لإنشاء علاجات معدنية‑عضوية من الجيل القادم تكون قوية وذات اختيارات دقيقة.
الاستشهاد: Wahdan, K.M., Mandour, H.S.A., El-Ghamry, H.A. et al. Structure elucidation and evaluation of the antimicrobial and antitumor activities of 5-methylthiazole-based Schiff base and its metal chelates. Sci Rep 16, 10738 (2026). https://doi.org/10.1038/s41598-026-40320-0
الكلمات المفتاحية: مُعقّدات الثيازول المعدنية, عوامل مكافحة السرطان النانوية, روابط قاعدة شيف, مركبات التنسيق المضادة للميكروبات, تصميم الأدوية عبر محاكاة الارتباط الجزيئي