Clear Sky Science · it
Elucidazione della struttura e valutazione delle attività antimicrobiche e antitumorali di una base di Schiff 5-metiltiazolica e dei suoi chelati metallici
Perché contano le piccole molecole legate a metalli
La resistenza agli antibiotici e il cancro sono due delle sfide più importanti della medicina moderna. I chimici cercano piccole molecole intelligenti che possano penetrare nelle cellule, legarsi a bersagli biologici e bloccare microrganismi dannosi o la crescita tumorale con effetti collaterali ridotti. Questo studio esplora una famiglia di tali molecole costruite a partire da un anello contenente zolfo e azoto chiamato tiazolo, poi rafforzate dall’aggiunta di ioni metallici. I ricercatori mostrano come particelle metallo‑organiche progettate con cura possano diventare efficaci contro batteri, funghi e cellule tumorali, usando inoltre calcoli avanzati per capire il motivo della loro attività.
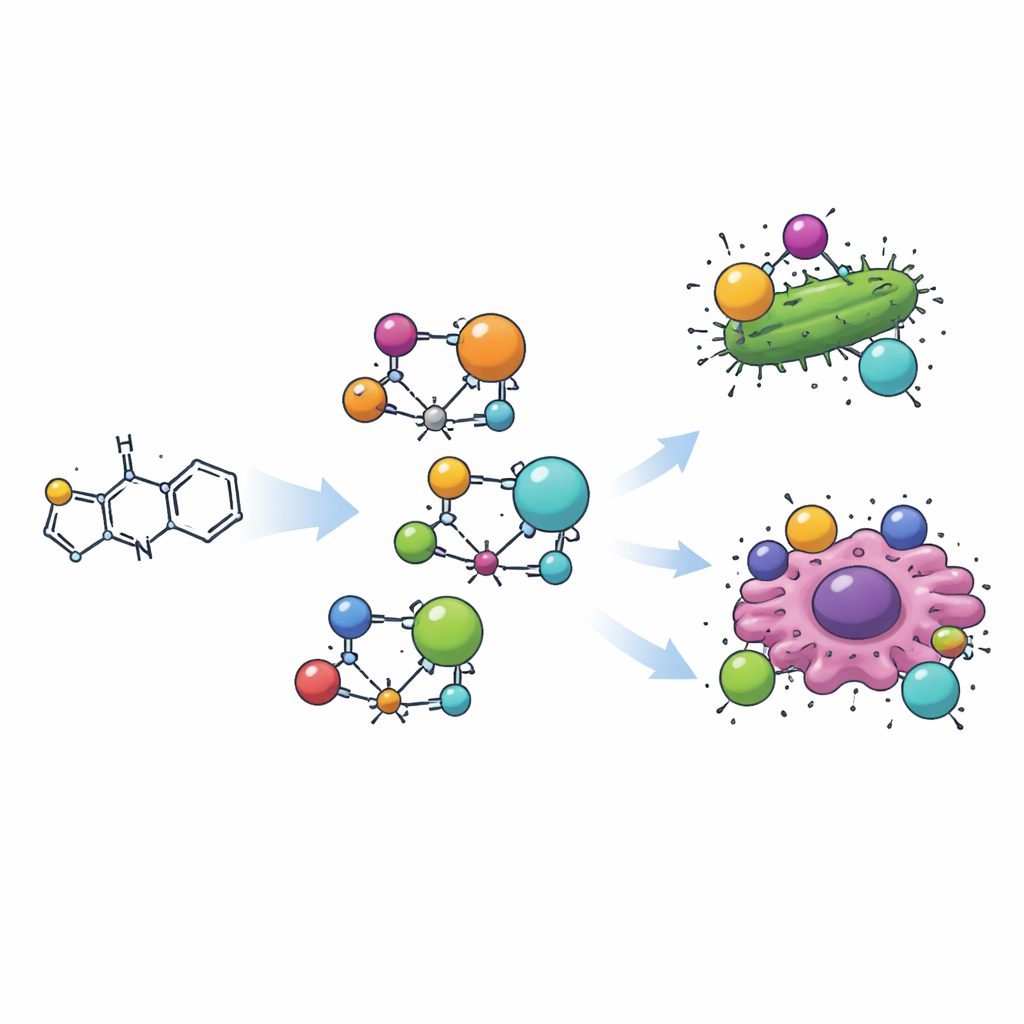
Costruire una nuova molecola pronta per la medicina
Il gruppo ha prima sintetizzato una molecola organica unendo un anello di tiazolo a un piccolo frammento aromatico tramite la classica reazione di base di Schiff. Questa nuova molecola, chiamata H2L, è stata quindi combinata con quattro diversi ioni metallici—manganese, rame, zirconio e cadmio—per formare quattro distinti complessi metallo‑organici. In ciascun complesso il ligando a base di tiazolo avvolge il metallo attraverso un atomo di azoto e un atomo di ossigeno vicino, agendo come una pinza. Misurazioni attente di colore, magnetismo e assorbimento di luce hanno rivelato che i metalli assumono geometrie tridimensionali diverse: manganese e cadmio formano strutture tetraedriche (a quattro vertici), il rame dà una unità planare quadrata, e lo zirconio occupa una disposizione ottaedrica (a sei vertici).
Osservare la struttura dagli atomi alle nanoparticelle
Per confermare l’architettura di questi complessi i ricercatori hanno combinato numerosi strumenti. Spettri infrarossi e di risonanza magnetica nucleare hanno mostrato che legami specifici nel ligando si spostano quando il metallo è coordinato, provando che il doppio legame azoto‑carbonio e un ossigeno vicino sono coinvolti nell’ancoraggio del metallo. La spettrometria di massa ha confermato i pesi molecolari attesi, mentre test termici hanno rivelato quando l’acqua e porzioni del quadro organico vengono rilasciate durante la decomposizione dei complessi. La diffrazione a raggi X e la microscopia elettronica a trasmissione hanno dimostrato che i materiali risultanti sono cristallini o quasi cristallini e, cosa cruciale, di dimensioni nanometriche. Le dimensioni delle particelle variavano approssimativamente da 7 a 34 nanometri, abbastanza piccole da attraversare più facilmente barriere biologiche rispetto ai materiali in massa.
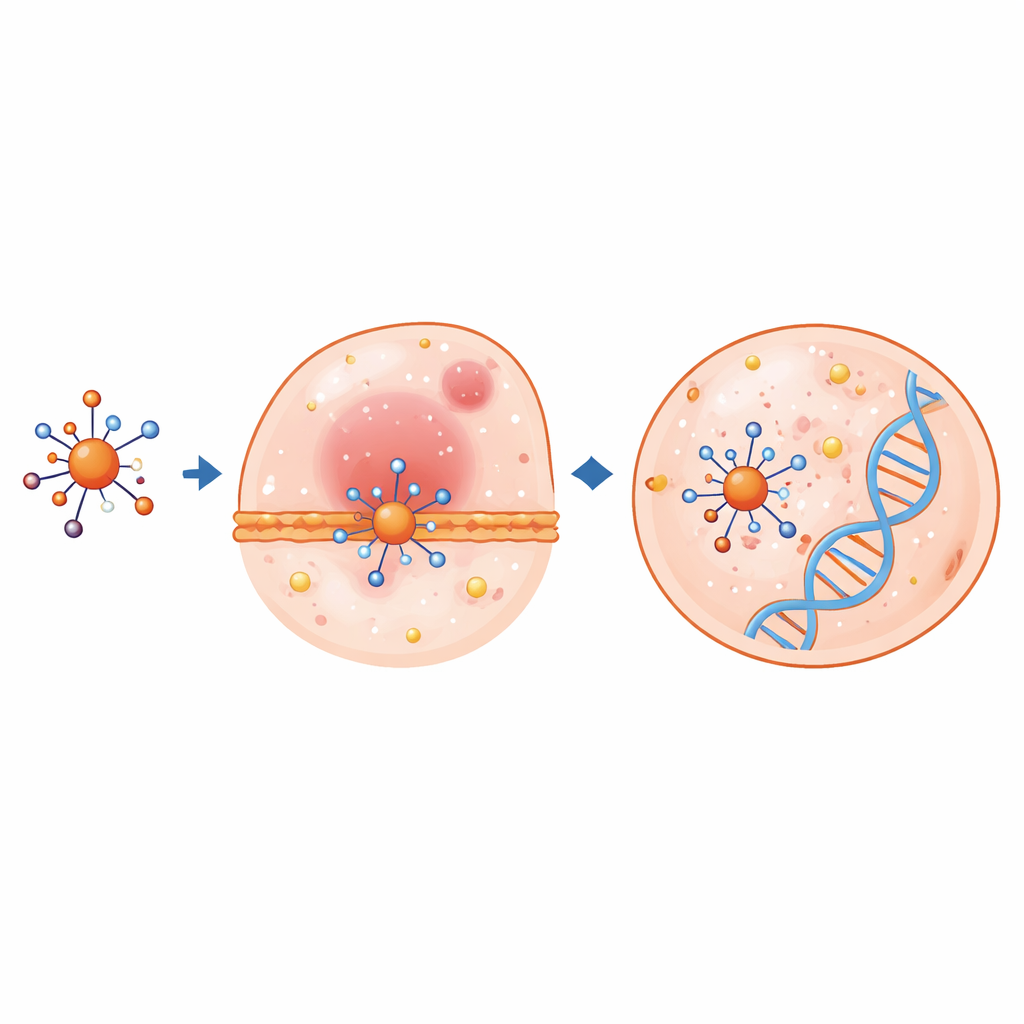
I computer rivelano come rispondono elettroni e cellule
Calcoli chimici quantistici avanzati hanno aiutato a spiegare come questi complessi potrebbero comportarsi nell’organismo. Utilizzando la teoria del funzionale della densità, gli scienziati hanno ottimizzato le strutture atomiche ed esaminato gli orbitali molecolari occupati più alti e non occupati più bassi, indicatori di quanto facilmente gli elettroni possono muoversi o essere condivisi. Quando il ligando si coordina ai metalli, lunghezze e angoli di legame chiave cambiano e il gap energetico tra orbitali occupati e vuoti spesso si riduce—segnale di una maggiore reattività chimica. Il complesso di rame in particolare mostra un gap molto piccolo e una forte tendenza ad accettare elettroni, caratteristiche che frequentemente si correlano con intensi effetti biologici. Mappe di potenziale elettrostatico hanno evidenziato le regioni delle molecole più probabili per interagire con parti caricate di proteine o DNA.
Combattere germi e attaccare cellule tumorali
La prova definitiva è stata biologica. Il ligando libero e i suoi quattro complessi metallici sono stati messi alla prova contro batteri e funghi comuni usando saggi su piastra standard. Tutti hanno mostrato attività antimicrobica notevole e, in molti casi, i complessi metallici hanno superato farmaci consolidati come la gentamicina e l’amfotericina B. Per esempio, alcuni complessi hanno prodotto zone di inibizione più ampie sia contro batteri Gram‑positivi sia Gram‑negativi, oltre che contro funghi problematici come Candida albicans. I composti sono stati inoltre testati su linee cellulari tumorali umane del fegato (HepG‑2) e del seno (MCF‑7). Anche qui il legame al metallo ha aumentato notevolmente la potenza. Il complesso di rame è stato particolarmente impressionante contro le cellule del cancro mammario, inibendo la crescita a concentrazioni inferiori rispetto al farmaco chemioterapico ampiamente usato 5‑fluorouracile. Studi di docking computazionale hanno supportato questi risultati, mostrando che il ligando e i complessi si inseriscono comodamente nelle tasche di proteine correlate al cancro e in eliche di DNA, formando interazioni stabilizzanti che potrebbero compromettere la funzione normale.
Cosa significa questo lavoro per i trattamenti futuri
Per un non specialista, il messaggio chiave è che piccoli cambiamenti progettuali a livello atomico—aggiungere un centro metallico, modulare la forma e ridistribuire gli elettroni—possono trasformare una modesta molecola organica in un complesso su scala nanometrica con forte attività biologica mirata. Questo studio mostra che basi di Schiff a base di tiazolo, abbinate a metalli come il rame, possono rivaleggiare o perfino superare farmaci standard nei test di laboratorio contro microrganismi e cellule tumorali. Sebbene sia necessario molto lavoro prima che uno di questi complessi diventi un farmaco, la combinazione di misure sperimentali e modellizzazione computazionale offre una roadmap per creare terapie metallo‑organiche di nuova generazione sia potenti sia selettive.
Citazione: Wahdan, K.M., Mandour, H.S.A., El-Ghamry, H.A. et al. Structure elucidation and evaluation of the antimicrobial and antitumor activities of 5-methylthiazole-based Schiff base and its metal chelates. Sci Rep 16, 10738 (2026). https://doi.org/10.1038/s41598-026-40320-0
Parole chiave: complessi metallici a base di tiazolo, agenti antitumorali a nanoparticelle, ligandi base di Schiff, composti di coordinazione antimicrobici, progettazione di farmaci mediante docking molecolare