Clear Sky Science · tr
5-metiltiazol bazlı Schiff bazı ve onun metal şelatlarının yapısal açıklanması ve antimikrobiyal ile antitümör aktivitelerinin değerlendirilmesi
Neden metal bağlantılı küçük moleküller önemli
Antibiyotik direnci ve kanser, modern tıbbın en büyük iki zorluğundan biridir. Kimyagerler, hücrelere girip biyolojik hedeflere tutunabilen ve daha az yan etkiyle zararlı mikropları veya tümör büyümesini durdurabilen küçük, akıllı moleküller arıyor. Bu çalışma, tiyazol adı verilen sülfür ve azot içeren bir halkadan türetilen ve ardından metal iyonları eklenerek güçlendirilen bu tür molekül ailesini inceliyor. Araştırmacılar, dikkatle tasarlanmış metal‑organik parçacıkların bakterilere, mantarlara ve kanser hücrelerine karşı güçlü savaşçılar haline gelebileceğini ve bunların neden işe yaradığını anlamak için gelişmiş hesaplamalardan yararlandıklarını gösteriyor.
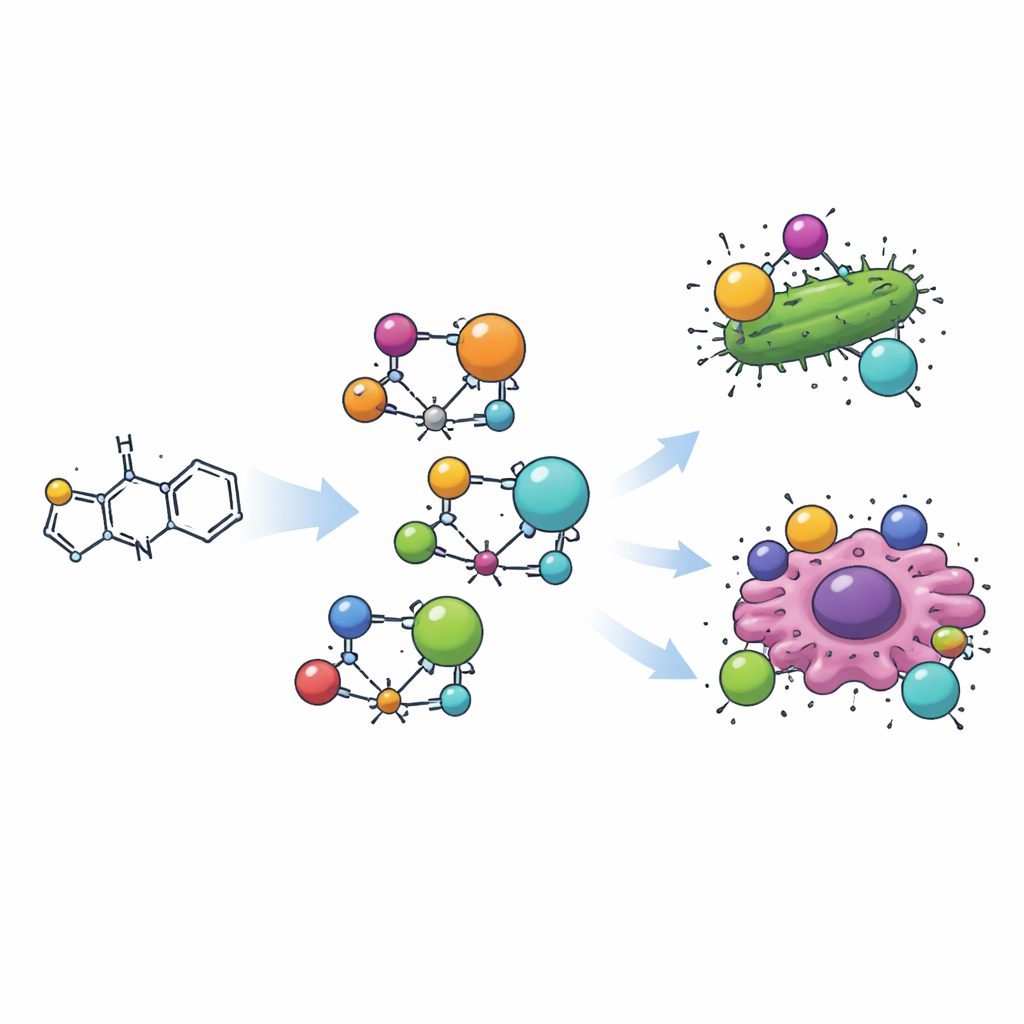
İlaç yapımına uygun yeni bir molekül inşa etmek
Ekip, önce tiyazol halkasını küçük bir aromatik (halkasal) parça ile klasik bir “Schiff bazı” reaksiyonu kullanarak birleştirerek organik bir molekül oluşturdu. H2L adını verdikleri bu yeni molekül daha sonra manganez, bakır, zirkonyum ve kadmiyum olmak üzere dört farklı metal iyonu ile birleştirilerek dört ayrı metal‑organik kompleks oluşturuldu. Her komplekste tiyazol bazlı ligand, metale bir azot atomu ve yakınındaki bir oksijen atomu üzerinden tutunarak metalin etrafını pençe gibi sarıyor. Renk, manyetizma ve ışık absorpsiyonu gibi dikkatli ölçümler, metallerin farklı üç boyutlu şekiller benimsediğini ortaya koydu: manganez ve kadmiyum tetrahedral (dört köşeli) yapılar oluştururken, bakır düz bir kare‑planar ünite ve zirkonyum ise oktahedral (altı köşeli) bir düzenlenme gösteriyor.
Atomlardan nanoparçacıklara yapıyı görmek
Bu komplekslerin nasıl inşa edildiğini doğrulamak için araştırmacılar birçok aracı bir araya getirdi. Kızılötesi ve nükleer manyetik rezonans spektrumları, metal bağlandığında ligand içindeki belirli bağların kaydığını göstererek azot‑karbon çift bağının ve yakınındaki bir oksijen atomunun metale tutunmada rol oynadığını kanıtladı. Kütle spektrometrisi beklenen moleküler ağırlıkları doğrularken, ısıya dayalı testler komplekslerin ayrışması sırasında suyun ve organik iskelet parçalarının ne zaman ayrıldığını ortaya koydu. X‑ışını kırınımı ve geçirimli elektron mikroskobu, ortaya çıkan malzemelerin kristalin veya neredeyse kristalin olduğunu ve—kritik olarak—nanometre ölçeğinde olduğunu gösterdi. Parçacık boyutları yaklaşık olarak 7 ila 34 nanometre arasında değişti; bu da hacimsel malzemelere göre biyolojik engellerden daha kolay geçebilecek kadar küçüktür.
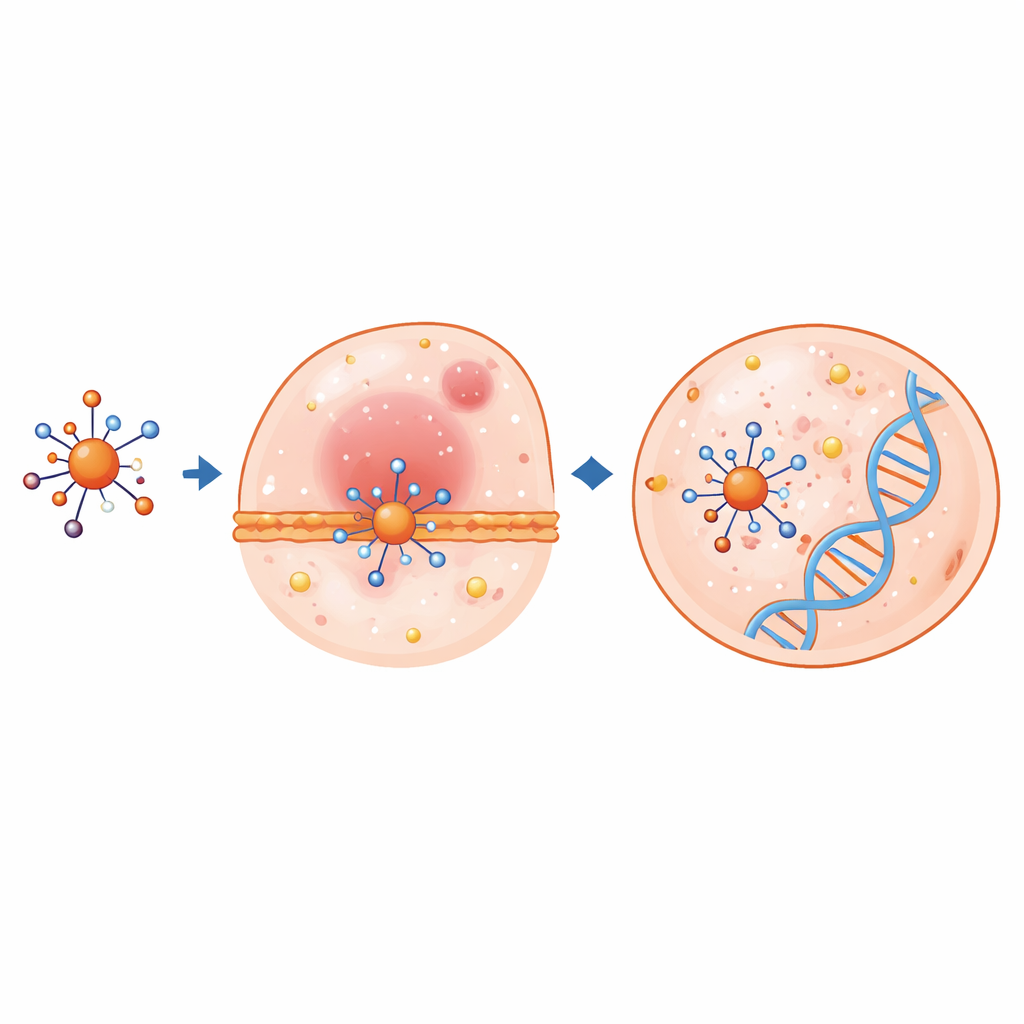
Bilgisayarlar elektronların ve hücrelerin nasıl tepki verdiğini ortaya koyuyor
Gelişmiş kuantum kimyası hesaplamaları, bu komplekslerin vücut içinde nasıl davranabileceğini açıklamaya yardımcı oldu. Yoğunluk fonksiyonel teorisi kullanılarak, atomik yapılar optimize edildi ve en yüksek dolu ile en düşük boş moleküler orbitaller incelendi; bunlar elektronların ne kadar kolay hareket edebileceğini veya paylaşılabileceğini gösterir. Ligand metalle bağlandığında önemli bağ uzunlukları ve açılar değişiyor ve dolu ile boş orbitaller arasındaki enerji boşluğu sık sık küçülüyor—bu durum daha yüksek kimyasal reaktiviteyi işaret ediyor. Özellikle bakır kompleksi çok küçük bir boşluğa ve elektronu kabul etme eğilimine sahip; bu özellikler genellikle güçlü biyolojik etkiyle ilişkilidir. Elektrostatik potansiyel haritaları, moleküllerin proteinlerin veya DNA'nın yüklü bölgeleriyle en olası etkileşim kuracağı bölgeleri vurguladı.
Mikroplarla savaşmak ve tümör hücrelerine saldırmak
Gerçek test biyolojik deneylerdi. Serbest ligand ve dört metal kompleksi, standart plak denemeleri kullanılarak yaygın bakteri ve mantarlara karşı sınandı. Tüm bileşikler kayda değer antimikrobiyal aktivite gösterdi ve birçok durumda metal kompleksleri gentamisin ve amfoterisin B gibi bilinen ilaçlardan daha iyi performans sergiledi. Örneğin bazı kompleksler, hem Gram‑pozitif hem Gram‑negatif bakterilere ve Candida albicans gibi sorunlu mantarlara karşı daha büyük inhibisyon zonları oluşturdu. Bileşikler ayrıca insan karaciğer kanseri (HepG‑2) ve meme kanseri (MCF‑7) hücre hatlarına karşı test edildi. Burada da metal bağlanması etkinliği büyük ölçüde artırdı. Bakır kompleksi, özellikle meme kanseri hücreleri üzerinde etkileyiciydi; yaygın kullanılan kemoterapi ilacı 5‑florourasilden daha düşük konsantrasyonlarda büyümeyi engelledi. Bilgisayar doklama çalışmaları, ligand ve komplekslerin kanserle ilişkili proteinlerin ve DNA sarmallarının ceplerine sıkıca oturabildiğini ve normal işlevi bozabilecek stabilize edici etkileşimler oluşturduğunu göstererek bu bulguları destekledi.
Bu çalışmanın gelecekteki tedaviler için anlamı
Bir uzman olmayan için temel mesaj, atomik düzeyde yapılan küçük tasarım değişikliklerinin—bir metal merkezi eklemek, şekli ayarlamak ve elektron dağılımını değiştirmek—sıradan bir organik molekülü güçlü, hedefe yönelik biyolojik aktiviteye sahip nanometre ölçeğinde bir komplekse dönüştürebileceğidir. Bu çalışma, tiazol bazlı Schiff bazlarının bakır gibi metallerle eşleştirildiğinde mikrop ve kanser hücrelerine karşı laboratuvar deneylerinde standart ilaçlarla rekabet edebileceğini veya onları aşabileceğini gösteriyor. Bu komplekslerin herhangi birinin ilaç haline gelmesinden önce çok daha fazla çalışma gerekirken, deneysel ölçümler ile bilgisayar modellemesinin birleşimi, hem güçlü hem de seçici olabilecek gelecek nesil metal‑organik terapiler oluşturmak için bir yol haritası sunuyor.
Atıf: Wahdan, K.M., Mandour, H.S.A., El-Ghamry, H.A. et al. Structure elucidation and evaluation of the antimicrobial and antitumor activities of 5-methylthiazole-based Schiff base and its metal chelates. Sci Rep 16, 10738 (2026). https://doi.org/10.1038/s41598-026-40320-0
Anahtar kelimeler: tiazol metal kompleksleri, nanosabıt anticancer ajanlar, Schiff bazı ligandları, antimikrobiyal koordinasyon bileşikleri, moleküler doklama ilaç tasarımı