Clear Sky Science · zh
普拉克索通过 Nrf2/SLC7A11/GPX4 通路缓解氧-葡萄糖剥夺/复氧诱导的 HT22 细胞铁死亡
为什么卒中后保护脑细胞很重要
当患者发生缺血性卒中时,血栓使部分脑组织缺氧缺糖。医生会紧急通畅被闭塞的血管,但具有讽刺意味的是,血流的骤然恢复本身也会损伤脆弱的脑细胞。本研究探讨了已用于帕金森病的药物普拉克索是否能在第二波损伤中保护神经细胞,方法是抑制近年来发现的一种与铁和失控氧化有关的细胞死亡形式。
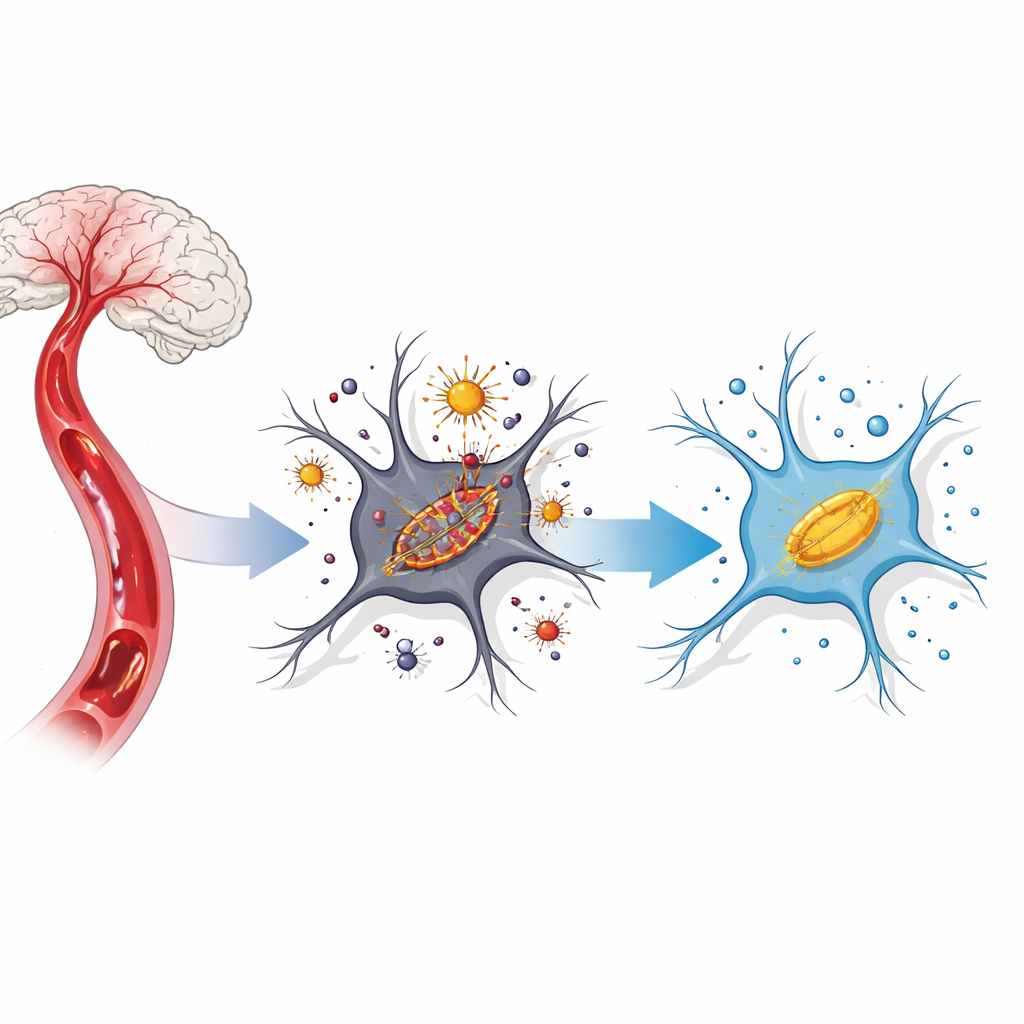
脑细胞内的有害连锁反应
在血流被切断然后恢复后,脑细胞会经历一系列化学应激。通常被封存的铁在细胞内变得游离并与氧反应,生成被称为活性氧的强烈分子。这些分子攻击富含脂质的细胞膜,尤其是线粒体这些微小的能量工厂。科学家现在称这种以铁驱动、针对膜的细胞死亡为“铁死亡”。在卒中模型中,当铁积聚、保护性抗氧化物下降以及线粒体收缩并功能失调时,会出现铁死亡的特征。
在类卒中实验模型中测试普拉克索
为了模拟卒中及随后的处理,研究人员使用小鼠海马神经细胞(HT22 细胞),短暂剥夺其氧气和葡萄糖然后恢复正常条件。该氧-葡萄糖剥夺/复氧模型重现了缺血-再灌注损伤的许多特征。团队以不同剂量和不同给药时机处理细胞,测量存活率、线粒体健康、铁水平、活性氧以及关键抗氧化系统。他们还使用专门触发铁死亡的化学物质埃拉斯丁(erastin),以观察普拉克索是否能直接拮抗这一过程。
药物如何在细胞内恢复平衡
在没有保护的情况下,类卒中处理降低了细胞存活率,破坏了线粒体膜电位,增加了铁和活性氧,并耗竭了抗氧化分子谷胱甘肽及依赖其作用的酶 GPX4。在电子显微镜下,线粒体显得更小、更致密,符合铁死亡的标志。普拉克索,尤以在复氧期给予的中等剂量最为明显,逆转了许多这些变化:细胞存活率提高,线粒体保持形态和电位,铁和氧化剂减少,谷胱甘肽与 GPX4 活性恢复。当细胞被埃拉斯丁损伤时也观察到类似益处,这强化了普拉克索通过抑制铁死亡而非仅仅发挥广义抗氧化作用的观点。
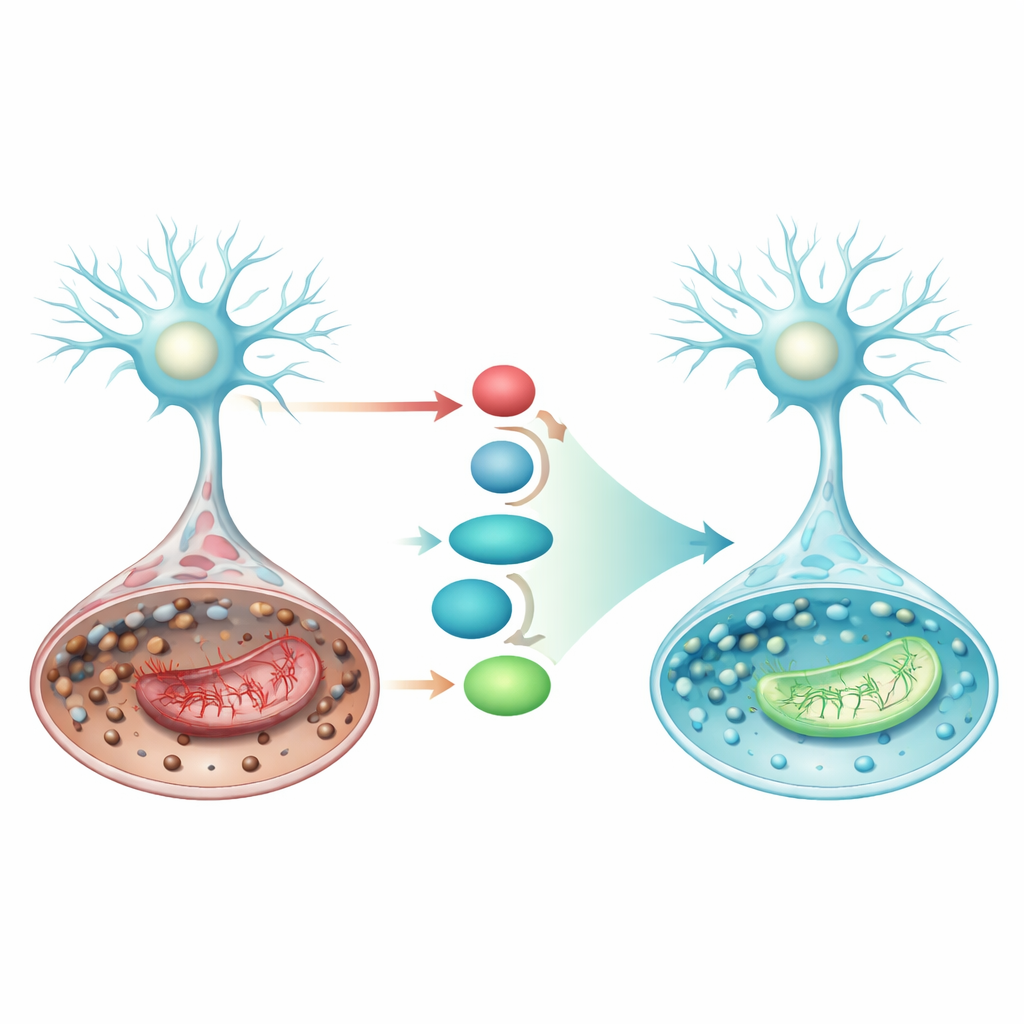
激活细胞内的防御通路
研究还聚焦于一条内在的细胞防御线,即 Nrf2 及其下游分子。当被激活时,Nrf2 转入细胞核并促进 SLC7A11 的产生——该转运蛋白负责输入合成谷胱甘肽的原料——以及 GPX4,即利用谷胱甘肽中和脂质过氧化物的酶。在类卒中条件下,SLC7A11 和 GPX4 水平降低,使细胞更容易发生铁死亡。普拉克索在蛋白和基因水平上显著提高了 Nrf2、SLC7A11 和 GPX4,同时抑制了可促使细胞进一步走向铁死亡与线粒体衰竭的 p53 蛋白。这些协调性的变化表明普拉克索增强了 Nrf2/SLC7A11/GPX4 轴,重建了细胞抗氧化盾,正是在最需要的部位发挥作用。
这对未来卒中治疗的意义
综合来看,这些发现表明普拉克索通过阻断铁死亡并维持线粒体功能,帮助神经细胞度过血流恢复后发生的氧化风暴。尽管该研究是在培养细胞中完成而非患者身上,但它指向了一种有前景的方式来重新定位现有的脑部药物用于卒中:不仅影响多巴胺信号传导,还可通过 Nrf2/SLC7A11/GPX4 通路稳定铁代谢和膜完整性。如果在动物模型和临床试验中能证实类似的保护作用,普拉克索或相关化合物有望未来被加入再灌注治疗,以减少缺血性卒中后持久的脑损伤。
引用: Zhang, L., Kang, X., Wang, Q. et al. Pramipexole alleviates ferroptosis in HT22 cells induced by oxygen–glucose deprivation/reoxygenation via the Nrf2/SLC7A11/GPX4 pathway. Sci Rep 16, 11134 (2026). https://doi.org/10.1038/s41598-026-40289-w
关键词: 缺血性卒中, 铁死亡, 普拉克索, 神经元保护, 氧化应激