Clear Sky Science · fr
Le pramipexole atténue la ferroptose dans les cellules HT22 induite par la privation/reoxygénation en oxygène–glucose via la voie Nrf2/SLC7A11/GPX4
Pourquoi protéger les cellules cérébrales après un AVC est important
Lorsqu’une personne subit un accident vasculaire cérébral ischémique, un caillot sanguin prive une portion du cerveau d’oxygène et de glucose. Les médecins s’efforcent de rouvrir rapidement le vaisseau obstrué, mais, paradoxalement, le retour brutal du flux sanguin peut lui‑même endommager des cellules cérébrales fragiles. Cette étude examine si le pramipexole, un médicament déjà utilisé dans la maladie de Parkinson, peut protéger les neurones contre cette seconde vague de lésions en calmant une forme récemment décrite de mort cellulaire liée au fer et à l’oxydation incontrôlée.
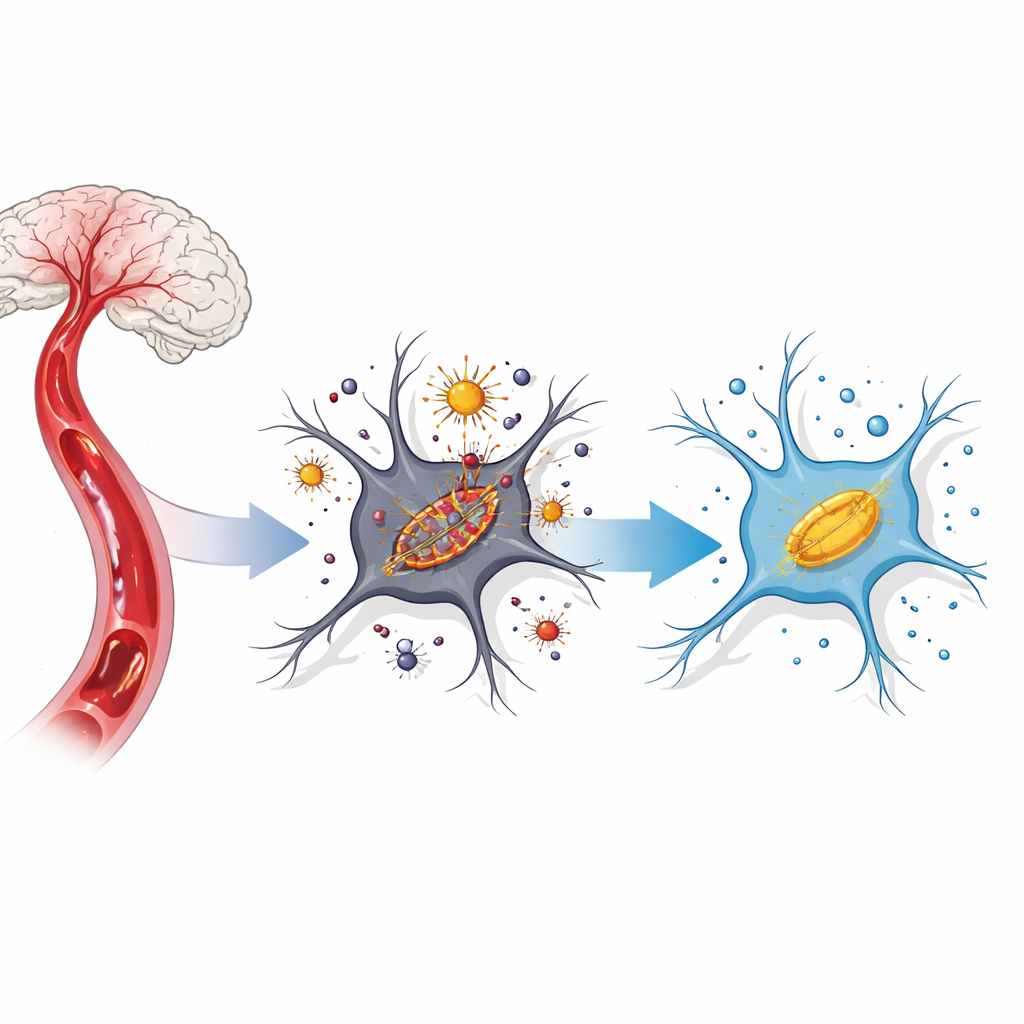
Une réaction en chaîne nocive à l’intérieur des cellules cérébrales
Après l’arrêt puis le rétablissement du flux sanguin, les cellules cérébrales subissent une tempête de stress chimique. Le fer, normalement confiné, se retrouve libre à l’intérieur de la cellule et réagit avec l’oxygène pour générer des molécules agressives appelées espèces réactives de l’oxygène. Celles‑ci attaquent les membranes cellulaires riches en lipides, en particulier dans les petites centrales énergétiques que sont les mitochondries. Les scientifiques désignent désormais cette mort cellulaire axée sur les membranes et pilotée par le fer comme la « ferroptose ». Dans les modèles d’AVC, la ferroptose apparaît lorsque le fer s’accumule, que les anti‑oxydants protecteurs diminuent et que les mitochondries deviennent rétrécies et dysfonctionnelles.
Tester le pramipexole dans un modèle de laboratoire imitant l’AVC
Pour reproduire ce qui se passe lors d’un AVC et du traitement qui suit, les chercheurs ont utilisé des cellules hippocampiques de souris (cellules HT22) et les ont temporairement privées d’oxygène et de glucose avant de rétablir des conditions normales. Ce modèle de privation/reoxygénation oxygène–glucose reproduit de nombreux aspects des lésions d’ischémie–reperfusion. L’équipe a exposé les cellules à différentes doses et calendriers de pramipexole et a mesuré la survie, la santé mitochondriale, les niveaux de fer, les espèces réactives de l’oxygène et les principaux systèmes antioxydants. Ils ont aussi utilisé l’erastine, un composé qui déclenche spécifiquement la ferroptose, pour vérifier si le pramipexole pouvait contrer directement ce processus.
Comment le médicament rétablit l’équilibre à l’intérieur des cellules
Sans protection, le traitement de type AVC a réduit la survie cellulaire, perturbé le potentiel de membrane mitochondrial, augmenté le fer et les espèces réactives de l’oxygène, et appauvri la molécule antioxydante glutathion ainsi que l’enzyme dépendante GPX4. Au microscope électronique, les mitochondries semblaient plus petites et plus denses, correspondant aux caractéristiques de la ferroptose. Le pramipexole, en particulier à une dose modérée administrée pendant la phase de reoxygénation, a inversé nombre de ces altérations : les cellules survivaient mieux, les mitochondries conservaient leur forme et leur charge électrique, le fer et les oxydants diminuaient, et l’activité du glutathion et de GPX4 rebondissait. Des bénéfices similaires ont été observés lorsque les cellules étaient lésées par l’erastine, renforçant l’idée que le pramipexole agit en limitant la ferroptose plutôt que seulement par une action antioxydante générale.
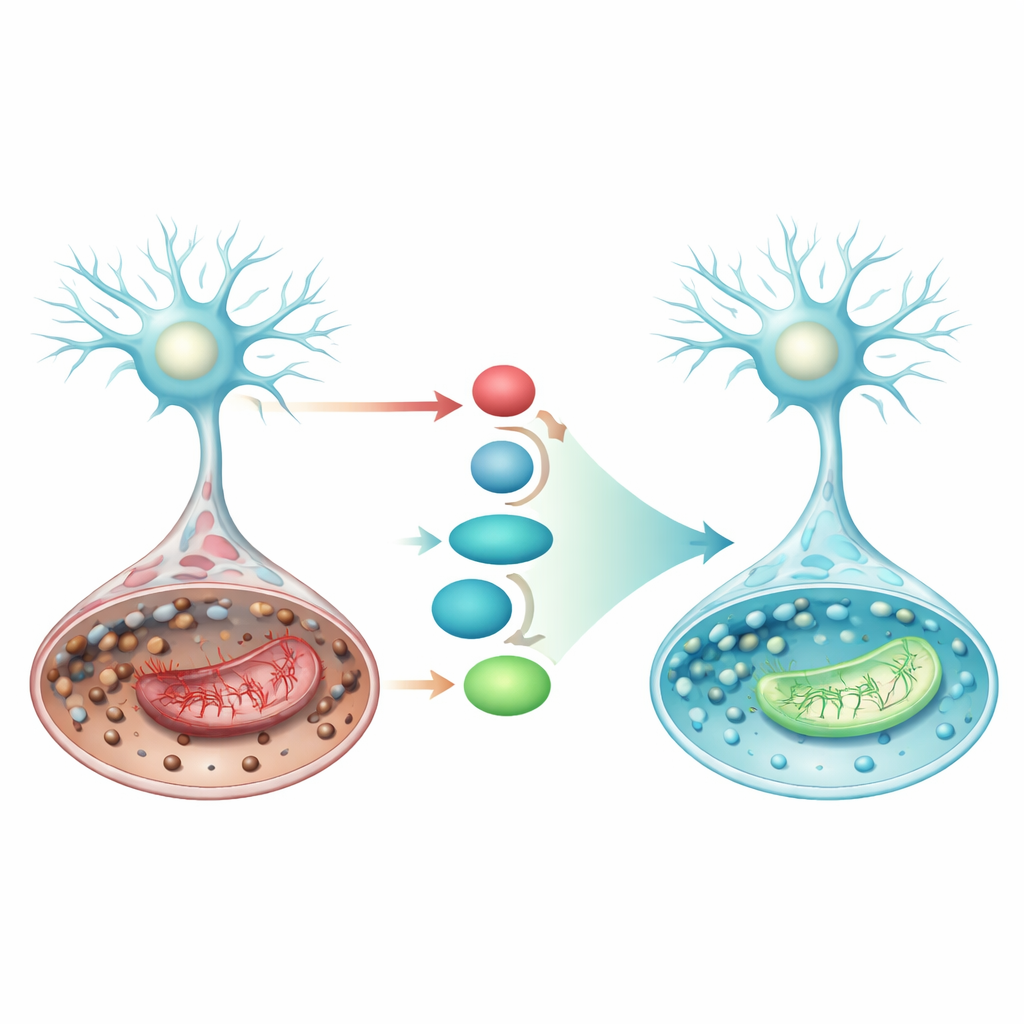
Activation d’une voie de défense interne
L’étude s’est aussi concentrée sur une ligne de défense cellulaire intrinsèque impliquant la protéine Nrf2 et ses partenaires en aval. Lorsqu’il est activé, Nrf2 migre dans le noyau et stimule la production de SLC7A11, un transporteur qui apporte la matière première pour le glutathion, et de GPX4, l’enzyme qui utilise le glutathion pour neutraliser les peroxydes lipidiques. Dans la condition de type AVC, les niveaux de SLC7A11 et de GPX4 chutaient, faisant basculer les cellules vers la ferroptose. Le pramipexole a fortement augmenté Nrf2, SLC7A11 et GPX4 aux niveaux protéique et génique et, simultanément, atténué p53, une protéine qui peut pousser les cellules vers la ferroptose et la défaillance mitochondriale. Ces changements coordonnés suggèrent que le pramipexole renforce l’axe Nrf2/SLC7A11/GPX4, reconstruisant le bouclier antioxydant de la cellule exactement là où il est le plus nécessaire.
Ce que cela pourrait signifier pour la prise en charge future des AVC
Pris ensemble, les résultats montrent que le pramipexole aide les neurones à traverser la tempête oxydative qui suit le rétablissement du flux sanguin, principalement en bloquant la ferroptose et en préservant la fonction mitochondriale. Bien que ce travail ait été réalisé sur des cultures cellulaires et non chez des patients, il indique une voie prometteuse pour réutiliser un médicament cérébral existant dans l’AVC : l’employer non seulement pour moduler la signalisation dopaminergique, mais aussi pour stabiliser la gestion du fer et l’intégrité des membranes via la voie Nrf2/SLC7A11/GPX4. Si une protection similaire est confirmée dans des modèles animaux et des essais cliniques, le pramipexole ou des composés apparentés pourraient un jour être ajoutés aux thérapies de reperfusion pour réduire les séquelles cérébrales durables après un infarctus cérébral ischémique.
Citation: Zhang, L., Kang, X., Wang, Q. et al. Pramipexole alleviates ferroptosis in HT22 cells induced by oxygen–glucose deprivation/reoxygenation via the Nrf2/SLC7A11/GPX4 pathway. Sci Rep 16, 11134 (2026). https://doi.org/10.1038/s41598-026-40289-w
Mots-clés: accident vasculaire ischémique, ferroptose, pramipexole, protection neuronale, stress oxydatif