Clear Sky Science · pt
Pramipexol alivia a ferroptose em células HT22 induzida por privação de oxigênio–glicose/reoxigenação via a via Nrf2/SLC7A11/GPX4
Por que proteger as células cerebrais após o AVC é importante
Quando uma pessoa tem um acidente vascular cerebral isquêmico, um coágulo sanguíneo priva parte do cérebro de oxigênio e glicose. Os médicos trabalham com urgência para reabrir o vaso bloqueado, mas, ironicamente, o retorno súbito do sangue pode por si só danificar células cerebrais frágeis. Este estudo investiga se o pramipexol, um fármaco já utilizado na doença de Parkinson, pode proteger os neurônios dessa segunda onda de dano ao moderar uma forma recentemente descrita de morte celular ligada ao ferro e à oxidação descontrolada.
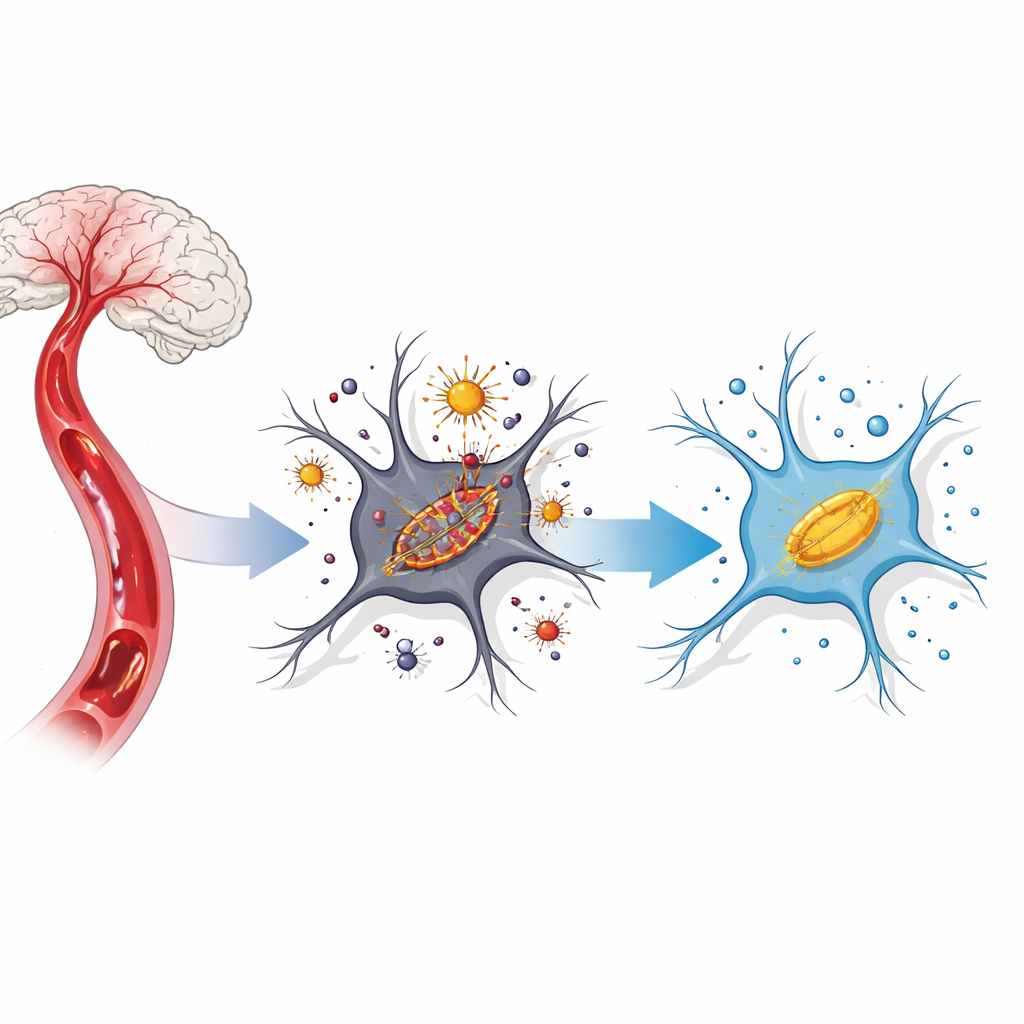
Uma reação em cadeia prejudicial dentro das células cerebrais
Após o corte e a restauração do fluxo sanguíneo, as células cerebrais enfrentam uma tempestade de estresse químico. O ferro que normalmente fica retido torna-se solto dentro da célula e reage com o oxigênio para gerar moléculas agressivas conhecidas como espécies reativas de oxigênio. Essas atacam as membranas celulares ricas em lipídios, especialmente em pequenas usinas chamadas mitocôndrias. Os cientistas agora chamam essa morte celular dirigida pelo ferro e focada nas membranas de “ferroptose”. Em modelos de AVC, a ferroptose aparece quando o ferro se acumula, os antioxidantes protetores caem e as mitocôndrias ficam encolhidas e disfuncionais.
Testando o pramipexol em um modelo de laboratório que imita AVC
Para simular o que acontece durante um AVC e o tratamento subsequente, os pesquisadores usaram células nervosas do hipocampo de camundongo (células HT22) e as privaram brevemente de oxigênio e glicose antes de restaurar as condições normais. Esse modelo de privação de oxigênio–glicose/reoxigenação reproduz muitas características da lesão por isquemia–reperfusão. A equipe expôs as células a diferentes doses e tempos de pramipexol e mediu sobrevivência, saúde mitocondrial, níveis de ferro, espécies reativas de oxigênio e sistemas antioxidantes chave. Eles também usaram erastina, um composto que desencadeia especificamente a ferroptose, para verificar se o pramipexol poderia contrariar esse processo diretamente.
Como a droga restaura o equilíbrio dentro das células
Sem proteção, o tratamento semelhante ao AVC reduziu a sobrevivência celular, perturbou o potencial de membrana mitocondrial, aumentou o ferro e as espécies reativas de oxigênio e esgotou a molécula antioxidante glutationa juntamente com a enzima GPX4 que dela depende. Ao microscópio eletrônico, as mitocôndrias pareciam menores e mais escuras, correspondendo a características da ferroptose. O pramipexol, particularmente em dose moderada administrada durante a fase de reoxigenação, reverteu muitas dessas alterações: as células sobreviveram melhor, as mitocôndrias mantiveram sua forma e carga elétrica, o ferro e os oxidantes diminuíram, e a glutationa e a atividade da GPX4 se recuperaram. Benefícios semelhantes foram observados quando as células foram danificadas pela erastina, reforçando a hipótese de que o pramipexol age reprimindo a ferroptose e não apenas por meio de uma antioxid ação geral.
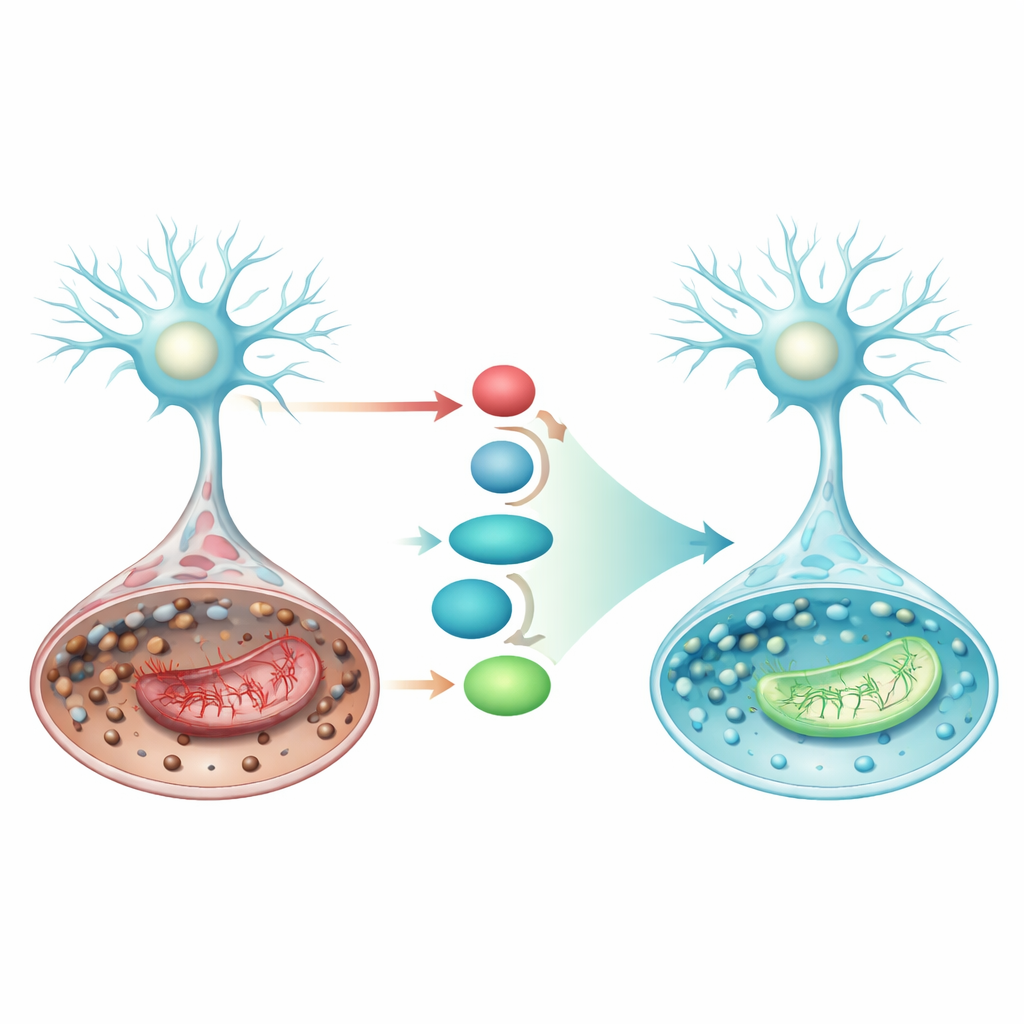
Ativando uma via de defesa interna
O estudo também se concentrou em uma linha de defesa celular embutida envolvendo a proteína Nrf2 e seus parceiros a jusante. Quando ativado, o Nrf2 se desloca para o núcleo celular e aumenta a produção de SLC7A11, um transportador que traz matéria-prima para a síntese de glutationa, e de GPX4, a enzima que usa a glutationa para neutralizar peróxidos lipídicos. Na condição semelhante ao AVC, os níveis de SLC7A11 e GPX4 caíram, inclinando as células para a ferroptose. O pramipexol aumentou fortemente Nrf2, SLC7A11 e GPX4 tanto nos níveis de proteína quanto de gene e, ao mesmo tempo, atenuou p53, uma proteína que pode empurrar as células ainda mais em direção à ferroptose e à falha mitocondrial. Essas mudanças coordenadas sugerem que o pramipexol fortalece o eixo Nrf2/SLC7A11/GPX4, reconstruindo o escudo antioxidante da célula exatamente onde ele é mais necessário.
O que isso pode significar para o cuidado do AVC no futuro
Em conjunto, os achados mostram que o pramipexol ajuda os neurônios a resistir à tempestade oxidativa que segue o restabelecimento do fluxo sanguíneo, principalmente ao bloquear a ferroptose e preservar a função mitocondrial. Embora esse trabalho tenha sido realizado em células em cultura e não em pacientes, aponta para uma nova e promissora maneira de reposicionar um fármaco cerebral existente para o AVC: usá‑lo não apenas para modular a sinalização dopaminérgica, mas para estabilizar o manejo do ferro e a integridade das membranas por meio da via Nrf2/SLC7A11/GPX4. Se proteção semelhante for confirmada em modelos animais e em ensaios clínicos, o pramipexol ou compostos relacionados podem um dia ser adicionados às terapias de reperfusão para reduzir os danos cerebrais duradouros após acidente vascular cerebral isquêmico.
Citação: Zhang, L., Kang, X., Wang, Q. et al. Pramipexole alleviates ferroptosis in HT22 cells induced by oxygen–glucose deprivation/reoxygenation via the Nrf2/SLC7A11/GPX4 pathway. Sci Rep 16, 11134 (2026). https://doi.org/10.1038/s41598-026-40289-w
Palavras-chave: acidente vascular cerebral isquêmico, ferroptose, pramipexol, proteção neuronal, estresse oxidativo