Clear Sky Science · sv
Pramipexole lindrar ferroptos i HT22‑celler inducerad av syre‑glukos‑deprivation/reioksygenering via Nrf2/SLC7A11/GPX4‑vägen
Varför det är viktigt att skydda hjärnceller efter stroke
När en person drabbas av ischemisk stroke så hindrar en blodpropp en del av hjärnan från att få syre och glukos. Läkare arbetar snabbt för att öppna upp det blockerade kärlet, men ironiskt nog kan den plötsliga återflödet av blod i sig skada känsliga hjärnceller. Denna studie undersöker om pramipexol, ett läkemedel som redan används vid Parkinsons sjukdom, kan skydda nervceller från denna andra våg av skada genom att dämpa en nyupptäckt form av celldöd kopplad till järn och okontrollerad oxidation.
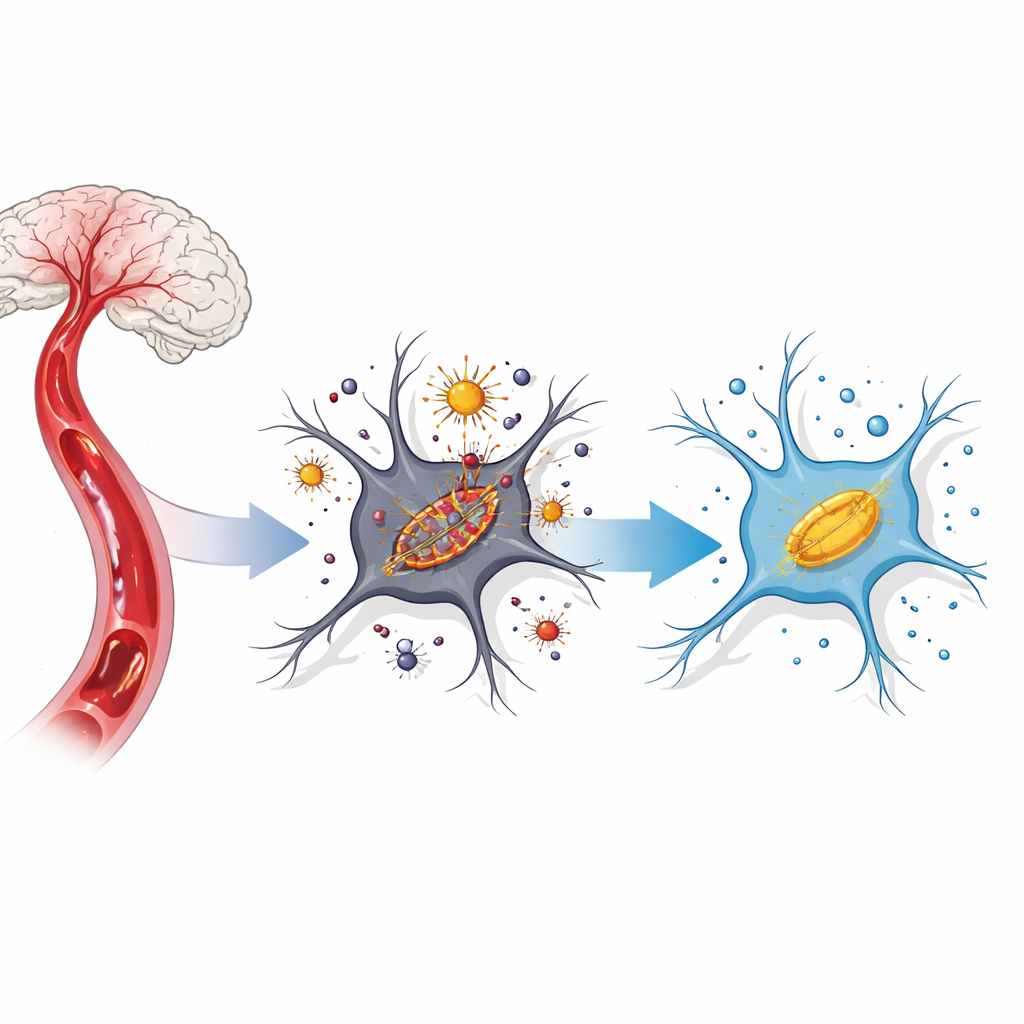
En skadlig kedjereaktion inne i hjärnceller
Efter att blodflödet avbryts och sedan återställs drabbas hjärnceller av en kemisk stressstorm. Järn som normalt är inlåst blir löst inne i cellen och reagerar med syre för att bilda aggressiva molekyler som kallas reaktiva syrearter. Dessa angriper cellmembran rika på lipider, särskilt i de små kraftverken som kallas mitokondrier. Forskare kallar nu denna järndrivna, membranfokuserade celldöd för “ferroptos.” I strokemodeller framträder ferroptos när järn ansamlas, skyddande antioxidanter sjunker och mitokondrier krymper och blir dysfunktionella.
Test av pramipexol i en strokeliknande labbmodell
För att efterlikna vad som händer under en stroke och efterföljande behandling använde forskarna musens hippocampala nervceller (HT22‑celler) och berövade dem kortvarigt både syre och glukos innan de återställde normala förhållanden. Denna syre‑glukos‑deprivation/reioksygenerings‑modell reproducerar många drag av ischemireperfusionsskada. Teamet utsatte cellerna för olika doser och tidpunkter av pramipexol och mätte överlevnad, mitokondriell hälsa, järnnivåer, reaktiva syrearter och centrala antioxidantsystem. De använde också erastin, ett kemiskt ämne som specifikt utlöser ferroptos, för att se om pramipexol direkt kunde motverka denna process.
Hur läkemedlet återställer balans inne i cellerna
Utan skydd minskade cellöverlevnaden av den strokeliknande behandlingen, mitokondriernas membranpotential stördes, järn och reaktiva syrearter ökade och antioxidantmolekylen glutation samt det glutation‑beroende enzymet GPX4 tömdes ut. Under elektronmikroskopet såg mitokondrierna mindre och mörkare ut, i överensstämmelse med kännetecken för ferroptos. Pramipexol, särskilt i en måttlig dos given under reioksygeneringsfasen, vände många av dessa förändringar: cellerna överlevde bättre, mitokondrierna behöll sin form och elektriska potential, järn och oxidanter minskade, och glutation samt GPX4‑aktivitet återhämtade sig. Liknande fördelar sågs när cellerna skadades av erastin, vilket stärker uppfattningen att pramipexol verkar genom att hämma ferroptos snarare än enbart genom generell antioxidation.
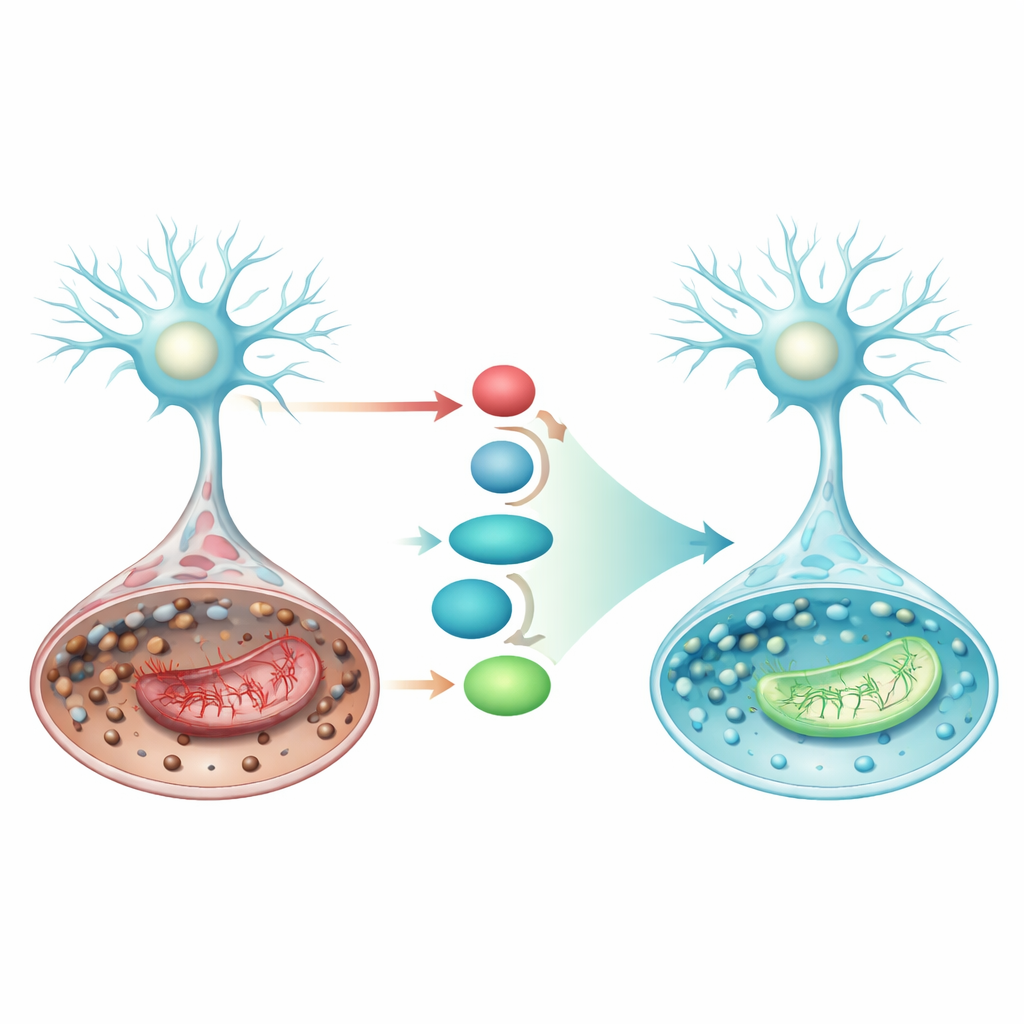
Aktivering av en intern försvarsväg
Studien fokuserade också på en inbyggd cellulär försvarslinje som involverar proteinet Nrf2 och dess nedströms partners. När Nrf2 aktiveras flyttar det in i cellkärnan och ökar produktionen av SLC7A11, en transportör som för in byggstenar för glutation, och GPX4, enzymet som använder glutation för att neutralisera lipidperoxider. Under den strokeliknande situationen sjönk nivåerna av SLC7A11 och GPX4, vilket lutade cellerna mot ferroptos. Pramipexol ökade kraftigt nivåerna av Nrf2, SLC7A11 och GPX4 på både protein‑ och genivå och dämpade samtidigt p53, ett protein som kan driva celler vidare mot ferroptos och mitokondriell kollaps. Dessa samordnade förändringar tyder på att pramipexol stärker Nrf2/SLC7A11/GPX4‑axeln och återskapar cellens antioxidantskydd precis där det behövs mest.
Vad detta kan innebära för framtida strokebehandling
Sammantaget visar fynden att pramipexol hjälper nervceller att klara av den oxidativa storm som följer när blodflödet återställs, främst genom att blockera ferroptos och bevara mitokondriernas funktion. Även om detta arbete utfördes i odlade celler snarare än hos patienter pekar det mot ett lovande nytt sätt att återanvända ett befintligt hjärnläkemedel för stroke: att använda det inte bara för att påverka dopaminsignalering, utan för att stabilisera järnhantering och membranintegritet via Nrf2/SLC7A11/GPX4‑vägen. Om liknande skydd kan bekräftas i djurmodeller och kliniska prövningar kan pramipexol eller besläktade föreningar en dag läggas till reperfusionsbehandlingar för att minska bestående hjärnskador efter ischemisk stroke.
Citering: Zhang, L., Kang, X., Wang, Q. et al. Pramipexole alleviates ferroptosis in HT22 cells induced by oxygen–glucose deprivation/reoxygenation via the Nrf2/SLC7A11/GPX4 pathway. Sci Rep 16, 11134 (2026). https://doi.org/10.1038/s41598-026-40289-w
Nyckelord: ischemisk stroke, ferroptos, pramipexol, neuronalt skydd, oxidativ stress