Clear Sky Science · de
Pramipexol lindert Ferroptose in HT22-Zellen, die durch Sauerstoff‑ und Glukoseentzug/Reoxygenierung induziert wird, über den Nrf2/SLC7A11/GPX4-Weg
Warum der Schutz von Gehirnzellen nach einem Schlaganfall wichtig ist
Bei einem ischämischen Schlaganfall entzündet ein Blutgerinnsel einen Teil des Gehirns an Sauerstoff und Zucker. Ärzte arbeiten dringend daran, das verschlossene Gefäß wieder zu öffnen, doch ironischerweise kann die plötzliche Rückkehr des Blutes selbst empfindliche Gehirnzellen schädigen. Diese Studie untersucht, ob Pramipexol, ein bereits bei der Parkinson‑Krankheit eingesetztes Medikament, Nervenzellen vor dieser zweiten Schadenswelle schützen kann, indem es eine kürzlich beschriebene Form des Zelltods beruhigt, die mit Eisen und unkontrollierter Oxidation verbunden ist.
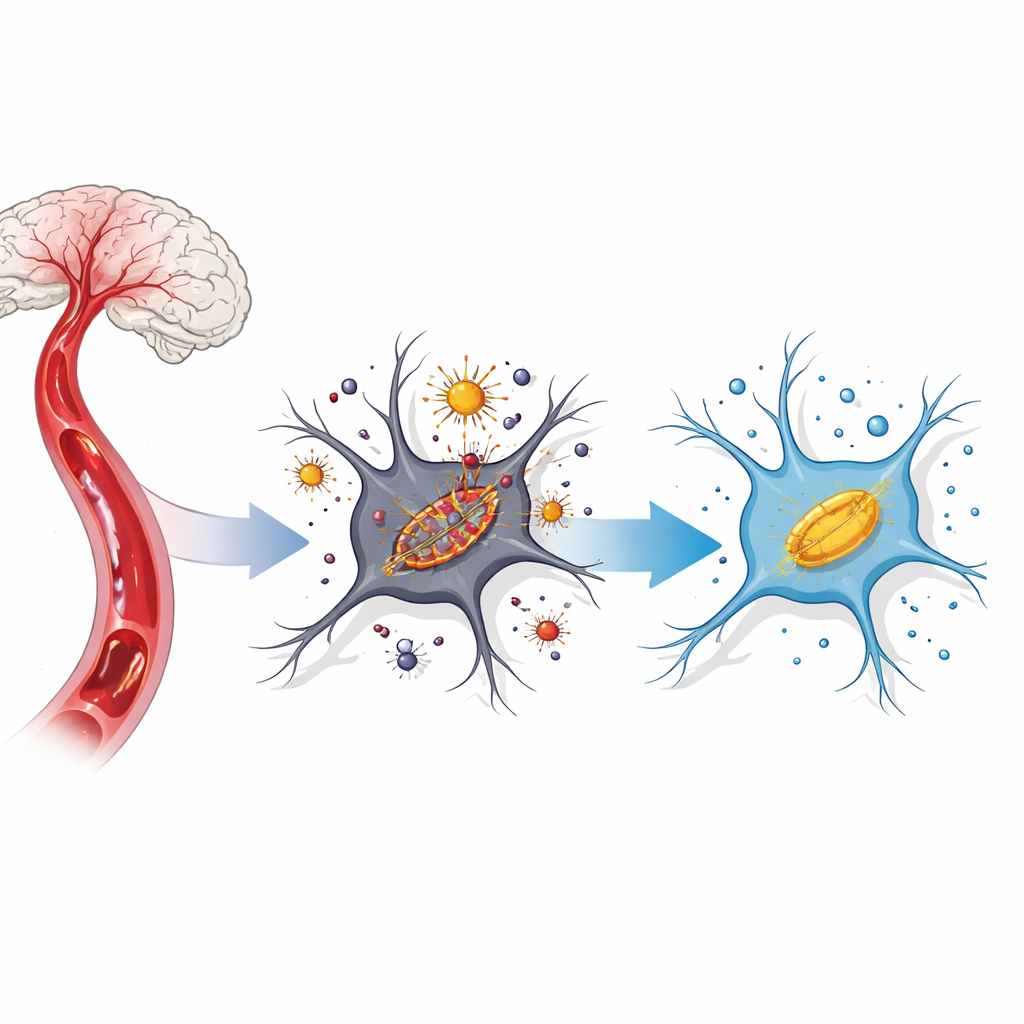
Eine schädliche Kettenreaktion in Gehirnzellen
Nachdem der Blutfluss unterbrochen und dann wiederhergestellt wurde, erleben Gehirnzellen einen Sturm chemischer Belastungen. Eisen, das normalerweise gebunden ist, wird innerhalb der Zelle mobil und reagiert mit Sauerstoff, wobei aggressive Verbindungen entstehen, die als reaktive Sauerstoffspezies bezeichnet werden. Diese greifen membranreiche Zellstrukturen an, vor allem in winzigen Kraftwerken, den Mitochondrien. Wissenschaftler bezeichnen diesen eisengetriebenen, membranfokussierten Zelltod inzwischen als „Ferroptose“. In Schlaganfall‑Modellen tritt Ferroptose auf, wenn Eisen akkumuliert, schützende Antioxidantien abnehmen und Mitochondrien geschrumpft und funktionsgestört erscheinen.
Pramipexol in einem stroke‑ähnlichen Labor‑Modell testen
Um das Geschehen während eines Schlaganfalls und der anschließenden Behandlung zu simulieren, verwendeten die Forscher hippocampale Mausnervenzellen (HT22‑Zellen) und entzogen ihnen kurzzeitig sowohl Sauerstoff als auch Glukose, bevor sie die normalen Bedingungen wiederherstellten. Dieses Modell des Sauerstoff‑ und Glukoseentzugs/Reoxygenierung bildet viele Merkmale der Ischämie‑Reperfusions‑Schädigung nach. Das Team setzte die Zellen unterschiedlichen Dosen und Zeitpunkten von Pramipexol aus und ermittelte Überleben, mitochondriale Gesundheit, Eisenwerte, reaktive Sauerstoffspezies und wesentliche antioxidative Systeme. Außerdem nutzten sie Erastin, eine Chemikalie, die gezielt Ferroptose auslöst, um zu prüfen, ob Pramipexol diesen Prozess direkt entgegenwirken kann.
Wie das Medikament das Gleichgewicht in der Zelle wiederherstellt
Ohne Schutz verringerte die stroke‑ähnliche Behandlung das Zellüberleben, störte das mitochondriale Membranpotenzial, erhöhte Eisen und reaktive Sauerstoffspezies und erschöpfte das Antioxidans Glutathion sowie das darauf angewiesene Enzym GPX4. Unter dem Elektronenmikroskop erschienen die Mitochondrien kleiner und dunkler, was den Kennzeichen der Ferroptose entsprach. Pramipexol, besonders in moderater Dosis während der Reoxygenierungsphase verabreicht, kehrte viele dieser Veränderungen um: Die Zellen überlebten besser, die Mitochondrien behielten Form und Membranladung, Eisen und Oxidantien gingen zurück, und Glutathion sowie die GPX4‑Aktivität erholten sich. Ähnliche Vorteile zeigten sich auch, wenn die Zellen durch Erastin geschädigt wurden, was die Annahme stützt, dass Pramipexol Ferroptose gezielt hemmt und nicht nur allgemein antioxidativ wirkt.
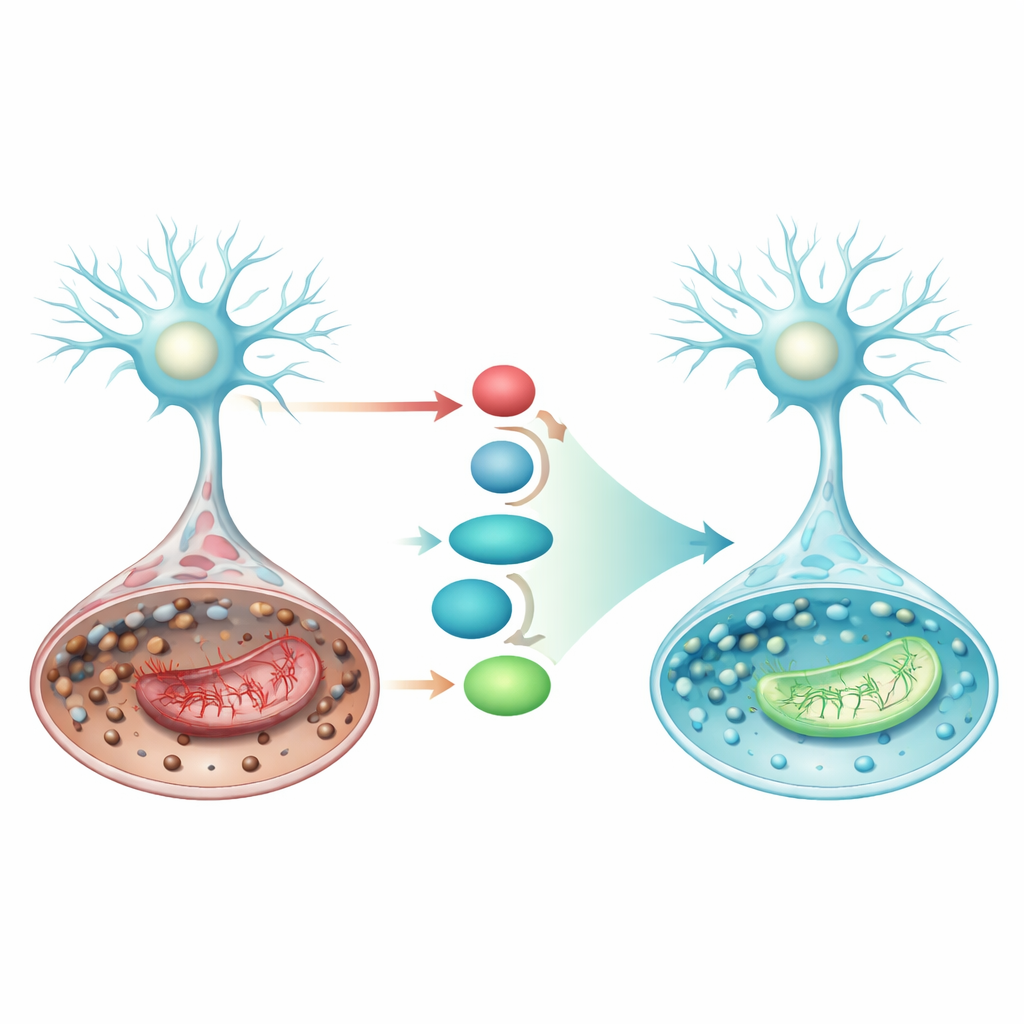
Aktivierung eines inneren Abwehrwegs
Die Studie untersuchte zudem eine eingebaute zelluläre Verteidigungslinie rund um das Protein Nrf2 und dessen nachgeschaltete Partner. Bei Aktivierung wandert Nrf2 in den Zellkern und steigert die Produktion von SLC7A11, einem Transporter, der Bausteine für Glutathion aufnimmt, sowie von GPX4, dem Enzym, das Glutathion nutzt, um Lipidperoxide zu neutralisieren. Unter den stroke‑ähnlichen Bedingungen fielen SLC7A11‑ und GPX4‑Spiegel, wodurch die Zellen in Richtung Ferroptose kippten. Pramipexol erhöhte Nrf2, SLC7A11 und GPX4 sowohl auf Protein‑ als auch auf Genebene deutlich und dämpfte gleichzeitig p53, ein Protein, das Zellen weiter in Richtung Ferroptose und mitochondrialem Versagen treiben kann. Diese koordinierten Veränderungen deuten darauf hin, dass Pramipexol die Nrf2/SLC7A11/GPX4‑Achse stärkt und den antioxidativen Schutz der Zelle genau dort wiederaufbaut, wo er am dringendsten benötigt wird.
Was das für die künftige Schlaganfallversorgung bedeuten könnte
Insgesamt zeigen die Ergebnisse, dass Pramipexol Nervenzellen hilft, den oxidativen Sturm nach der Wiederherstellung des Blutflusses zu überstehen, vor allem indem es Ferroptose blockiert und die Mitochondrienfunktion bewahrt. Obwohl diese Arbeit an kultivierten Zellen und nicht an Patienten durchgeführt wurde, weist sie auf einen vielversprechenden neuen Weg hin, ein vorhandenes Zentralnervensystem‑Medikament für den Schlaganfall umzunutzen: Es nicht nur zur Beeinflussung der Dopamin‑Signalgebung zu verwenden, sondern um den Umgang mit Eisen und die Membranintegrität über den Nrf2/SLC7A11/GPX4‑Weg zu stabilisieren. Bestätigen Tiermodelle und klinische Studien einen ähnlichen Schutz, könnten Pramipexol oder verwandte Verbindungen eines Tages den Reperfusionsbehandlungen hinzugefügt werden, um bleibende Hirnschäden nach ischämischem Schlaganfall zu verringern.
Zitation: Zhang, L., Kang, X., Wang, Q. et al. Pramipexole alleviates ferroptosis in HT22 cells induced by oxygen–glucose deprivation/reoxygenation via the Nrf2/SLC7A11/GPX4 pathway. Sci Rep 16, 11134 (2026). https://doi.org/10.1038/s41598-026-40289-w
Schlüsselwörter: ischämischer Schlaganfall, Ferroptose, Pramipexol, neuronalem Schutz, oxidativer Stress