Clear Sky Science · nl
Pramipexole verlicht ferroptose in HT22-cellen geïnduceerd door zuurstof‑glucose‑deprivatie/reoxygenatie via de Nrf2/SLC7A11/GPX4-route
Waarom het beschermen van hersencellen na een beroerte ertoe doet
Wanneer iemand een ischemische beroerte krijgt, onttrekt een bloedstolsel een deel van de hersenen van zuurstof en suiker. Artsen proberen snel het geblokkeerde vat te openen, maar ironisch genoeg kan de plotselinge terugkeer van bloed juist kwetsbare hersencellen beschadigen. Deze studie onderzoekt of pramipexole, een geneesmiddel dat al wordt gebruikt bij de ziekte van Parkinson, zenuwcellen kan beschermen tegen deze tweede schadegolf door een recent ontdekte vorm van celdood die met ijzer en ongebreidelde oxidatie te maken heeft te dempen.
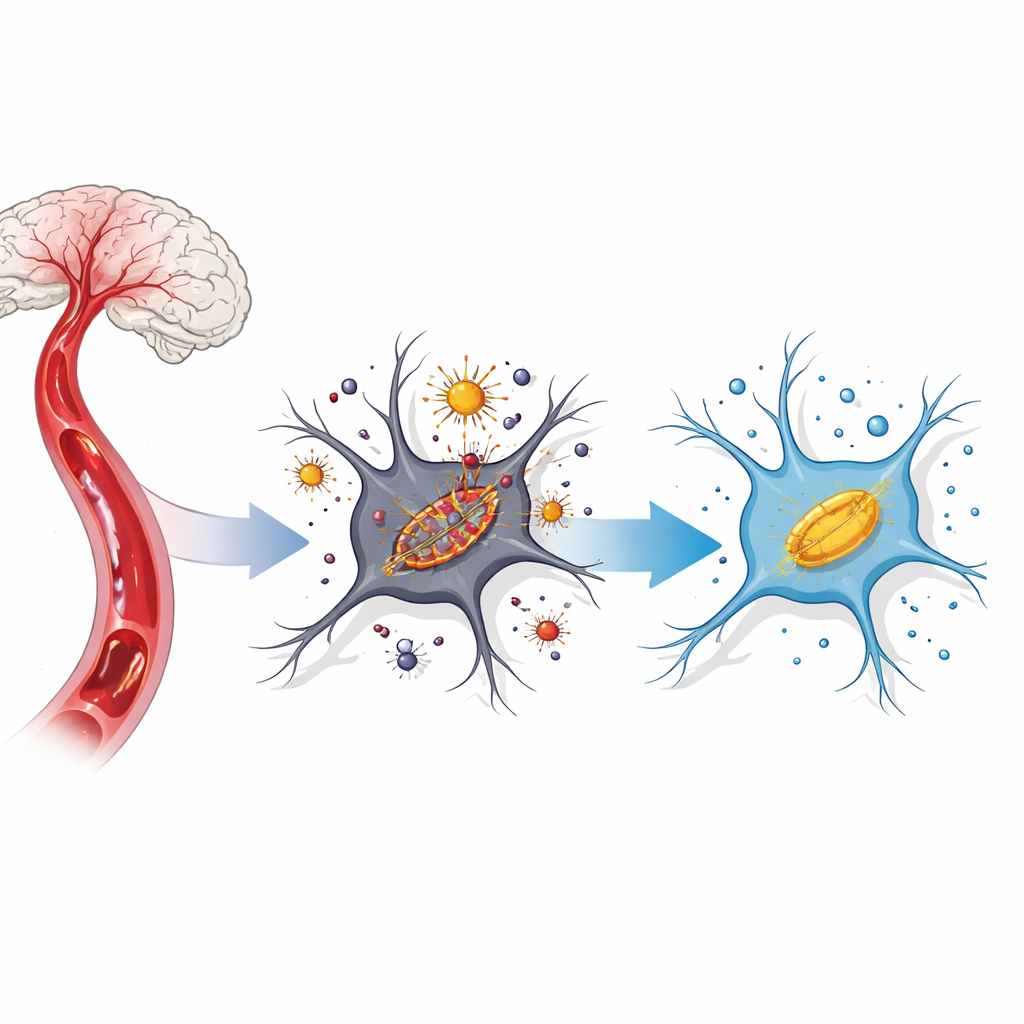
Een schadelijke kettingreactie in hersencellen
Nadat de bloedstroom is afgesneden en vervolgens weer is hersteld, ondervinden hersencellen een storm van chemische stress. IJzer dat normaal gebonden is raakt vrij in de cel en reageert met zuurstof om agressieve moleculen te vormen die reactieve zuurstofsoorten worden genoemd. Deze vallen celmembranen aan die rijk zijn aan vetten, vooral in de kleine energiecentrales genaamd mitochondriën. Wetenschappers noemen deze door ijzer aangedreven, membraangerichte celdood nu “ferroptose.” In beroertemodellen verschijnt ferroptose wanneer ijzer zich ophoopt, beschermende antioxidanten afnemen en mitochondriën verschrompeld en disfunctioneel worden.
Pramipexole testen in een beroerte‑achtig laboratoriummodel
Om na te bootsen wat er gebeurt tijdens een beroerte en de daaropvolgende behandeling, gebruikten de onderzoekers muizengeheuapse hippocampuscellen (HT22-cellen) en onthielden ze tijdelijk zowel zuurstof als glucose voordat ze de normale omstandigheden herstelden. Dit model van zuurstof‑glucose‑deprivatie/reoxygenatie reproduceert veel kenmerken van ischemie‑reperfusieschade. Het team stelde cellen bloot aan verschillende doseringen en tijdstippen van pramipexole en mat overleving, mitochondriale gezondheid, ijzergehalte, reactieve zuurstofsoorten en sleutelantioxidantsystemen. Ze gebruikten ook erastine, een chemische stof die specifiek ferroptose triggert, om te onderzoeken of pramipexole dit proces rechtstreeks kon tegengaan.
Hoe het middel het evenwicht in de cel herstelt
Zonder bescherming verminderde de beroerte‑achtige behandeling de celoverleving, verstoorde het mitochondriale membraanpotentieel, verhoogde het ijzer en reactieve zuurstofsoorten en putte het de antioxidant glutathion en het op dit molecuul afhankelijke enzym GPX4 uit. Onder de elektronenmicroscoop leken mitochondriën kleiner en donkerder, overeenkomend met kenmerken van ferroptose. Pramipexole, met name bij een matige dosis toegediend tijdens de reoxygenatiefase, keerde veel van deze veranderingen om: cellen overleefden beter, mitochondriën behielden hun vorm en elektrische lading, ijzer en oxidanten daalden, en glutathion en GPX4‑activiteit herstelden zich. Vergelijkbare voordelen werden gezien wanneer cellen werden beschadigd door erastine, wat het idee versterkt dat pramipexole werkt door ferroptose te onderdrukken in plaats van alleen via algemene antioxidatie.
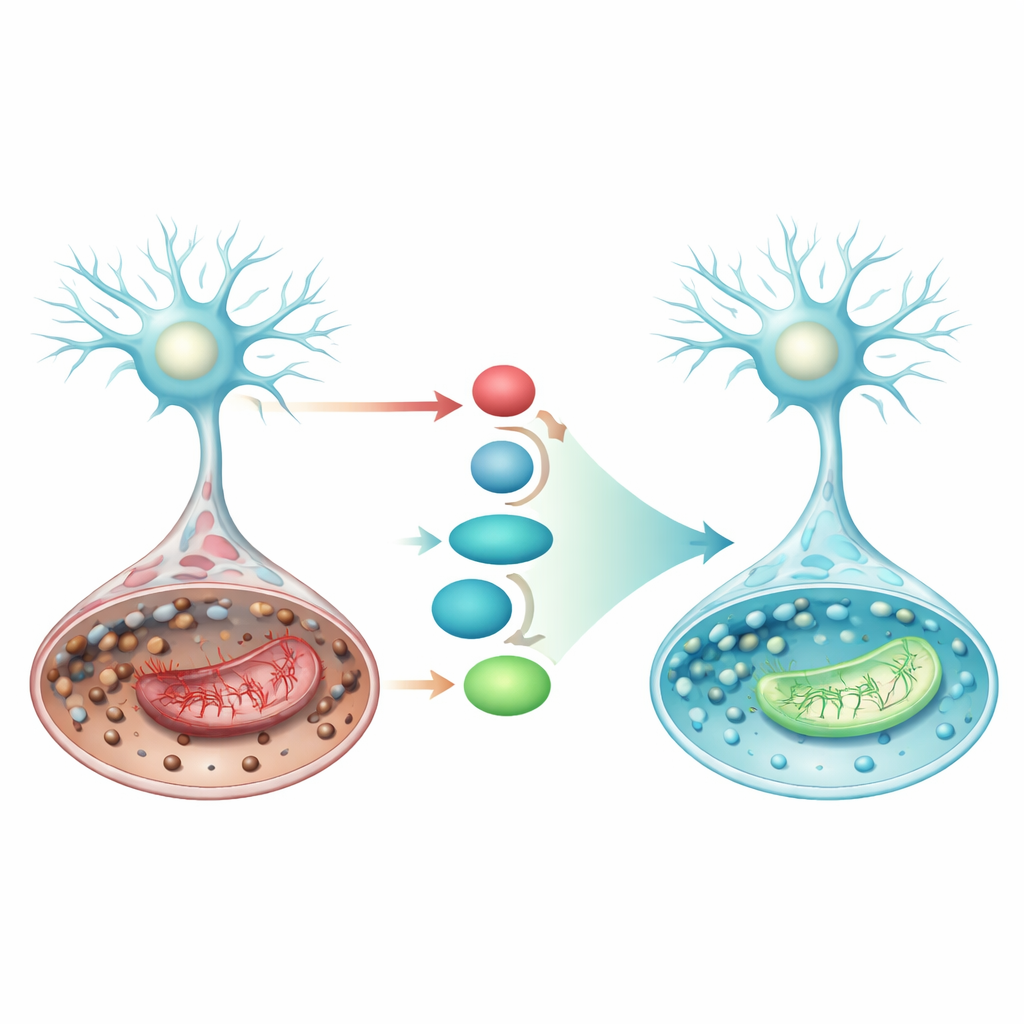
Het inschakelen van een interne verdedigingsroute
De studie richtte zich ook op een ingebouwde cellulaire verdedigingslijn met het eiwit Nrf2 en zijn downstreampartners. Wanneer geactiveerd, verhuist Nrf2 naar de celkern en bevordert het de productie van SLC7A11, een transporter die grondstoffen voor glutathion binnenbrengt, en GPX4, het enzym dat glutathion gebruikt om lipideperoxiden te neutraliseren. In de beroerte‑achtige condities daalden SLC7A11‑ en GPX4‑niveaus, waardoor cellen meer richting ferroptose neigden. Pramipexole verhoogde sterk Nrf2, SLC7A11 en GPX4 op zowel eiwit‑ als geniveau en dempte tegelijkertijd p53, een eiwit dat cellen verder richting ferroptose en mitochondriale uitval kan duwen. Deze gecoördineerde verschuivingen suggereren dat pramipexole de Nrf2/SLC7A11/GPX4‑as versterkt en het antioxidantenscherm van de cel precies daar herstelt waar het het meest nodig is.
Wat dit kan betekenen voor toekomstige beroertezorg
Alles bij elkaar laten de bevindingen zien dat pramipexole zenuwcellen helpt de oxidatieve storm na herstel van de bloedstroom te doorstaan, vooral door ferroptose te blokkeren en mitochondriale functie te behouden. Hoewel dit werk in gekweekte cellen en niet in patiënten is uitgevoerd, wijst het op een veelbelovende manier om een bestaand hersengeneesmiddel te herbestemmen voor beroerte: niet alleen om dopamine‑signaalgeving te beïnvloeden, maar om ijzerhuishouding en membraanintegriteit te stabiliseren via de Nrf2/SLC7A11/GPX4‑route. Als vergelijkbare bescherming kan worden bevestigd in diermodellen en klinische trials, zouden pramipexole of verwante verbindingen mogelijk op termijn kunnen worden toegevoegd aan reperfusietherapieën om blijvende hersenschade na ischemische beroerte te verminderen.
Bronvermelding: Zhang, L., Kang, X., Wang, Q. et al. Pramipexole alleviates ferroptosis in HT22 cells induced by oxygen–glucose deprivation/reoxygenation via the Nrf2/SLC7A11/GPX4 pathway. Sci Rep 16, 11134 (2026). https://doi.org/10.1038/s41598-026-40289-w
Trefwoorden: ischemische beroerte, ferroptose, pramipexole, neurale bescherming, oxiderende stress