Clear Sky Science · tr
Pramipeksol, oksijen–glukoz yokluğu/yeniden oksijenlenme ile indüklenen HT22 hücrelerindeki ferroptozisi Nrf2/SLC7A11/GPX4 yolu aracılığıyla hafifletir
Neden inmeden sonra beyin hücrelerini korumak önemli?
Bir kişide iskemik inme olduğunda, bir kan pıhtısı beynin bir bölümünü oksijen ve glikozdan mahrum bırakır. Hekimler tıkalı damarı acilen açmaya çalışır, ancak ironik olarak kanın ani geri dönüşü hassas beyin hücrelerine zarar verebilir. Bu çalışma, Parkinson hastalığında zaten kullanılan bir ilaç olan pramipeksolün, demir ve kontrolsüz oksidasyonla ilişkili yeni tanımlanmış bir hücre ölümü biçimini yatıştırarak sinir hücrelerini bu ikinci dalga zarardan koruyup koruyamayacağını araştırıyor.
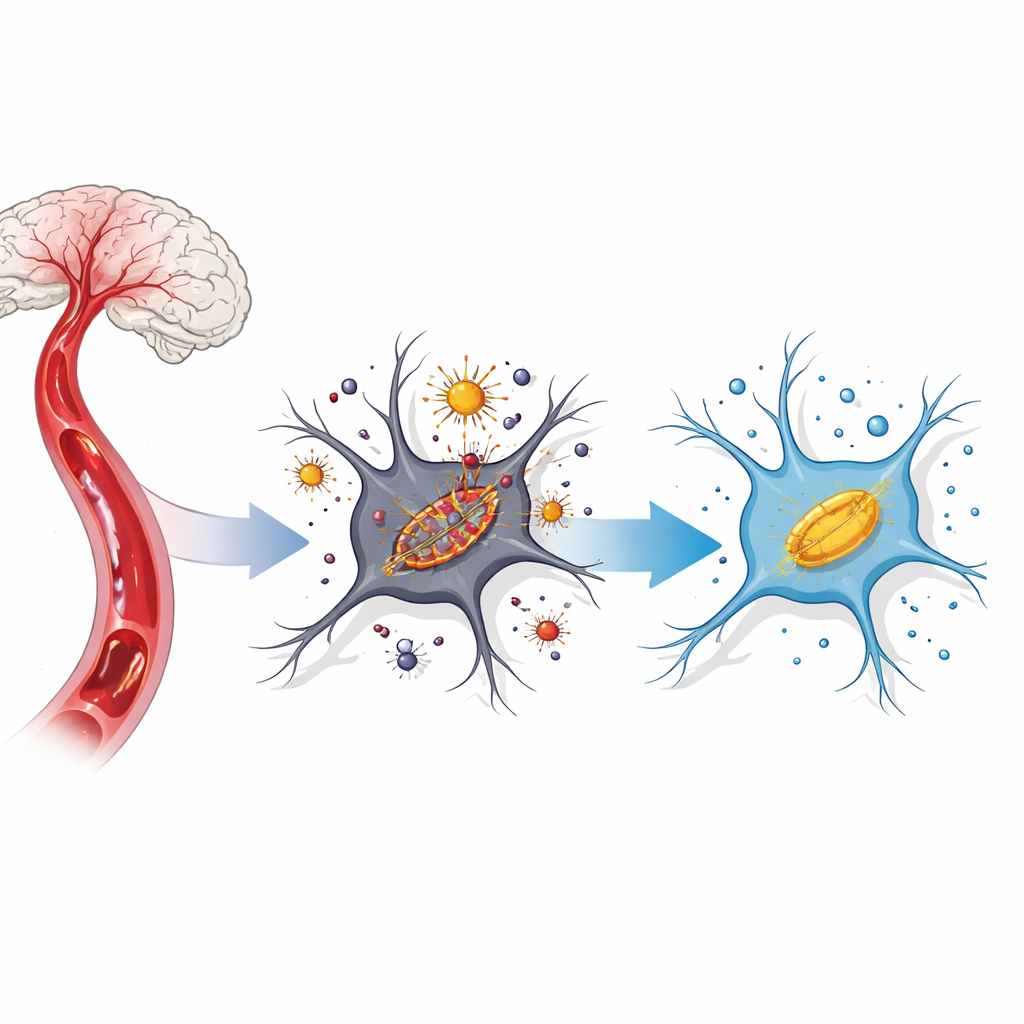
Beyin hücreleri içinde zararlı bir zincirleme reaksiyon
Kan akışı kesilip sonra yeniden sağlandığında, beyin hücreleri kimyasal bir stres fırtınası yaşar. Normalde kilitli olan demir hücre içinde serbestleşir ve oksijenle reaksiyona girerek reaktif oksijen türleri olarak bilinen saldırgan moleküller üretir. Bunlar, özellikle mitokondri adı verilen küçük enerji santrallerinde yağ açısından zengin hücre zarlarına saldırır. Bilim insanları artık bu demir kaynaklı, zar odaklı hücre ölümüne “ferroptozis” adını veriyor. İnme modellerinde ferroptozis, demir birikimi arttığında, koruyucu antioksidanlar düştüğünde ve mitokondriler küçülmüş ve işlevsiz hale geldiğinde ortaya çıkıyor.
İnme benzeri bir laboratuvar modelinde pramipeksolün testi
İnmeye ve sonrasındaki tedaviye benzer koşulları taklit etmek için araştırmacılar fare hippocampusundan elde edilen sinir hücreleri (HT22 hücreleri) kullandı ve bunları kısa süreliğine oksijen ve glikozdan yoksun bıraktıktan sonra normal koşullara döndürdü. Bu oksijen–glukoz yokluğu/yeniden oksijenlenme modeli iskemik–reperfüzyon hasarının birçok özelliğini yeniden üretir. Ekip hücreleri farklı doz ve zamanlamalarda pramipeksole maruz bırakarak hayatta kalma, mitokondriyal sağlık, demir düzeyleri, reaktif oksijen türleri ve temel antioksidan sistemleri ölçtü. Ayrıca pramipeksolün bu süreci doğrudan karşılayıp karşılayamayacağını görmek için spesifik olarak ferroptozisi tetikleyen bir kimyasal olan erastini de kullandılar.
İlaç hücre içindeki dengeyi nasıl yeniden kuruyor
Koruma olmadan, inme benzeri işlem hücre hayatta kalmasını azalttı, mitokondriyal membran potansiyelini bozdu, demir ve reaktif oksijen türlerini artırdı ve glutatyon ile buna bağlı enzim GPX4’ü tüketti. Elektron mikroskobunda mitokondriler daha küçük ve daha koyu görünerek ferroptozisin ayırt edici özellikleriyle uyum gösterdi. Pramipeksol, özellikle yeniden oksijenlenme aşamasında verilen orta dozda, bu değişikliklerin birçoğunu geri çevirdi: hücreler daha iyi hayatta kaldı, mitokondriler şekil ve elektriksel potansiyelini korudu, demir ve oksidanlar azaldı ve glutatyon ile GPX4 aktivitesi toparlandı. Hücrelere erastinle zarar verildiğinde benzer faydaların görülmesi, pramipeksolün yalnızca genel bir antioksidan etkiden ziyade ferroptozisi engelleyerek hareket ettiğine dair kanıtları güçlendiriyor.
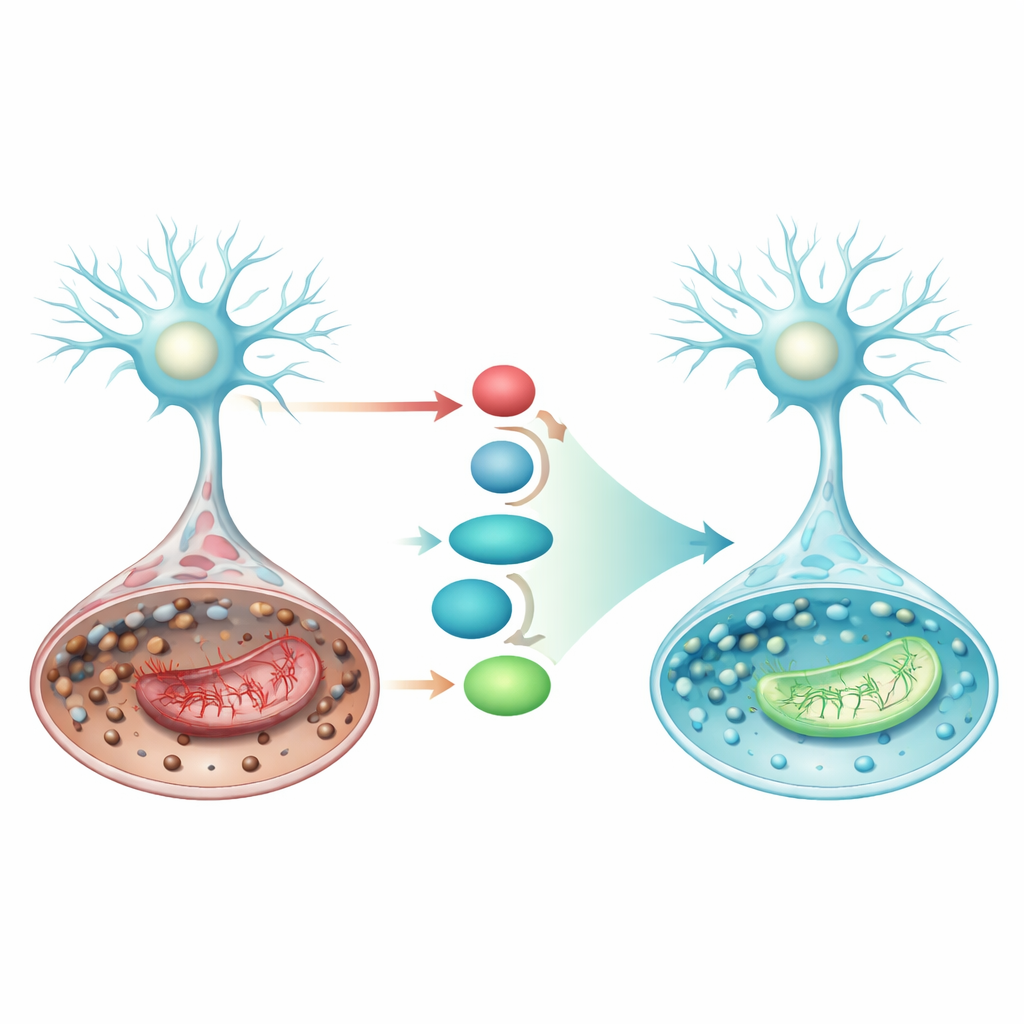
Hücresel iç savunma yolunu açmak
Çalışma ayrıca Nrf2 proteini ve onun aşağı akış ortaklarını içeren yerleşik bir hücresel savunma hattına odaklandı. Aktive olduğunda Nrf2 hücre çekirdeğine geçer ve glutatyon için hammadde taşıyan SLC7A11 transporteri ile glutatyonu kullanarak lipit peroksitleri nötralize eden enzim GPX4’ün üretimini artırır. İnme benzeri koşulda SLC7A11 ve GPX4 düzeyleri düşerek hücreleri ferroptozise doğru eğdi. Pramipeksol, hem protein hem de gen düzeyinde Nrf2, SLC7A11 ve GPX4’ü güçlü biçimde yükseltti ve aynı zamanda hücreleri ferroptozise ve mitokondriyal çöküşe daha da itebilen p53 proteinini bastırdı. Bu koordineli değişimler, pramipeksolün Nrf2/SLC7A11/GPX4 eksenini güçlendirerek hücrenin antioksidan kalkanını tam olarak ihtiyaç duyulan yerde yeniden inşa ettiğini düşündürüyor.
Gelecekteki inme bakımına ne anlama gelebilir?
Bir arada değerlendirildiğinde bulgular, pramipeksolün restorasyon sonrası oluşan oksidatif fırtınaya karşı sinir hücrelerinin dayanmasına yardımcı olduğunu; bunun başlıca mekanizmasının ferroptozisi engellemek ve mitokondriyal işlevi korumak olduğunu gösteriyor. Bu çalışmalar kültürlenmiş hücrelerde yapılmış olup hasta verilerini içermese de, mevcut bir beyin ilacını inmeye yeniden amaçlamanın ümit verici bir yoluna işaret ediyor: pramipeksolün yalnızca dopamin sinyalini etkilemesinden öte, Nrf2/SLC7A11/GPX4 yolu aracılığıyla demir yönetimini ve zar bütünlüğünü stabilize etmek için kullanılabileceği fikri. Benzer koruyucu etkiler hayvan modellerinde ve klinik çalışmalarda doğrulanabilirse, pramipeksol veya ilişkili bileşikler bir gün iskemik inme sonrası kalıcı beyin hasarını azaltmak amacıyla reperfüzyon tedavilerine eklenebilir.
Atıf: Zhang, L., Kang, X., Wang, Q. et al. Pramipexole alleviates ferroptosis in HT22 cells induced by oxygen–glucose deprivation/reoxygenation via the Nrf2/SLC7A11/GPX4 pathway. Sci Rep 16, 11134 (2026). https://doi.org/10.1038/s41598-026-40289-w
Anahtar kelimeler: iskemik inme, ferroptozis, pramipeksol, nöronal koruma, oksidatif stres