Clear Sky Science · it
Il pramipexolo attenua la ferroptosi nelle cellule HT22 indotta da deprivazione/riperfusione di ossigeno‑glucosio tramite la via Nrf2/SLC7A11/GPX4
Perché è importante proteggere le cellule cerebrali dopo un ictus
Quando una persona subisce un ictus ischemico, un coagulo interrompe l’apporto di ossigeno e zucchero a una parte del cervello. I medici intervengono con urgenza per riaprire il vaso ostruito, ma paradossalmente il ritorno improvviso del sangue può danneggiare le cellule cerebrali già fragili. Questo studio indaga se il pramipexolo, un farmaco già impiegato per il morbo di Parkinson, possa proteggere i neuroni da questa seconda ondata di danno calmando una forma di morte cellulare recentemente descritta, legata al ferro e alla perossidazione ossidativa incontrollata.
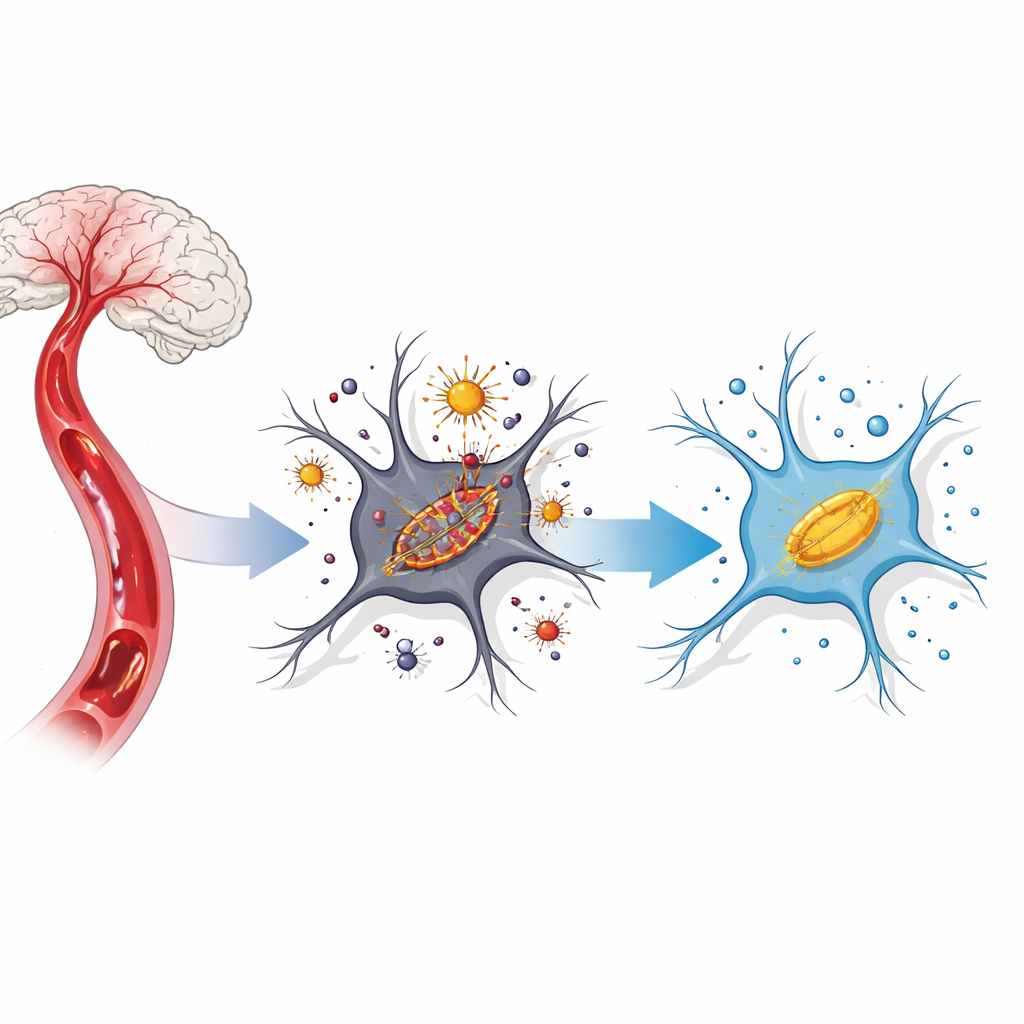
Una reazione a catena dannosa all’interno delle cellule cerebrali
Dopo il blocco e il ripristino del flusso sanguigno, le cellule cerebrali subiscono una tempesta di stress chimico. Il ferro che normalmente è sequestrato diventa libero all’interno della cellula e reagisce con l’ossigeno generando molecole aggressive note come specie reattive dell’ossigeno. Queste attaccano le membrane cellulari ricche di lipidi, in particolare nei piccoli organelli energetici chiamati mitocondri. Gli scienziati definiscono ora questa morte cellulare guidata dal ferro e focalizzata sulle membrane “ferroptosi”. Nei modelli di ictus la ferroptosi si manifesta quando il ferro si accumula, gli antiossidanti protettivi diminuiscono e i mitocondri risultano rimpiccioliti e disfunzionali.
Testare il pramipexolo in un modello di laboratorio simile all’ictus
Per mimare quanto avviene durante un ictus e il trattamento successivo, i ricercatori hanno usato cellule nervose ippocampali murine (cellule HT22) e le hanno temporaneamente private di ossigeno e glucosio prima di ripristinare condizioni normali. Questo modello di deprivazione/riperfusione di ossigeno‑glucosio riproduce molte caratteristiche del danno da ischemia‑riperfusione. Il gruppo ha esposto le cellule a diverse dosi e tempi di somministrazione del pramipexolo e ha misurato la sopravvivenza, la salute mitocondriale, i livelli di ferro, le specie reattive dell’ossigeno e i principali sistemi antiossidanti. Hanno inoltre utilizzato erastin, una sostanza chimica che induce specificamente la ferroptosi, per verificare se il pramipexolo potesse contrastare direttamente questo processo.
Come il farmaco ristabilisce l’equilibrio nella cellula
In assenza di protezione, il trattamento simile all’ictus riduceva la sopravvivenza cellulare, alterava il potenziale di membrana mitocondriale, aumentava ferro e specie reattive dell’ossigeno e deplezionava il glutatione, l’antiossidante, insieme all’enzima GPX4 che ne dipende. Al microscopio elettronico i mitocondri apparivano più piccoli e scuri, in linea con i segni della ferroptosi. Il pramipexolo, in particolare a dose moderata somministrata durante la fase di riperfusione, ha invertito molte di queste alterazioni: le cellule mostravano migliore sopravvivenza, i mitocondri mantenevano forma e potenziale elettrico, ferro e ossidanti diminuivano e glutatione e attività di GPX4 si ripristinavano. Benefici simili sono stati osservati quando le cellule erano danneggiate da erastin, rafforzando l’ipotesi che il pramipexolo agisca limitando la ferroptosi piuttosto che soltanto come antiossidante generale.
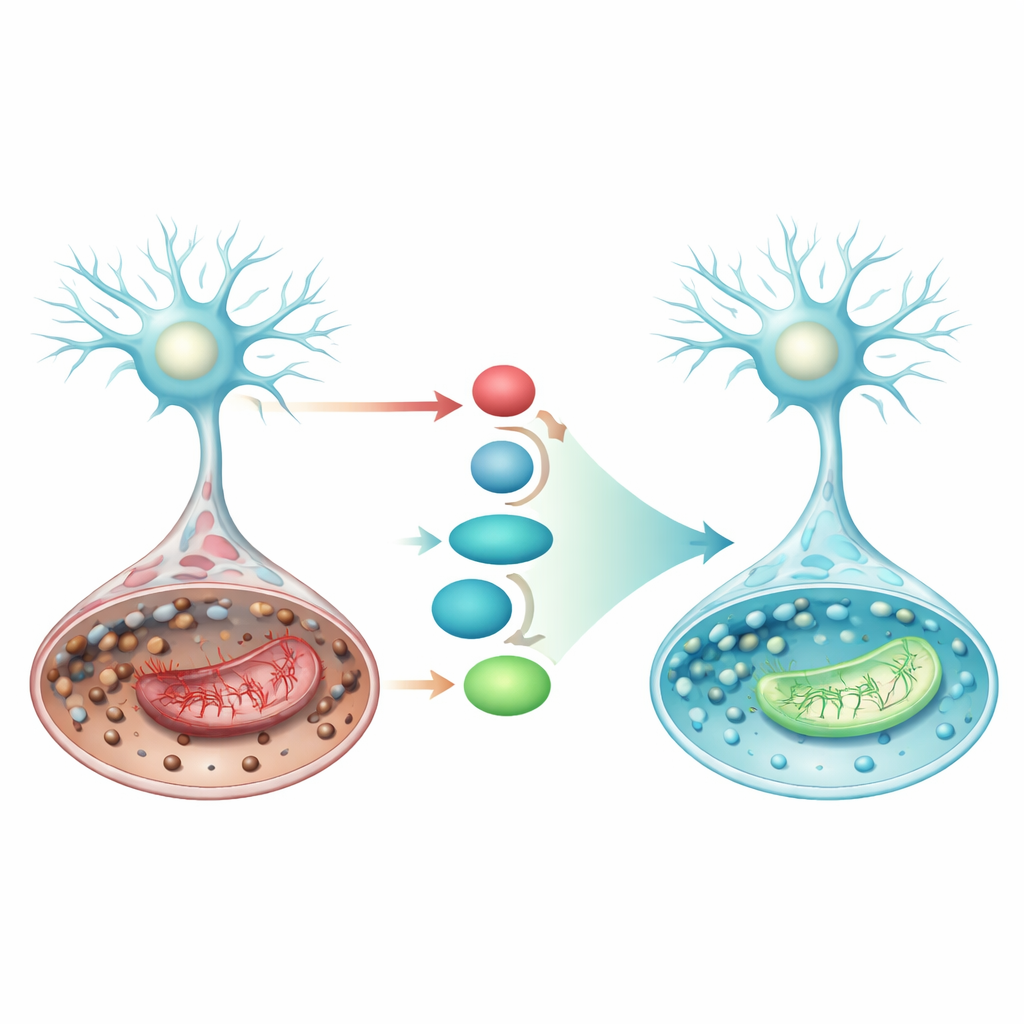
Attivare una via di difesa interna
Lo studio si è inoltre concentrato su una linea di difesa cellulare intrinseca che coinvolge la proteina Nrf2 e i suoi effettori a valle. Quando è attivato, Nrf2 si sposta nel nucleo cellulare e aumenta la produzione di SLC7A11, un trasportatore che porta il materiale necessario per sintetizzare il glutatione, e di GPX4, l’enzima che utilizza il glutatione per neutralizzare i perossidi lipidici. Nella condizione simile all’ictus, i livelli di SLC7A11 e GPX4 diminuivano, favorendo la ferroptosi. Il pramipexolo aumentava significativamente Nrf2, SLC7A11 e GPX4 sia a livello proteico che trascrizionale e, allo stesso tempo, riduceva p53, una proteina che può spingere ulteriormente le cellule verso la ferroptosi e il cedimento mitocondriale. Questi cambiamenti coordinati suggeriscono che il pramipexolo rinforzi l’asse Nrf2/SLC7A11/GPX4, ricostruendo lo scudo antiossidante proprio dove è più necessario.
Cosa potrebbe significare per la cura dell’ictus in futuro
Nel complesso, i risultati mostrano che il pramipexolo aiuta i neuroni a resistere alla tempesta ossidativa che segue il ripristino del flusso sanguigno, principalmente bloccando la ferroptosi e preservando la funzione mitocondriale. Pur essendo lavoro condotto in cellule in coltura e non in pazienti, apre la strada a un promettente riposizionamento di un farmaco cerebrale esistente per l’ictus: non solo per modulare la segnalazione dopaminergica, ma per stabilizzare la gestione del ferro e l’integrità delle membrane attraverso la via Nrf2/SLC7A11/GPX4. Se una protezione analoga fosse confermata in modelli animali e studi clinici, il pramipexolo o composti affini potrebbero un giorno essere aggiunti alle terapie di riperfusione per ridurre il danno cerebrale residuo dopo un ictus ischemico.
Citazione: Zhang, L., Kang, X., Wang, Q. et al. Pramipexole alleviates ferroptosis in HT22 cells induced by oxygen–glucose deprivation/reoxygenation via the Nrf2/SLC7A11/GPX4 pathway. Sci Rep 16, 11134 (2026). https://doi.org/10.1038/s41598-026-40289-w
Parole chiave: ictus ischemico, ferroptosi, pramipexolo, protezione neuronale, stress ossidativo