Clear Sky Science · es
Pramipexol alivia la ferroptosis en células HT22 inducida por privación de oxígeno y glucosa/reoxigenación a través de la vía Nrf2/SLC7A11/GPX4
Por qué importa proteger las células cerebrales tras un ictus
Cuando una persona sufre un ictus isquémico, un coágulo interrumpe el suministro de oxígeno y glucosa a una zona del cerebro. Los médicos actúan con urgencia para reabrir el vaso obstruido, pero paradójicamente la rápida restitución del flujo sanguíneo puede dañar las células cerebrales vulnerables. Este estudio investiga si el pramipexol, un fármaco ya usado en la enfermedad de Parkinson, puede proteger a las neuronas de esta segunda oleada de daño al frenar una forma de muerte celular recientemente descrita, vinculada al hierro y a la oxidación descontrolada.
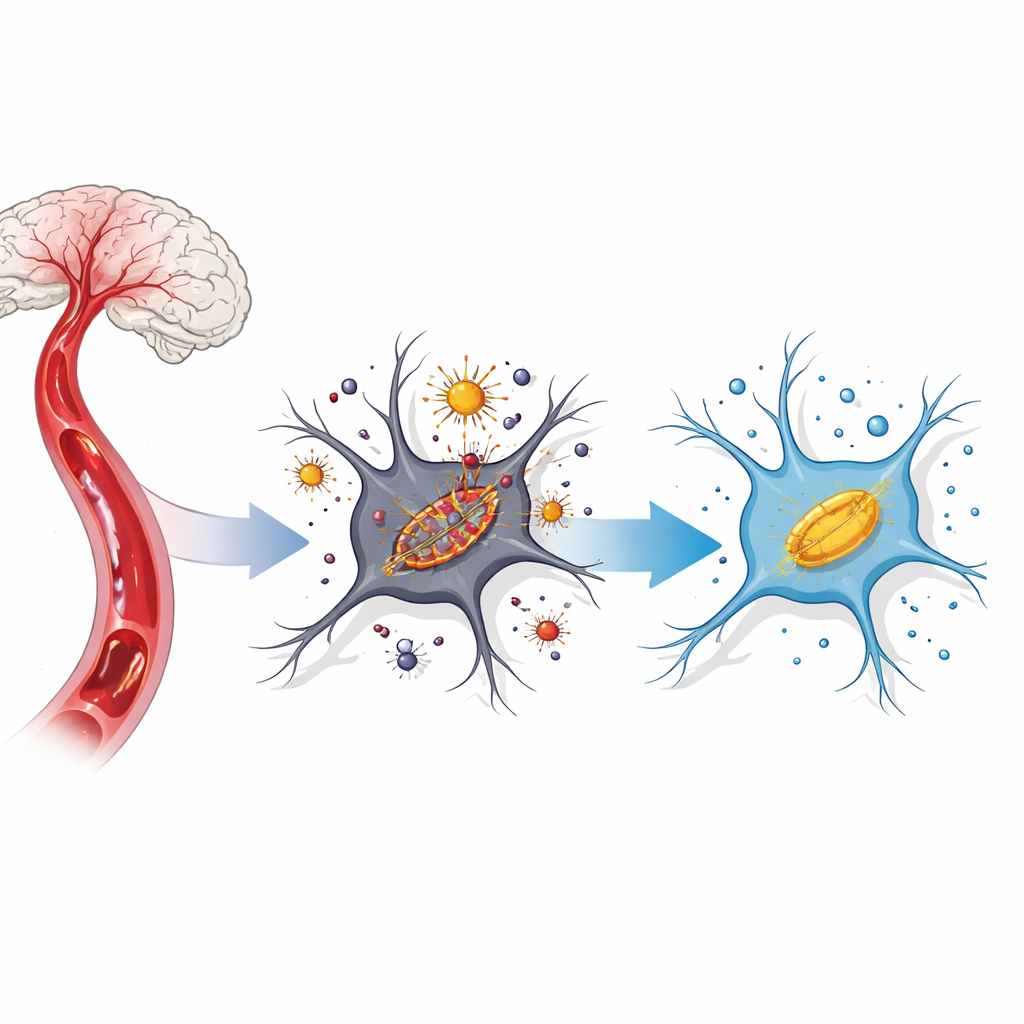
Una reacción en cadena dañina dentro de las células cerebrales
Tras la interrupción y posterior restauración del flujo sanguíneo, las células cerebrales sufren una tormenta de estrés químico. El hierro que normalmente está secuestrado queda libre dentro de la célula y reacciona con el oxígeno para generar moléculas agresivas conocidas como especies reactivas de oxígeno. Éstas atacan las membranas ricas en lípidos, especialmente en las pequeñas centrales llamadas mitocondrias. Los científicos denominan ahora a esta muerte celular dirigida por hierro y centrada en membranas «ferroptosis». En modelos de ictus, la ferroptosis aparece cuando el hierro se acumula, disminuyen los antioxidantes protectores y las mitocondrias se encogen y funcionan mal.
Evaluación del pramipexol en un modelo de laboratorio similar al ictus
Para reproducir lo que ocurre durante un ictus y su tratamiento, los investigadores usaron células nerviosas del hipocampo de ratón (células HT22) y las privaron brevemente de oxígeno y glucosa antes de restaurar las condiciones normales. Este modelo de privación de oxígeno y glucosa/reoxigenación recrea muchas características de la lesión por isquemia–reperfusión. El equipo expuso las células a distintas dosis y tiempos de pramipexol y midió la supervivencia, la salud mitocondrial, los niveles de hierro, las especies reactivas de oxígeno y los principales sistemas antioxidantes. También emplearon erastina, un compuesto que desencadena específicamente la ferroptosis, para comprobar si el pramipexol podía contrarrestar este proceso de forma directa.
Cómo el fármaco restaura el equilibrio dentro de las células
Sin protección, el tratamiento similar a un ictus redujo la supervivencia celular, alteró el potencial de membrana mitocondrial, aumentó el hierro y las especies reactivas de oxígeno, y agotó la molécula antioxidante glutatión junto con la enzima GPX4 que depende de él. Bajo el microscopio electrónico, las mitocondrias parecían más pequeñas y oscuras, coincidiendo con los rasgos de la ferroptosis. El pramipexol, especialmente a una dosis moderada administrada durante la fase de reoxigenación, revirtió muchos de estos cambios: las células sobrevivieron más, las mitocondrias conservaron su forma y carga eléctrica, disminuyeron el hierro y los oxidantes, y el glutatión y la actividad de GPX4 se recuperaron. Se observaron beneficios similares cuando las células fueron dañadas por erastina, lo que refuerza la hipótesis de que el pramipexol actúa restringiendo la ferroptosis y no solo mediante una antioxidación general.
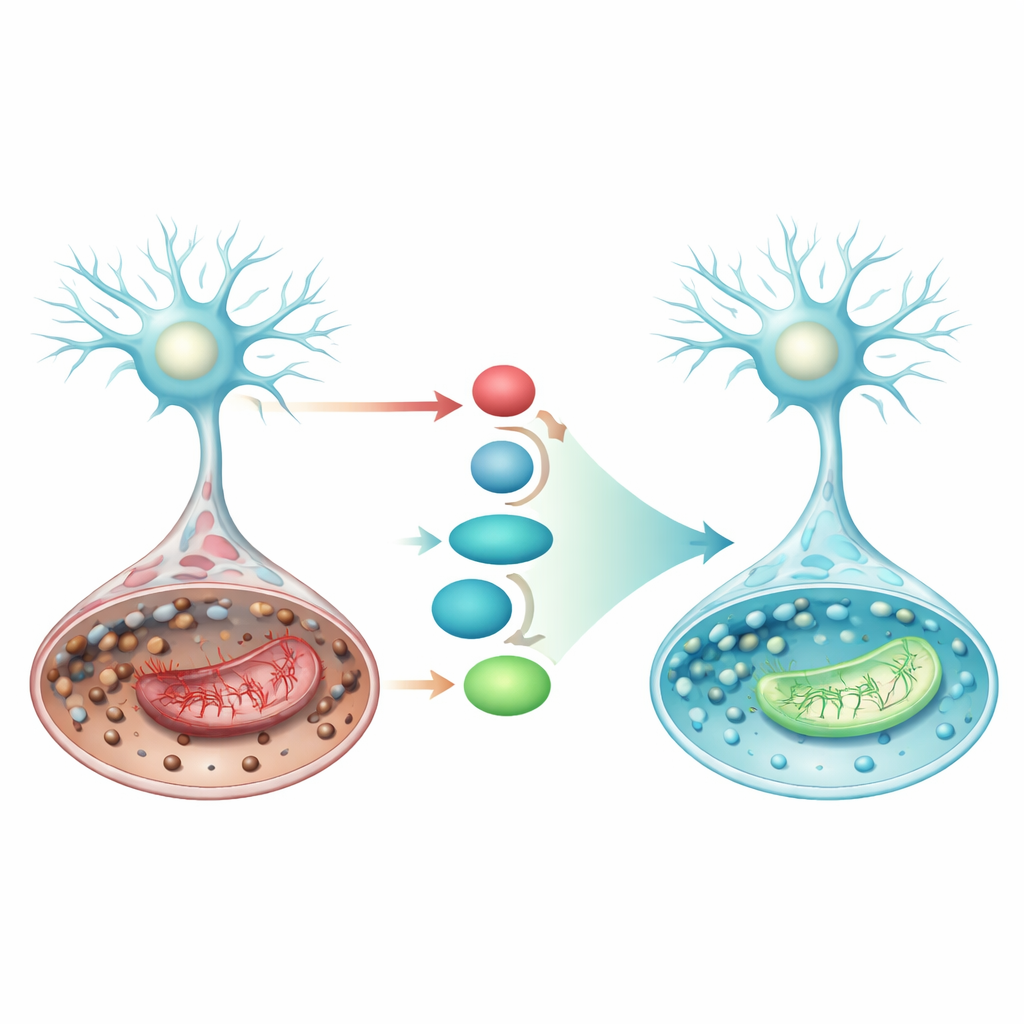
Activación de una vía de defensa interna
El estudio también se centró en una línea de defensa celular integrada que involucra la proteína Nrf2 y sus socios aguas abajo. Cuando se activa, Nrf2 se traslada al núcleo celular y aumenta la producción de SLC7A11, un transportador que aporta materia prima para el glutatión, y de GPX4, la enzima que utiliza el glutatión para neutralizar peróxidos lipídicos. En la condición similar al ictus, los niveles de SLC7A11 y GPX4 cayeron, inclinando a las células hacia la ferroptosis. El pramipexol aumentó de forma marcada Nrf2, SLC7A11 y GPX4 tanto a nivel de proteína como de transcripción y, al mismo tiempo, atenuó p53, una proteína que puede empujar a las células aún más hacia la ferroptosis y el fallo mitocondrial. Estos cambios coordinados sugieren que el pramipexol fortalece el eje Nrf2/SLC7A11/GPX4, reconstruyendo el escudo antioxidante celular exactamente donde más se necesita.
Qué podría significar esto para la atención del ictus en el futuro
En conjunto, los hallazgos muestran que el pramipexol ayuda a las neuronas a resistir la tormenta oxidativa que sigue a la restauración del flujo sanguíneo, principalmente al bloquear la ferroptosis y preservar la función mitocondrial. Aunque este trabajo se realizó en cultivos celulares y no en pacientes, apunta a una vía prometedora para reutilizar un fármaco cerebral existente en el ictus: utilizarlo no solo para modular la señalización dopaminérgica, sino para estabilizar el manejo del hierro y la integridad de las membranas a través de la vía Nrf2/SLC7A11/GPX4. Si una protección similar se confirma en modelos animales y ensayos clínicos, el pramipexol o compuestos relacionados podrían algún día añadirse a las terapias de reperfusión para reducir el daño cerebral persistente tras un ictus isquémico.
Cita: Zhang, L., Kang, X., Wang, Q. et al. Pramipexole alleviates ferroptosis in HT22 cells induced by oxygen–glucose deprivation/reoxygenation via the Nrf2/SLC7A11/GPX4 pathway. Sci Rep 16, 11134 (2026). https://doi.org/10.1038/s41598-026-40289-w
Palabras clave: ictus isquémico, ferroptosis, pramipexol, protección neuronal, estrés oxidativo