Clear Sky Science · ar
بريمبيكسول يخفف الفِرُوپتوزيس في خلايا HT22 المستحثة بنقص الأكسجين–الغلوكوز/إعادة الأكسجة عبر مسار Nrf2/SLC7A11/GPX4
لماذا تهم حماية خلايا الدماغ بعد السكتة
عند حدوث سكتة إقفارية، يحرم جلطة دموية جزءاً من الدماغ من الأكسجين والسكّر. يعمل الأطباء بسرعة لإعادة فتح الوعاء المسدود، لكن المفارقة أن عودة الدم المفاجئة قد تضر بدورها بالخلايا الدماغية الهشة. تستقصي هذه الدراسة ما إذا كان بريمبيكسول، وهو دواء مستخدم بالفعل في مرض باركنسون، قادرًا على حماية الخلايا العصبية من موجة الضرر الثانية هذه من خلال تهدئة شكل حديث الاكتشاف من موت الخلايا المرتبط بالحديد والأكسدة المفرطة.
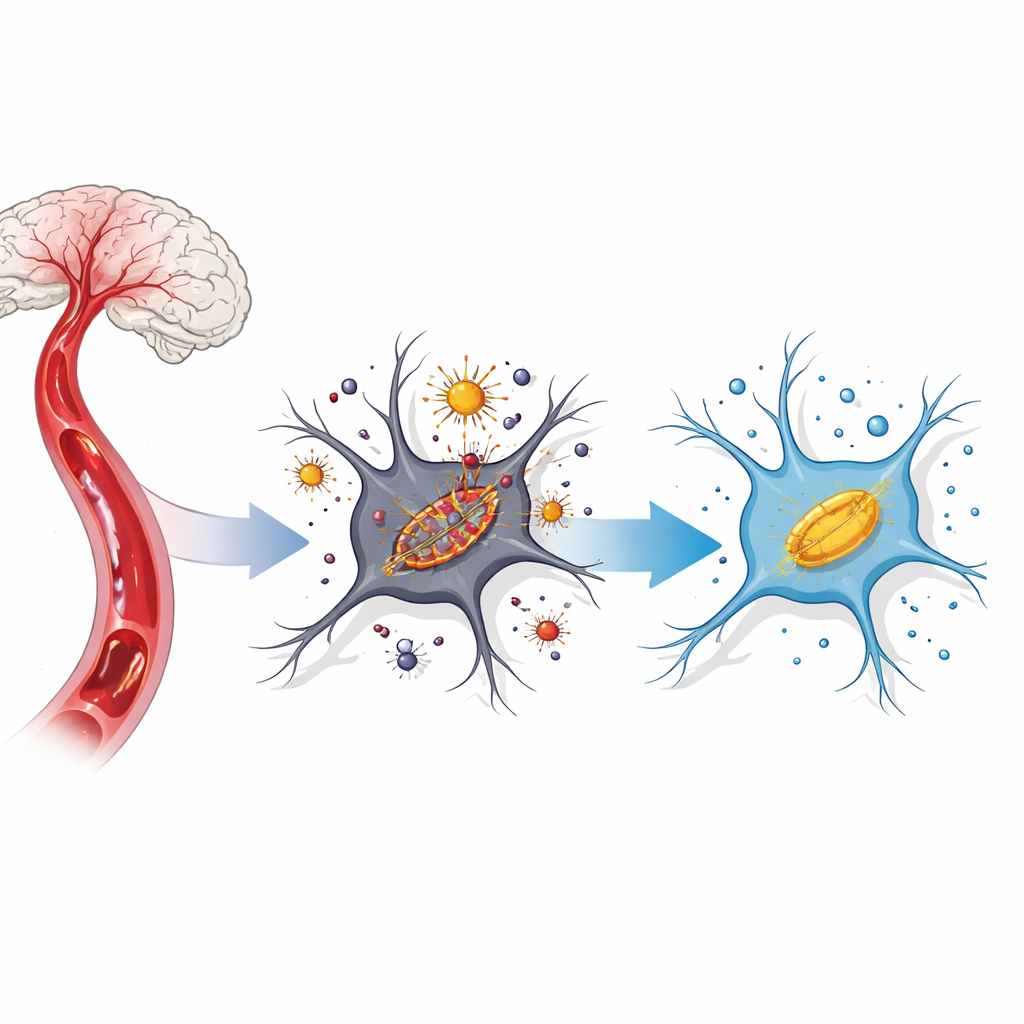
سلسلة تفاعلات ضارة داخل خلايا الدماغ
بعد انقطاع تدفّق الدم ثم عودته، تتعرّض خلايا الدماغ لعاصفة من الضغوط الكيميائية. يصبح الحديد الذي يكون عادة محتبسًا داخل الخلية سائلاً ويتفاعل مع الأكسجين لتوليد جزيئات عدوانية تعرف بجذور الأكسجين التفاعلية. تهاجم هذه الجزيئات أغشية الخلايا الغنية بالدهون، لا سيما في الميتوكوندريا الصغيرة. يطلق العلماء الآن على هذا النوع من موت الخلايا الذي يقوده الحديد والمركز على الأغشية اسم «الفِرُوپتوزيس». في نماذج السكتة، يظهر الفِرُوپتوزيس عندما يتراكم الحديد، وتهبط مضادات الأكسدة الواقية، وتصبح الميتوكوندريا منكمشة ومعطلة الوظيفة.
اختبار بريمبيكسول في نموذج مخبري يشبه السكتة
لمحاكاة ما يحدث أثناء السكتة والعلاج اللاحق، استخدم الباحثون خلايا عصبية من الحُصين الفأرية (خلايا HT22) وحرمّوها مؤقتًا من الأكسجين والغلوكوز قبل إعادة الظروف الطبيعية. يُعيد نموذج نقص الأكسجين–الغلوكوز/إعادة الأكسجة هذا العديد من سمات إصابة الإقفار–إعادة التروية. عرض الفريق الخلايا لجرعات وتوقيتات مختلفة من بريمبيكسول وقاسوا النجاة، وصحة الميتوكوندريا، ومستويات الحديد، وجذور الأكسجين التفاعلية، وأنظمة مضادات الأكسدة الرئيسية. استخدموا أيضًا الإراستين، وهو مركب يحفز الفِرُوپتوزيس بشكل خاص، لمعرفة ما إذا كان بريمبيكسول يستطيع مواجهة هذه العملية مباشرةً.
كيف يعيد الدواء التوازن داخل الخلايا
بدون حماية، أدى العلاج الشبيه بالسكتة إلى انخفاض بقاء الخلايا، واضطراب فرق الجهد الغشائي في الميتوكوندريا، وزيادة الحديد وجذور الأكسجين التفاعلية، واستنزاف جزيء الجلوتاثيون المناعي بالإضافة إلى إنزيم GPX4 المعتمد عليه. تحت المجهر الإلكترونّي، بدت الميتوكوندريا أصغر وأكثر قتامة، بما يتوافق مع سمات الفِرُوپتوزيس. عكس بريمبيكسول، لا سيما عند جرعة معتدلة أعطيت أثناء مرحلة إعادة الأكسجة، العديد من هذه التغيرات: تحسّن بقاء الخلايا، وحافظت الميتوكوندريا على شكلها وشحنها الكهربائية، وانخفضت مستويات الحديد والمؤكسدات، وانتعشت مستويات الجلوتاثيون ونشاط GPX4. لوحظت فوائد مماثلة عندما تضررت الخلايا بالإراستين، مما يقوّي الفرضية بأن بريمبيكسول يعمل بكبح الفِرُوپتوزيس وليس من خلال مضادات أكسدة عامة فقط.
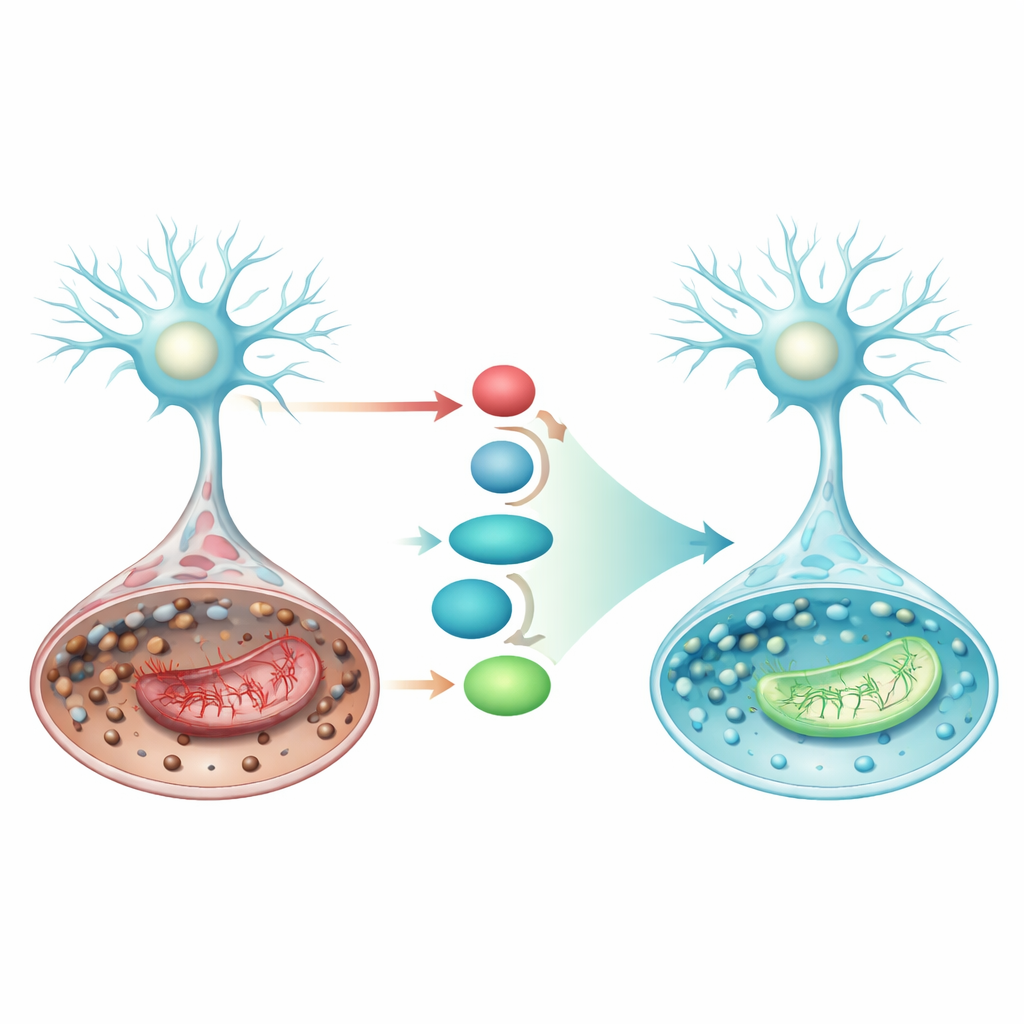
تشغيل مسار دفاعي داخلي
ركزت الدراسة أيضًا على خط دفاع خلوي مدمج يشمل البروتين Nrf2 وشركاءه التاليين. عند تفعيله، ينتقل Nrf2 إلى نواة الخلية ويعزّز إنتاج SLC7A11، وهو ناقل يجلب المواد الخام لتكوين الجلوتاثيون، وGPX4، الإنزيم الذي يستخدم الجلوتاثيون لتحييد البيروكسيدات الدهنية. في الحالة الشبيهة بالسكتة، انخفضت مستويات SLC7A11 وGPX4، مما ميّل الخلايا نحو الفِرُوپتوزيس. زاد بريمبيكسول بقوة من Nrf2 وSLC7A11 وGPX4 على مستوى البروتين والجين، وفي الوقت نفسه خفّض من p53، وهو بروتين يمكن أن يدفع الخلايا أكثر نحو الفِرُوپتوزيس وفشل الميتوكوندريا. تشير هذه التحولات المنسقة إلى أن بريمبيكسول يقوّي محور Nrf2/SLC7A11/GPX4، معيدًا بناء الدرع المضاد للأكسدة في الخلية تمامًا حيث يلزم.
ماذا قد يعني ذلك لرعاية السكتة مستقبلًا
تجتمع الأدلة لتظهر أن بريمبيكسول يساعد الخلايا العصبية على تحمل العاصفة التأكسدية التي تلي عودة تدفّق الدم، وذلك أساسًا عن طريق حجب الفِرُوپتوزيس والحفاظ على وظيفة الميتوكوندريا. رغم أن العمل أُنجز في خلايا مزروعة في المختبر وليس في مرضى، فإنه يشير إلى طريقة واعدة لإعادة استخدام دواء دماغي قائم للسكتة: استخدامه ليس فقط لتعديل إشارات الدوبامين، بل لاستقرار تعامل الخلايا مع الحديد وسلامة الأغشية عبر محور Nrf2/SLC7A11/GPX4. إذا تأكدت حماية مماثلة في نماذج حيوانية وتجارب سريرية، فقد يُضاف بريمبيكسول أو مركبات ذات صلة يومًا ما إلى علاجات إعادة التروية لتقليل التلف الدماغي المستديم بعد السكتة الإقفارية.
الاستشهاد: Zhang, L., Kang, X., Wang, Q. et al. Pramipexole alleviates ferroptosis in HT22 cells induced by oxygen–glucose deprivation/reoxygenation via the Nrf2/SLC7A11/GPX4 pathway. Sci Rep 16, 11134 (2026). https://doi.org/10.1038/s41598-026-40289-w
الكلمات المفتاحية: السكتة الإقفارية, الفِرُوپتوزيس, بريمبيكسول, حماية الخلايا العصبية, الإجهاد التأكسدي