Clear Sky Science · pl
Pramipeksol łagodzi ferroptozę w komórkach HT22 wywołaną niedoborem tlenu i glukozy/ponownym utlenowaniem poprzez szlak Nrf2/SLC7A11/GPX4
Dlaczego ochrona komórek mózgu po udarze ma znaczenie
Gdy dochodzi do udaru niedokrwiennego, skrzep blokuje dopływ krwi, pozbawiając część mózgu tlenu i cukru. Lekarze działają pilnie, by ponownie udrożnić naczynie, lecz paradoksalnie nagły powrót krwi może sam wyrządzić szkody w wrażliwych komórkach mózgu. W tym badaniu sprawdzono, czy pramipeksol — lek już stosowany w chorobie Parkinsona — może ochronić neurony przed tą drugą falą uszkodzeń, hamując niedawno opisany typ śmierci komórkowej związany z żelazem i wymykającym się spod kontroli utlenianiem.
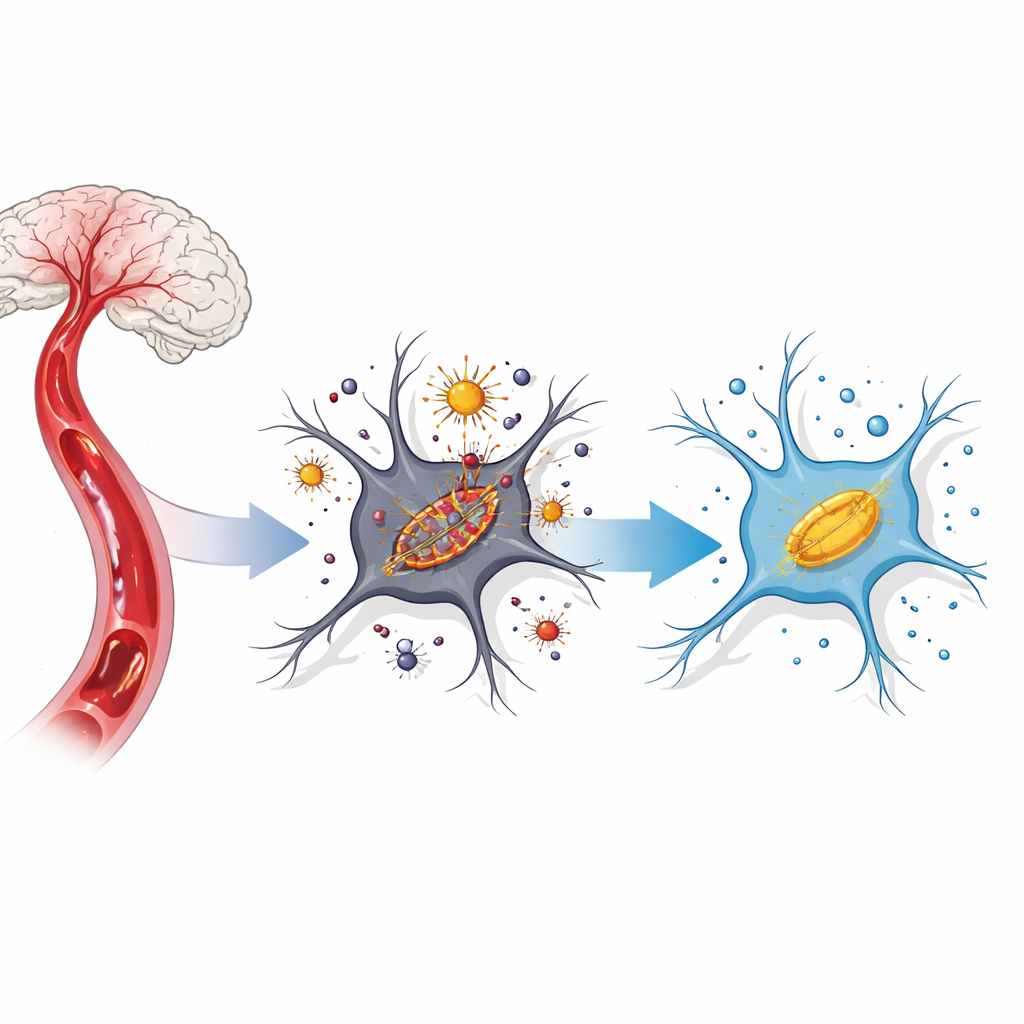
Szkodliwa reakcja łańcuchowa w komórkach mózgu
Po odcięciu i przywróceniu przepływu krwi komórki mózgu doświadczają burzy chemicznego stresu. Żelazo, które zwykle jest związane, staje się luźne wewnątrz komórki i reaguje z tlenem, tworząc agresywne cząsteczki zwane reaktywnymi formami tlenu. Atakują one błony komórkowe bogate w lipidy, zwłaszcza w niewielkich elektrowniach komórkowych — mitochondriach. Naukowcy określają teraz tę żelazozależną, ukierunkowaną na błony śmierć komórkową mianem „ferroptozy”. W modelach udaru ferroptoza pojawia się wraz z nagromadzeniem żelaza, spadkiem mechanizmów antyoksydacyjnych i kurczeniem się oraz dysfunkcją mitochondriów.
Testowanie pramipeksolu w laboratoryjnym modelu przypominającym udar
Aby odwzorować zdarzenia występujące podczas udaru i następnego leczenia, badacze użyli mysich komórek hipokampa (komórek HT22) i krótko pozbawili je tlenu oraz glukozy, po czym przywrócili normalne warunki. Model niedoboru tlenu i glukozy/ponownego utlenowania odtwarza wiele cech uszkodzenia niedokrwienno-reperfuzyjnego. Zespół wystawiał komórki na różne dawki i schematy podawania pramipeksolu oraz mierzył przeżywalność, stan mitochondriów, poziom żelaza, reaktywne formy tlenu i kluczowe systemy antyoksydacyjne. Użyto też erastynu — związku specyficznie indukującego ferroptozę — aby sprawdzić, czy pramipeksol może bezpośrednio przeciwdziałać temu procesowi.
Jak lek przywraca równowagę wewnątrz komórek
Bez ochrony leczenie naśladujące udar zmniejszało przeżywalność komórek, naruszało potencjał błony mitochondrialnej, zwiększało poziomy żelaza i reaktywnych form tlenu oraz wyczerpywało glutation — główną cząsteczkę antyoksydacyjną — wraz z zależną od niego enzymatyczną aktywnością GPX4. W mikroskopie elektronowym mitochondria wyglądały mniejsze i gęstsze, co odpowiada cechom ferroptozy. Pramipeksol, zwłaszcza w umiarkowanej dawce podanej w fazie ponownego utlenowania, odwrócił wiele z tych zmian: komórki lepiej przeżywały, mitochondria zachowały kształt i potencjał elektryczny, spadły poziomy żelaza i utleniaczy, a poziomy glutationu i aktywność GPX4 odbiły się. Podobne korzyści zaobserwowano, gdy uszkodzenie wywołano erastyną, co wzmacnia argument, że pramipeksol działa przez hamowanie ferroptozy, a nie tylko przez ogólne działanie antyoksydacyjne.
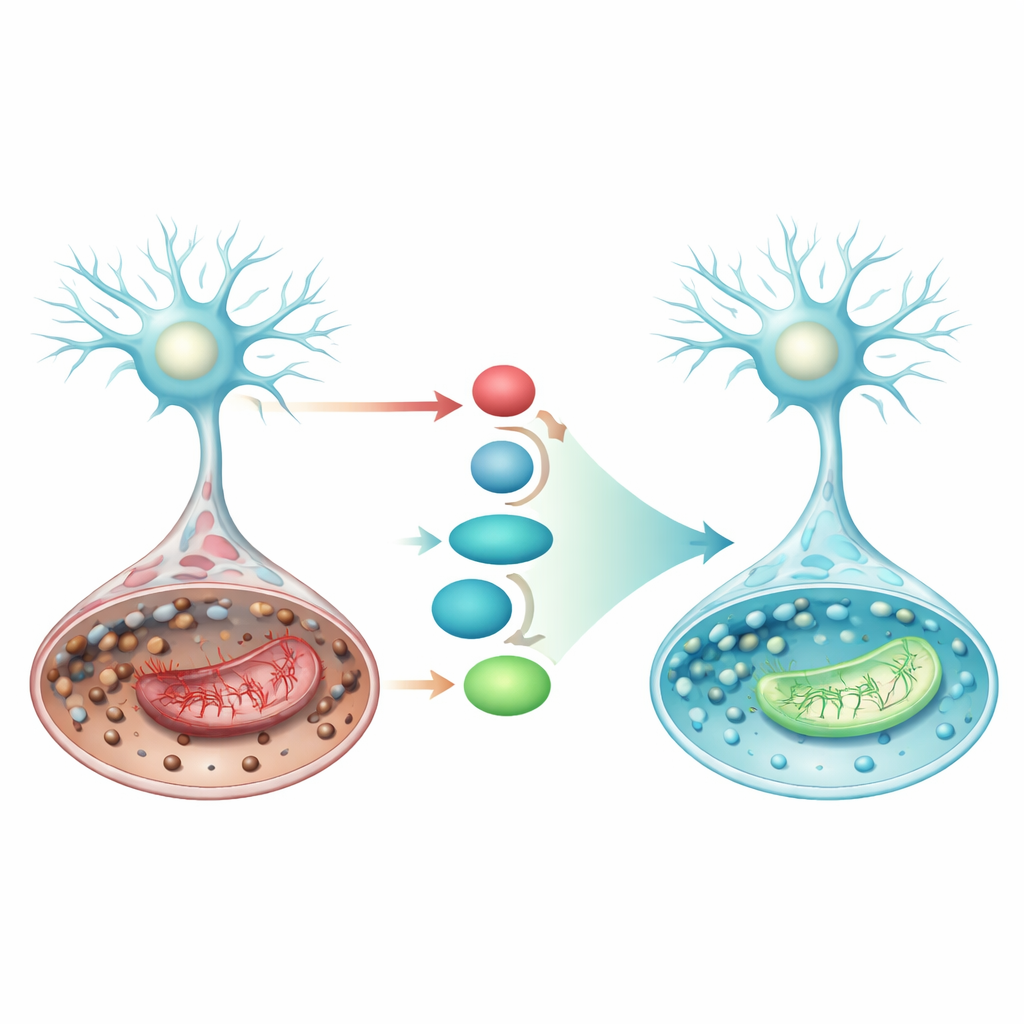
Włączenie wewnętrznej ścieżki obronnej
Badanie skupiło się także na wbudowanej linii obrony komórkowej obejmującej białko Nrf2 i jego efektory. Po aktywacji Nrf2 przemieszcza się do jądra komórkowego i zwiększa produkcję SLC7A11 — transportera dostarczającego substraty do syntezy glutationu — oraz GPX4, enzymu wykorzystującego glutation do neutralizacji nadtlenków lipidowych. W warunkach przypominających udar poziomy SLC7A11 i GPX4 spadały, co skłaniało komórki ku ferroptozie. Pramipeksol silnie podniósł ekspresję Nrf2, SLC7A11 i GPX4 zarówno na poziomie białek, jak i genów, a jednocześnie stłumił p53 — białko, które może popychać komórki w stronę ferroptozy i upadku funkcji mitochondrialnej. Te skoordynowane zmiany sugerują, że pramipeksol wzmacnia oś Nrf2/SLC7A11/GPX4, odbudowując tarczę antyoksydacyjną komórki tam, gdzie jest najbardziej potrzebna.
Co to może oznaczać dla przyszłej opieki po udarze
Podsumowując, wyniki pokazują, że pramipeksol pomaga neuronom przetrwać oksydacyjny sztorm następujący po przywróceniu przepływu krwi, głównie poprzez blokowanie ferroptozy i zachowanie funkcji mitochondriów. Choć prace przeprowadzono w hodowlach komórkowych, a nie u pacjentów, otwierają obiecującą możliwość ponownego zastosowania istniejącego leku mózgowego w udarze: nie tylko do modulowania sygnalizacji dopaminergicznej, lecz także do stabilizacji gospodarki żelazem i integralności błon za pośrednictwem szlaku Nrf2/SLC7A11/GPX4. Jeśli podobna ochrona potwierdzi się w modelach zwierzęcych i badaniach klinicznych, pramipeksol lub pokrewne związki mogłyby w przyszłości zostać dodane do terapii reperfuzyjnych, by zmniejszyć trwałe uszkodzenia mózgu po udarze niedokrwiennym.
Cytowanie: Zhang, L., Kang, X., Wang, Q. et al. Pramipexole alleviates ferroptosis in HT22 cells induced by oxygen–glucose deprivation/reoxygenation via the Nrf2/SLC7A11/GPX4 pathway. Sci Rep 16, 11134 (2026). https://doi.org/10.1038/s41598-026-40289-w
Słowa kluczowe: udar niedokrwienny, ferroptoza, pramipeksol, ochrona neuronów, stres oksydacyjny